A aprovação do anticorpo anti-CCR4 mogamulizumab permite que os doentes com linfoma cutâneo de células T (CTCL) dos subtipos micose fungóide (MF) e síndrome de Sézary (SS) recebam, pela primeira vez, uma intervenção não quimioterapêutica eficaz após uma terapia sistémica prévia. A opção terapêutica inovadora foi capaz de mostrar uma sobrevivência sem progressão significativamente melhorada e uma resposta a longo prazo nos compartimentos do sangue e da pele, em comparação com a terapia comparativa.
O linfoma cutâneo de células T (CTCL) caracteriza-se pela migração de células T degeneradas para a pele [3]. A doença rara mas grave pode afectar a pele, o sangue, os gânglios linfáticos e os compartimentos dos órgãos internos [4,5]. Os subtipos mais frequentes observados são MF e SS, como salientou o Prof. Dr. Reinhard Dummer, de Zurique, [3,5–7]. São típicas as manchas e placas vermelhas, que apresentam semelhanças com outras doenças de pele e, por conseguinte, são frequentemente atribuídas à psoríase ou ao eczema [8]. Por conseguinte, são necessários, em média, dois a sete anos até ao diagnóstico – tempo precioso durante o qual a doença pode progredir [8]. Isto deve-se ao facto de, mesmo nas fases iniciais, até 34% dos doentes com MF sofrerem progressão da doença [7]. Na fase avançada, apenas 52% das pessoas afectadas sobrevivem mais de cinco anos [9].
Elevada procura de uma terapia eficaz
O diagnóstico mais precoce possível de CTCL é crucial para iniciar uma gestão terapêutica eficaz. Para além do aumento do risco de mortalidade, os doentes sofrem também de uma enorme deterioração da sua qualidade de vida, de acordo com o especialista [10]. Por conseguinte, o objectivo da terapia deve ser a remissão nos compartimentos afectados, o alívio dos sintomas e a minimização da progressão da doença [11].
Anticorpo anti-CCR4 aprovado
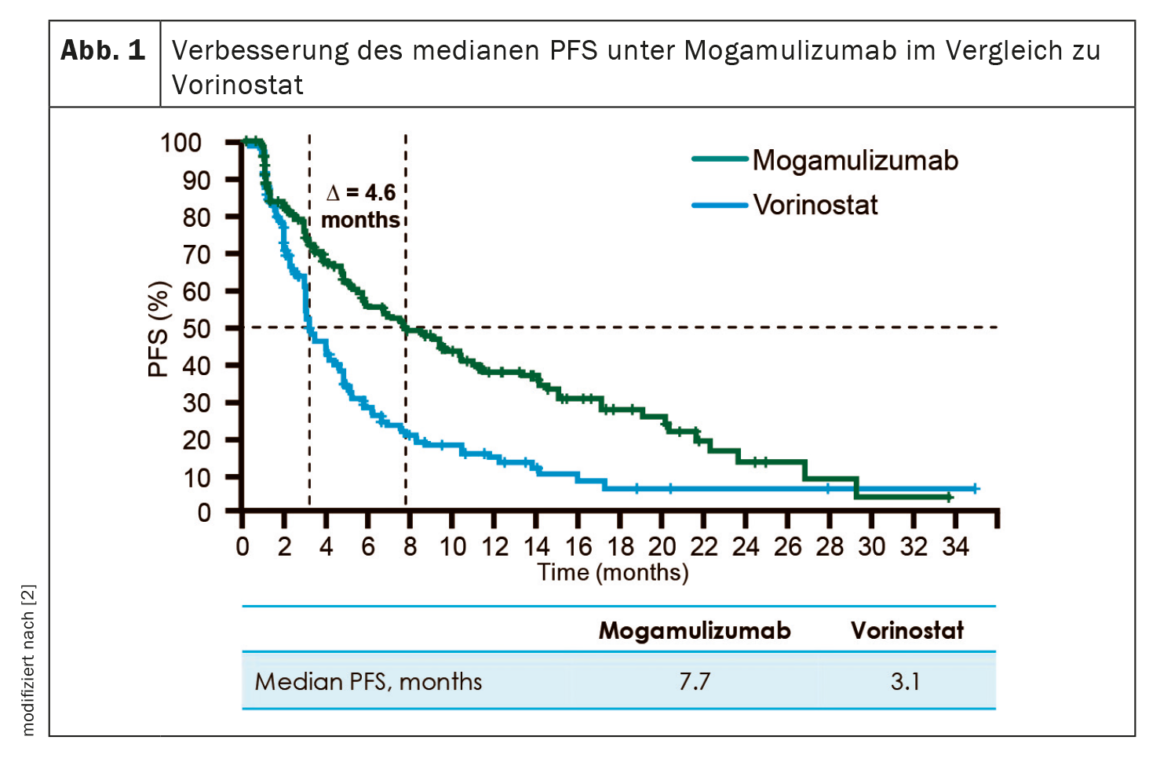
Com mogamulizumab (Poteligeo®), foi agora aprovada na Suíça a primeira terapêutica com anticorpos para doentes adultos com CTCL com MF ou SS que tenham recebido pelo menos uma terapêutica sistémica prévia [1]. A aprovação baseia-se nos resultados do ensaio MAVORIC de fase III [2]. Aleatorizados numa proporção de 1:1, 372 doentes receberam mogamulizumab 1,0 mg/kg i.v. semanalmente durante os primeiros 28 dias e no dia 1 e no dia 15 nos ciclos subsequentes, ou vorinostat 400 mg diariamente (não aprovado na Suíça). Emmanuella Guenova, Lausanne, MD, explicou que o mogamulizumab prolongou a PFS mediana em mais do dobro (7,7 meses vs. 3,1 meses) em comparação com o vorinostat (Fig. 1) [2]. Para além disso, a terapêutica com anticorpos resultou numa resposta global mais elevada – especialmente nos compartimentos da pele (41,9% vs. 15,6%) e do sangue (66,9% vs. 18,4%) [1]. A duração média da resposta foi de 20,6 e 25,5 meses, respectivamente [2]. Além disso, foi alcançada uma melhoria da qualidade de vida em 80% das pessoas afectadas no 11º ciclo de terapia [12]. Globalmente, o tratamento com mogamulizumab foi bem tolerado e apresentou um perfil de segurança controlável [2,13]. As reacções adversas mais frequentemente notificadas foram reacções relacionadas com a infusão (30%) e erupção cutânea (21,5%) [1].
Fonte: Kyowa Kyrin
Literatura:
- Poteligeo® SmPC, a partir de Maio de 2022, em
www.swissmedicinfo.ch. - Kim YH, et al: Mogamulizumab versus vorinostat no linfoma cutâneo de células T previamente tratado (MAVORIC): um ensaio internacional, aberto, aleatório e controlado de fase 3. Lancet Oncol 2018; 19(9): 1192-1204.
- Nicolay JP, et al: CCR4 no linfoma cutâneo de células T: direcionamento terapêutico de um driver patogênico. Eur J Immunol 2021; 51: 1660-1671.
- Organização Nacional para as Doenças Raras: Base de dados de doenças raras: Linfomas cutâneos de células T. Disponível em: https://rarediseases.org/rare-diseases/cutaneous-t-cell-lymphomas (último acesso em 04.11.2022).
- Krejsgaard T, et al. Inflamação maligna no linfoma cutâneo de células T – uma aquisição hostil. Semin Immunopathol 2017;39(3): 269-282.
- Dippel E, et al: S2k – Guideline – Cutaneous Lymphomas (ICD10 C82 – C86) Status: 30.06.2021. Disponível em: www.awmf.org/uploads/tx_szleitlinien/032-027l_S2k_Kutane_Lymphome_2021-12.pdf (último acesso 04.11.2022).
- Agar N, et al.: Resultados de sobrevivência e factores de prognóstico na micose fungóide/síndrome de Sézary: validação da proposta revista de estadiamento da Sociedade Internacional de Linfomas Cutâneos/Organização Europeia para a Investigação e Tratamento do Cancro. J Clin Oncol. 2010;28(31): 4730-4739.
- Fundação CL: um guia para o doente. Disponível em: www.clfoundation.org/sites/default/files/2018-04/a_patients_guide.pdf (último acesso em 04.11.2022)
- Scarisbrick JJ, et al: Estudo do Consórcio Internacional de Linfoma Cutâneo sobre o Resultado em Estádios Avançados de Micose Fungoide e Síndrome de Sézary: Efeito de Marcadores de Prognóstico Específicos na Sobrevivência e Desenvolvimento de um Modelo de Prognóstico. J Clin Oncol 2015; 33(32): 3766-3773.
- Demierre MF, et al. Impacto significativo do linfoma cutâneo de células T na qualidade de vida dos doentes: resultados de um inquérito de 2005 da National Cutaneous Lymphoma Foundation. Cancro 2006; 107(10): 2504-2511.
- Shalabi D, et al: Evasão imunitária e estratégias actuais de imunoterapia na micose fungóide (MF) e na síndrome de Sézary (SS). Chinese Clin Oncol 2019; 8(1): 11.
- Porcu P, et al: Quality of Life Effect of the Anti-CCR4 Monoclonal Antibody Mogamulizumab Versus Vorinostat in Patients With Cutaneous T-cell Lymphoma. Clin Lymphoma Myeloma Leuk. 2021; 21(2): 97-105.
- Afifi S, et al. Uma avaliação da segurança do medicamento mogamulizumab para o tratamento do linfoma cutâneo de células T. Opinião de peritos Drug Saf. 2019; 18(9): 769-776.
InFo ONCOLOGy & HEMATOLOGy 2023; 11(2): 19