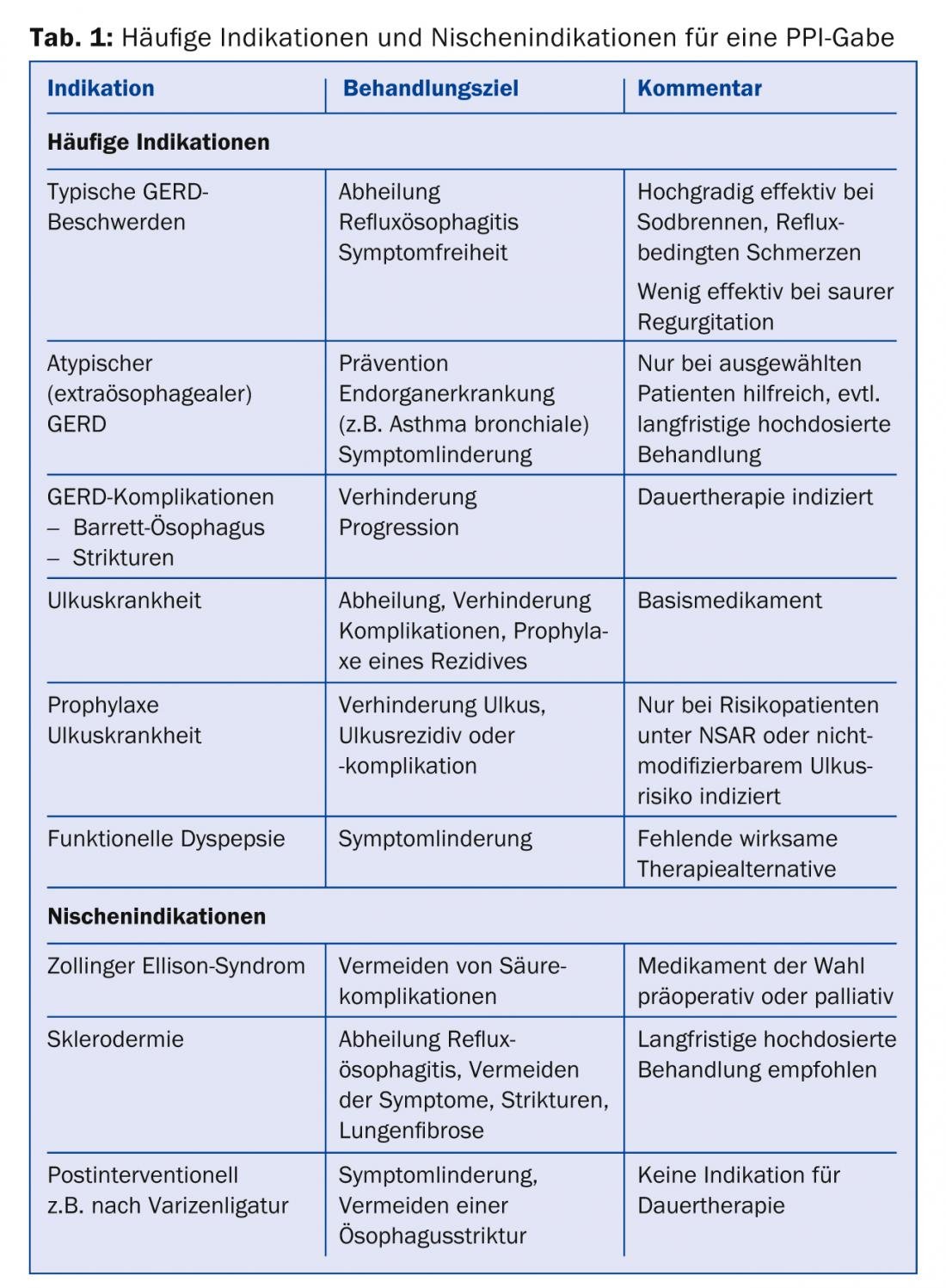
Os inibidores da bomba de prótons (PPIs) são a terceira classe de medicamentos mais utilizados na prática clínica actual a nível mundial, depois dos antibióticos e estatinas (Tab. 1). Estes inibidores de ácido altamente potentes curam e melhoram eficazmente os sintomas da doença do refluxo gastro-esofágico e outras doenças causadas pelo ácido estomacal. No entanto, com a utilização generalizada e frequentemente a longo prazo dos PPI, mesmo pequenos riscos para a saúde são relevantes. A tarefa do médico de família é evitar o uso desnecessário de PPI sem privar os pacientes com boas indicações deste medicamento eficaz. O artigo seguinte dá uma visão geral das indicações e riscos na utilização.
Qual é o papel dos PPI no tratamento da doença do refluxo gastroesofágico (DRGE)? Os PPIs são a classe mais eficaz de medicamentos para a GERD. Devido à disponibilidade de PPIs, a maioria dos pacientes com sintomas típicos de refluxo (por exemplo, azia, regurgitação ácida) pode ser bem tratada pelo médico de clínica geral ou mesmo por auto-medicação com PPIs [1,2]. Esclarecimentos adicionais ou encaminhamento para um gastroenterologista só são necessários para o tratamento dos sintomas de refluxo que são refractários à terapia. Também é importante verificar sempre a indicação de terapia a longo prazo com PPIs em pacientes sem sintomas. Muitas vezes a dose pode ser reduzida e até 40% de todos os pacientes permanecem sem sintomas durante meses, mesmo depois de descontinuarem os PPI [3]. Esta proporção pode ser ainda aumentada através da administração de medicamentos a pedido (por exemplo, antiácidos, alginatos como o Gaviscon®) [2].
Com PPIs, esofagite de refluxo e estrangulamentos pépticos como complicações da DRGE podem curar ou ser evitadas [4]. O esófago de Barrett é outra consequência clinicamente importante do GERD e pode levar ao adenocarcinoma do esófago em cerca de 0,2% por ano [5]. Estudos de controlo de casos sugerem que os PPIs podem impedir a progressão para o carcinoma aqui [6]. Os resultados do grande estudo ASPECT, prospectivo e randomizado, estarão em breve disponíveis para esclarecer definitivamente esta questão [7]. Na nossa opinião, a terapia a longo prazo com um PPI já está indicada para o esófago de Barrett.
As manifestações extra-esofágicas de GERD incluem tosse crónica, rouquidão e sensação de globo. Nestes doentes, a relação entre refluxo e sintomas é menos clara e as queixas de ORL (sinusite crónica, “gotejamento pós-nasal”) bem como as doenças pneumológicas podem contribuir para a patogénese [1]. As taxas de sucesso do tratamento com PPI são correspondentemente mais modestas [8].
Se os sintomas persistirem, o médico de clínica geral tem duas opções: tratamento empírico com PPI ao dobro da dose padrão durante oito a doze semanas, e medição objectiva do pH para determinar a gravidade da exposição ao ácido esofágico e a relação entre os sintomas de refluxo e os sintomas extra-esofágicos [8]. O doente deve ser envolvido nesta decisão. É importante que em caso de tratamento PPI mal sucedido ou medição negativa do pH, o PPI deve ser interrompido.
Úlcera péptica de indicação
Os PPIs são os medicamentos básicos para o tratamento da úlcera péptica e das suas complicações. Assim, na situação de hemorragia, a neutralização do pH gástrico pode activar a coagulação do sangue e limitar a hemorragia [9]. Além disso, a maioria das úlceras gástricas ou duodenais cicatrizam dentro de algumas semanas após a terapia com PPI [10]. Os PPIs também fazem parte da terapia de erradicação do H. pylori. Também aqui, o PPI deve ser interrompido após a úlcera ter sarado e o factor de risco ter sido removido. A terapia PPI contínua para a profilaxia do desenvolvimento de úlceras ou recidiva de úlceras é indicada em doentes de alto risco que tomam AINE e em doentes que já tiveram uma úlcera e têm factores de risco não modificáveis [11].
Indicação de dispepsia funcional
Os PPIs são eficazes no tratamento da dispepsia funcional (FD) em alguns casos e também podem ser dados empiricamente na ausência de sintomas de alarme e após excluir a infecção por H. pylori. Infelizmente, a taxa de sucesso dos PPIs para esta indicação é baixa (“número necessário para tratar”, NNT: 10, em comparação com NNT 2-3 para sintomas típicos de refluxo) [12].
Não-resposta à administração PPI
Nem todos os sintomas de GERD respondem ao tratamento com PPI. Por exemplo, os sintomas de refluxo volumétrico podem ser reduzidos pela medicação no melhor dos casos. Mesmo para pacientes com sintomas típicos de DRGE (Fig. 1), o efeito da PPI não é perfeito.

Embora até 90% de todos os pacientes respondam ao tratamento, cerca de um terço de todos os pacientes em terapia PPI a longo prazo não se tornam completamente livres de sintomas [1,2]. Além disso, um grande número de pacientes com DRGE tomam medicamentos de venda livre, para além do PPI [13]. Sugerimos uma abordagem sequencial no caso de uma resposta insatisfatória ao PPI (Fig. 2) .

Se os sintomas são típicos sob PPI, deve ser experimentada uma preparação de alginato (por exemplo, Gaviscon®). Os alginatos formam uma camada viscosa em frente à entrada do esófago e podem assim impedir o refluxo ácido e não-ácido [14]. Além disso, o PPI poderia ser alterado e/ou a dose aumentada.
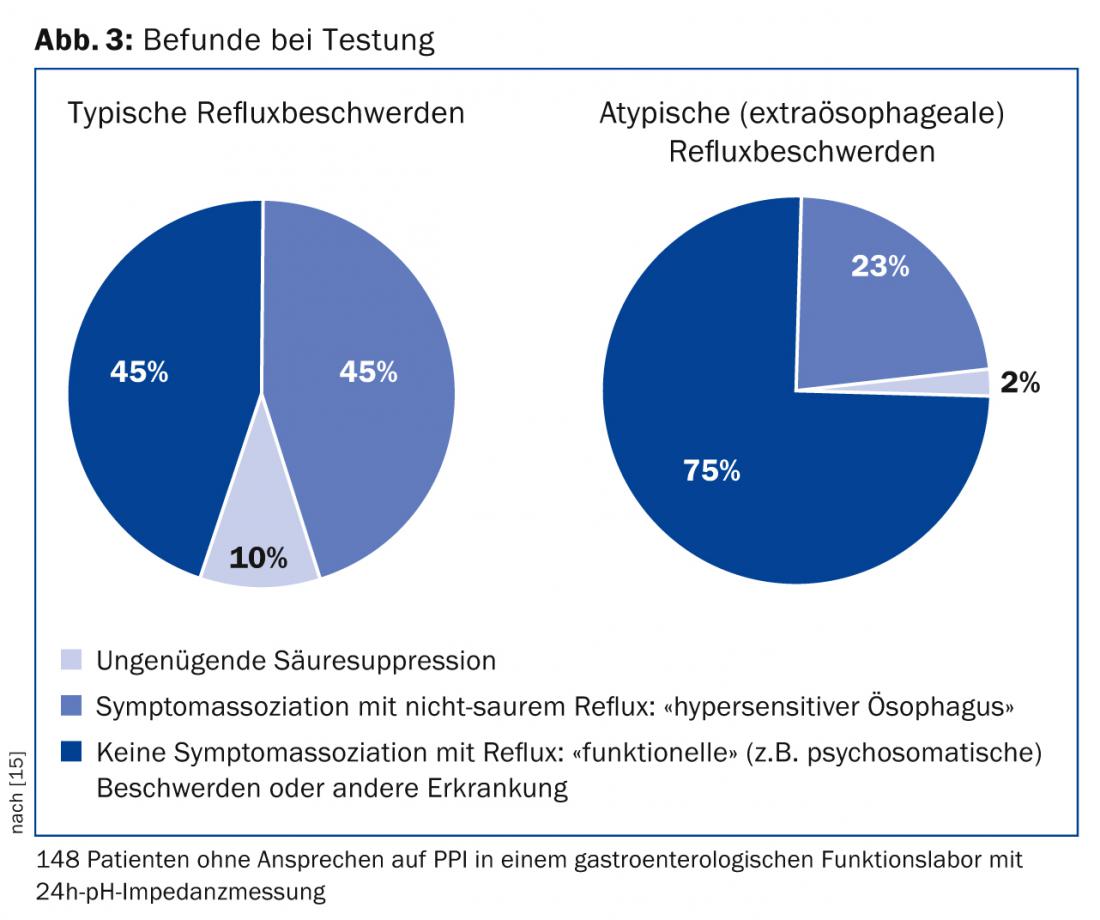
Em caso de sintomas atípicos ou de não resposta à PPI apesar das medidas mencionadas, devem ser realizados mais diagnósticos gastroenterológicos. A primeira indicação é uma gastroscopia para excluir uma úlcera péptica ou neoplasia. Se os resultados forem normais, deve então ser efectuada uma manometria e uma medição da impedância de pH para identificar a causa das queixas [1,2]. Por exemplo, apenas cerca de metade de todos os doentes com “queixas de refluxo” que são encaminhados para um laboratório funcional gastroenterológico têm uma doença de refluxo objectivável (Fig. 3) [15]. Por exemplo, os doentes que sofrem de acalasia são inicialmente mal diagnosticados como doentes com DRGE em cerca de 40% dos casos e tratados com PPI [16].
Um diagnóstico exacto das queixas refractárias permite então um tratamento específico (figs. 2 e 3) . Se o refluxo ácido for confirmado como a causa da queixa, a supressão de ácido deve ser ainda mais optimizada. Na ausência de refluxo patológico, mas na presença de associação sintomática entre refluxo e azia ou dor torácica (o chamado “esófago sensível”), podem ser administrados alginatos para além de PPIs. Além disso, a sensibilidade visceral pode ser modulada com antidepressivos de baixa dose (por exemplo, amitriptilina 25 mg nocté). Na ausência de doença de refluxo e associação de sintomas, o PPI pode ser descontinuado. Em vez disso, uma perturbação de motilidade ou uma perturbação psicossomática deve ser tratada, se necessário, ou devem ser organizados outros diagnósticos.
Ressalto ácido de risco
É a experiência clínica que a azia se agrava muitas vezes brevemente após a descontinuação de uma PPI. Os sintomas de refluxo podem ser desencadeados após a administração de PPI a curto prazo, mesmo em sujeitos anteriormente livres de sintomas [17]. Este efeito de ricochete pode dificultar a descontinuação dos PPIs e contribuir para a administração desnecessária de PPIs [18]. Se os sintomas de ressalto ocorrerem após a descontinuação, o PPI deve ser reduzido gradualmente (por exemplo, uma semana dose única padrão, uma semana meia dose padrão). Além disso, recomendamos antiácidos ou alginatos, conforme necessário, durante o desmame.
Outros riscos de um PPI
Ao contrário dos receios iniciais, os PPIs não aumentam o risco de cancro gástrico [19]. Muitos estudos de controlo de casos encontraram uma associação de risco de cancro com a indicação de tratamento com PPI (DRGE, úlceras gástricas, etc.) mas não com a utilização de PPI [20]. Por outro lado, um PPI pode mascarar sintomas de cancro gástrico. Portanto, a gastroscopia é obrigatória em caso de sintomas de alarme antes do tratamento empírico com PPI e deve ser sempre considerada novamente em caso de efeito de PPI insuficiente.
A perda do efeito antibacteriano do ácido gástrico aumenta o risco de enterite infecciosa com shigella e salmonela, entre outros [21]. Especialmente para doentes hospitalizados ou com necessidade de cuidados, o aumento do risco de infecções por Clostridium difficile (HR 2,5) ou pneumonia (HR 1,4) é provável que seja relevante [22]. Nos doentes com cirrose hepática, as PPIs não podem parar o sangramento da varizes esofágica, mas podem aumentar o risco de peritonite bacteriana espontânea, pelo que não devem ser administradas neste grupo de doentes [23].
As considerações fisiológicas também sugerem uma absorção reduzida de vitamina B12, cálcio, magnésio e ferro com utilização de PPI [24]. Com a abundância actual de alimentos com quantidades suficientes de vitaminas e minerais, este risco raramente é relevante [24]. No entanto, em caso de queixas compatíveis com a subnutrição destas substâncias mencionadas, o controlo deve ser generoso. Estudos da associação também identificaram a osteoporose como uma possível complicação da utilização de PPI a longo prazo (RH para risco de fractura 1,25) [25]. É importante notar que todos estes riscos foram encontrados em estudos de caso-controlo, mas não em grandes ensaios prospectivos aleatórios, pelo que não estão livres da influência de possíveis confundidores.
As interacções medicamentosas dos PPIs e outros riscos estão resumidas no Quadro 2. Uma interacção medicamentosa inicialmente temida entre PPI e clopidogrel foi refutada em estudos recentes. Os PPI, por exemplo, implicam o risco teórico de bloqueio do clopidogrel, uma vez que podem bloquear o citocromo CYP2C19, que é importante para a activação do clopidogrel. No entanto, num grande estudo em que os pacientes receberam clopidogrel sozinho ou juntamente com um PPI após a inserção de um stent coronário, o risco de eventos adversos cardíacos foi exactamente o mesmo em ambos os braços do estudo com menos eventos adversos gastrointestinais com PPI [26]. Assim, a interacção farmacológica do PPI e do clopidogrel não é relevante na prática. Este discurso mostra como as considerações fisiológicas podem ocasionalmente induzir em erro e como a “morbidez” confusa pode fingir interacções relevantes em estudos de caso-controlo.

A indicação adequada é crucial
Apesar de todas as vantagens, é importante alertar contra o uso acrítico destas drogas: As estimativas sugerem que 25-75% de todos os pacientes tratados com PPIs não têm uma indicação adequada. Em séries de casos típicos de pacientes hospitalizados, 20% tomam PPI na admissão, 40% são iniciados com PPI durante a hospitalização e 50% são encontrados com PPI na medicação de alta [27]. Isto é quase sempre sem indicação adequada e sem que na carta de alta seja sugerido um tempo para uma revisão da medicação. Os pacientes hospitalizados frequentemente são assim susceptíveis de serem tratados frequentemente com PPIs também em regime ambulatório [28]. É precisamente este grupo de pacientes que é vulnerável aos problemas acima mencionados.
CONCLUSÃO PARA A PRÁTICA
- A introdução de PPIs como inibidores seguros e eficazes da secreção ácida teve um grande impacto positivo no tratamento de muitas doenças gastro-esofágicas.
- No entanto, é preciso ser avisado contra uma utilização acrítica destes medicamentos.
- Continua a ser a tarefa responsável do GP parar o PPI “desnecessário”, continuar o PPI “necessário”, útil na dose efectiva mais baixa e, sobretudo, distinguir com certeza entre as duas situações.
UM RETENIR
- La mise sur le marché des IPP comme inhibiteurs sûrs et efficaces de la sécrétion d’acide a eu un important effet positif sur le traitement de nombreuses maladies de l’estomac et de l’oesophage.
- Toutefois une mise en garde contre une utilisation irrationnelle de ces médicaments est nécessaire.
- Há um elevado nível de responsabilidade por parte do médico de família em parar as PPIs “inúteis”, em continuar as PPIs “necessárias” nas doses mais eficazes e, sobretudo, em diferenciar as duas situações com precisão.
Prof. Dr. med. Mark Fox
PD Dr. Med. Benjamin Misselwitz
Daniel Pohl, MD
Literatura:
- Fox M, Forgacs I: Doença do refluxo gastro-esofágico. BMJ 2006; 332: 88-93.
- Tytgat GN, et al: Novo algoritmo para o tratamento da doença do refluxo gastro-esofágico. Aliment Pharmacol Ther 2008 Fev 1; 27(3): 249-256.
- Schwizer W, et al: O efeito da infecção por Helicobacter pylori e erradicação em doentes com doença de refluxo gastroesofágico: um estudo multicêntrico paralelo, duplo-cego, controlado por placebo. United European Gastroenterology Journal 2013; 1(4): 226-235.
- Castell DO, et al: Esomeprazol (40 mg) em comparação com lansoprazol (30 mg) no tratamento da esofagite erosiva. Am J Gastroenterol 2002; 97(3): 575-583.
- de Jonge PJ, et al: o esófago de Barrett: epidemiologia, risco de cancro e implicações para a gestão. Trip 2014 Jan; 63(1): 191-202.
- Singh S, et al: Medicamentos supressores de ácido e risco de adenocarcinoma de esófago em doentes com esófago de Barrett: uma revisão sistemática e meta-análise. Trip 2013 12 de Novembro.
- Jankowski J, Sharma P: Artigo de revisão: abordagens ao tratamento do esófago de Barrett – o papel dos inibidores da bomba de prótons e outras intervenções. Aliment Pharmacol Ther 2004 Fev; 19 Suppl 1: 54-59.
- Sifrim D, Barnes N: tosse crónica relacionada com GERD: como identificar pacientes que irão responder à terapia anti-refluxo? J Clin Gastroenterol. 2010 Abr; 44(4): 234-236.
- Sung JJ, et al: Esomeprazol intravenoso para prevenção de úlcera péptica recorrente: um ensaio aleatório. Ann Intern Med 2009 Abr 7; 150(7): 455-464.
- Leodolter A, et al: Uma meta-análise comparando as taxas de erradicação, cura e recaída em doentes com úlcera gástrica ou duodenal associada à Helicobacter pylori-associada. Aliment Pharmacol Ther 2001 Dez; 15(12): 1949-1958.
- Chan FK, Sung JJ: Papel dos supressores ácidos na profilaxia de danos da AINE. Best Pract Res Clin Gastroenterol 2001 Jun; 15(3): 433-445. PubMed PMID: 11403537.
- Wang WH, et al: Effects of proton-pump inhibitors on functional dyspepsia: uma meta-análise de ensaios aleatórios controlados por placebo. Clin Gastroenterol Hepatol. 2007 Fev; 5(2): 178-185; quiz 40.
- Hungin AP, et al: Revisão sistemática: Padrões de utilização e aderência de inibidores da bomba de protões na doença do refluxo gastroesofágico. Clin Gastroenterol Hepatol 2012 Fev; 10(2): 109-116.
- Sweis R, et al: supressão do refluxo pós-prandial por um alginato formador de jangadas (Gaviscon Advance) em comparação com um simples antiácido documentado por ressonância magnética e monitorização de pH-impedância: avaliação mecanicista em voluntários saudáveis e estudo aleatório, controlado e duplo-cego em doentes com refluxo. Aliment Pharmacol Ther 2013 Jun; 37(11): 1093-1102.
- Mainie I, et al: Refluxo ácido e não ácido em doentes com sintomas persistentes apesar da terapia de supressão de ácido: um estudo multicêntrico utilizando a monitorização combinada de impedância ambulatorial-pH. Gut. 2006 Oct; 55(10): 1398-1402.
- Kessing BF, Bredenoord AJ, Smout AJ: Diagnóstico errado da doença do refluxo gastroesofágico na acalasia. Clin Gastroenterol Hepatol. 2011 Dez; 9(12): 1020-1024.
- Reimer C, et al.: A terapia com inibidores de bomba de prótons induz sintomas relacionados com ácido em voluntários saudáveis após a retirada da terapia. Gastroenterologia 2009; 137(1): 80-87.
- Howden CW, Kahrilas PJ: Editorial: quão “difícil” é retirar o tratamento PPI? Am J Gastroenterol 2010 Jul; 105(7): 1538-1540.
- Klinkenberg-Knol EC, et al: Tratamento omeprazol de longo prazo na doença de refluxo gastroesofágico resistente: eficácia, segurança e influência na mucosa gástrica. Gastroenterologia 2000 Abr; 118(4): 661-669.
- Tamim H, et al.: Associação entre o uso de fármacos supressores de ácidos e o risco de cancro gástrico. Um estudo de caso-controlo aninhado. Drug Saf 2008; 31(8): 675-684.
- Leonard J, Marshall JK, Moayyedi P: Revisão sistemática do risco de infecção entérica em pacientes que tomam a supressão de ácidos. Am J Gastroenterol 2007 Set; 102(9): 2047-2056; quiz 57.
- Howell MD, et al: Iatrogenic gastric acid suppression and the risk of nosocomial Clostridium difficile infection. Arch Intern Med. 2010 10 de Maio; 170(9): 784-790.
- Goel GA, et al: Aumento da taxa de peritonite bacteriana espontânea entre pacientes cirróticos que recebem supressão de ácido farmacológico. Clin Gastroenterol Hepatol 2012 Abr; 10(4): 422-427.
- Pohl D, et al.: Será que precisamos de ácido gástrico? Digestão 2008; 77(3-4): 184-197.
- Gray SL, et al: uso de inibidor da bomba de prótons, fractura da anca, e alteração da densidade mineral óssea em mulheres na pós-menopausa: resultados da Iniciativa de Saúde da Mulher. Arch Intern Med 2010 10 de Maio; 170(9): 765-771.
- Bhatt DL, et al: Clopidogrel com ou sem omeprazol na doença arterial coronária. N Engl J Med 2010 Nov 11; 363(20): 1909-1917.
- Yachimski PS, et al: Inibidores da bomba de prótons para profilaxia da hemorragia nosocomial do tracto gastrointestinal superior: efeito de directrizes padronizadas sobre a prática de prescrição. Arch Intern Med. 2010 10 de Maio; 170(9): 779-783.
- Arasaradnam RP, et al: Auditoria ao inibidor de bomba de prótons (PPI) prescrevendo: estão as directrizes da NICE a ser seguidas? Clin Med 2003 Jul-Aug; 3(4): 387-388.
PRÁTICA DO GP 2014; 9(6): 26-31