Oncotype DX®, MammaPrint® e EndoPredict® são testes de ensaio genético validados com valor prognóstico comprovado. Os testes podem actualmente ser utilizados no carcinoma mamário precoce (luminal A/B) na gama intermédia para ajudar na tomada de decisões. Os ensaios aleatórios prospectivos sobre o valor preditivo dos testes (TailorX, PlanB e MINDACT) estão ainda pendentes. Os custos têm sido cobertos pelas caixas de seguro de saúde desde Janeiro de 2015.
Quais os pacientes que beneficiam de quimioterapia adjuvante e quais os que não beneficiam é uma das questões centrais de todos os conselhos interdisciplinares. Os ensaios actualmente no mercado prometem uma melhor especificidade do que os parâmetros clinicopatológicos convencionais e devem ajudar a evitar quimioterapia desnecessária. Especialmente em pacientes com o chamado perfil de risco intermédio, existe incerteza sobre a terapia, que os ensaios visam eliminar. Até agora, o risco de recorrência tem sido avaliado com base em factores de risco como a biologia do tumor, classificação, propagação do tumor, estado dos gânglios linfáticos e idade. Já no ano 2000, o trabalho de Perou et al. descreveu a heterogeneidade dos tumores e a sua classificação em subtipos moleculares. A formação de clusters de expressão genética resulta nos subtipos intrínsecos tais como luminal (A e B), Her2 enriquecido e basal como. No entanto, dados mais recentes mostram que estes subtipos não são uniformes em si mesmos e, portanto, mostram também prognósticos diferentes. Ao determinar os receptores hormonais, o receptor Her2 e o factor de proliferação Ki67, estes subtipos, classificados como grupos de expressão genética, podem também ser detectados imunohistoquímicamente.
A classificação dos pacientes em Luminal A ou B é imprecisa na gama intermédia de Ki67. Isto pode levar as pacientes com cancro da mama precoce a receberem quimioterapia desnecessariamente.
Que testes existem?
Os testes que se seguem são actualmente os mais utilizados na Europa:
Oncotype DX® (GenomicHealth Inc., Redwood City, EUA): É um teste de prognóstico para doentes com cancro da mama receptor de estrogénio positivo. O teste é realizado utilizando transcrição inversa seguida de PCR quantitativa (RT-qPCR). O tecido é fixado em formalina e incorporado em parafina (FFPE). Os níveis de expressão genética de 21 genes (16 genes de informação e cinco genes de referência) são determinados (Fig. 1).
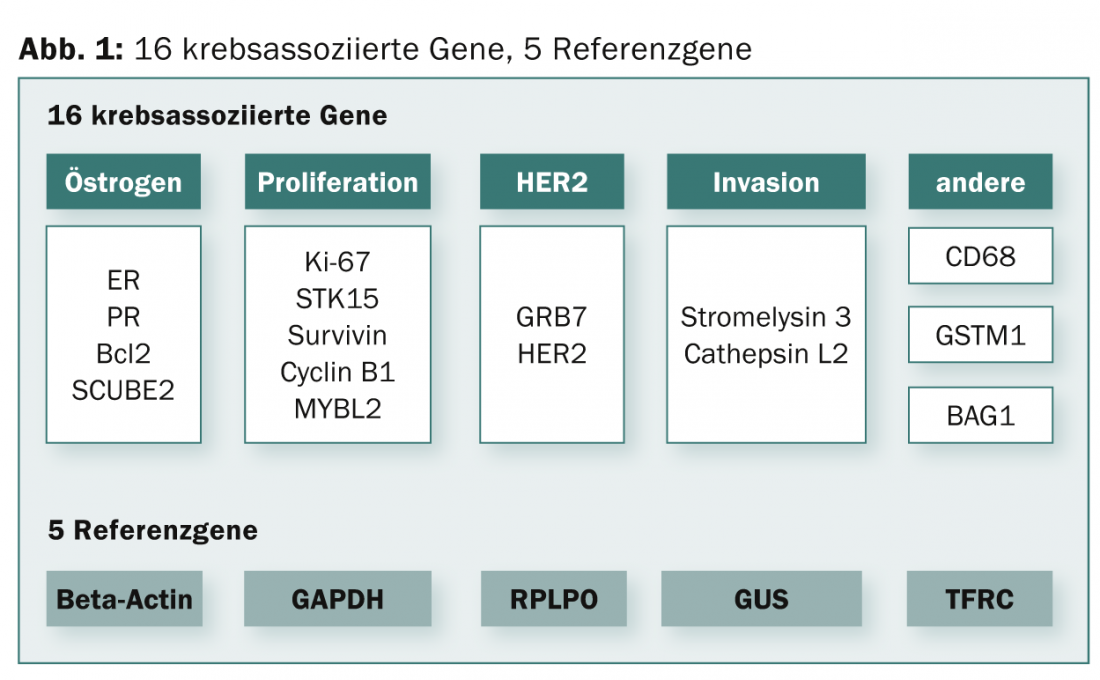
Um algoritmo matemático é então utilizado para calcular a pontuação de recorrência (RS). O RS é uma pontuação prognóstica contínua (escala: 1-100), que ainda hoje está dividida em três grupos de risco (“baixo risco”, RS: <18; “risco intermédio”, RS: 18-30; “alto risco”, RS: >30). O teste é realizado de forma centralizada nos EUA. Está disponível um grande número de estudos de validação prospectivos-retrospectivos [1–3]. Estão disponíveis análises económicas de saúde/estudos de impacto de decisões [4–6].
O valor preditivo do teste de resposta à quimioterapia com CMF ou FAC (5-fluorouracil, doxorubicina/adriamicina, ciclofosfamida) foi investigado retrospectivamente no tecido tumoral arquivado. Os doentes com baixo índice de RS não mostraram qualquer benefício desta quimioterapia [7].
EndoPredict® (Sividon Diagnostics GmbH, D): É um teste de prognóstico para carcinomas mamários HER2-negativos positivos para as ER. É determinado por RT-qPCR utilizando FFPE. O nível de expressão genética de doze genes (oito genes de informação e quatro genes de referência) é determinado e uma pontuação prognóstica (EP) é calculada usando um algoritmo matemático. A pontuação varia de 1 a 15 e tem dois grupos de risco: EP ≤5 = “baixo risco”, EP >5 = “alto risco”. Além disso, o teste EndoPredict® foi complementado com uma pontuação de risco molecular-clínico-patológico (EPclin Score). O estado nodal e a dimensão do tumor estão incluídos na classificação de risco. Isto também resulta em duas classes de risco em “baixo risco”, EPclin ≤3.3 e “alto risco”, EPclin >3.3 (Fig. 2).
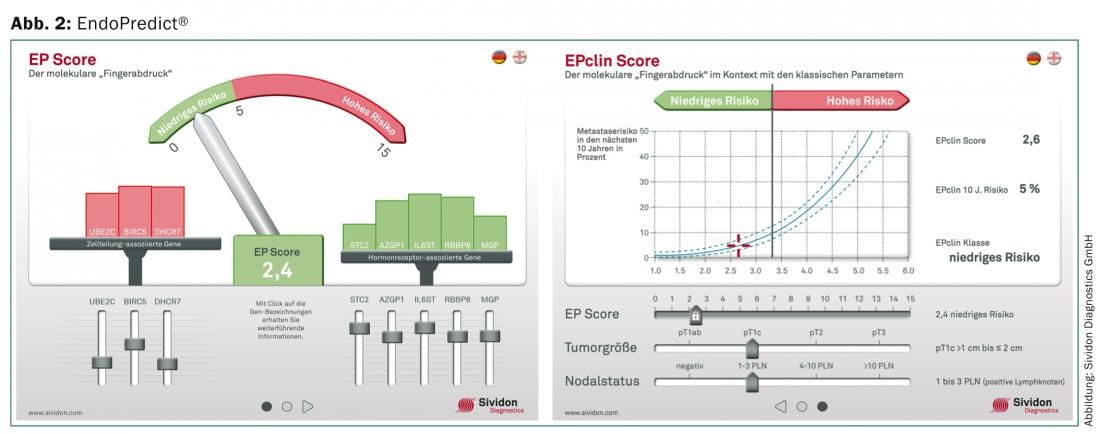
O EndoPredict® pode ser executado de forma descentralizada em patologia molecular. Estão disponíveis estudos comparativos sobre a uPA, PAI-1 [8]. Até ao momento, o teste só pode ser realizado na Alemanha, Áustria e Suíça. Estão disponíveis numerosos estudos de validação prospectivos-retrospectivos [9], mas até à data faltam estudos prospectivos-randomizados.
MammaPrint® (Agendia, Amsterdam, NDL): É o primeiro teste de ensaio genético aprovado pela FDA. É um teste de expressão genética baseado em microarranjos que anteriormente só podia ser realizado utilizando tecido fresco. Isto era uma desvantagem no manuseamento. Recentemente, o teste também pode ser realizado com tecido FFPE. Um total de 70 genes de informação e várias centenas de genes de referência são quantificados no tecido tumoral a fim de realizar a classificação do risco. Existem apenas dois grupos de risco também para este teste. O grupo de baixo risco (“bom prognóstico”) mostra um curso clínico significativamente melhor do que o grupo de alto risco (“mau prognóstico”). Isto foi demonstrado por numerosos estudos de validação independentes [10]. O teste é realizado num laboratório central em Amesterdão.
Recomendações das directrizes
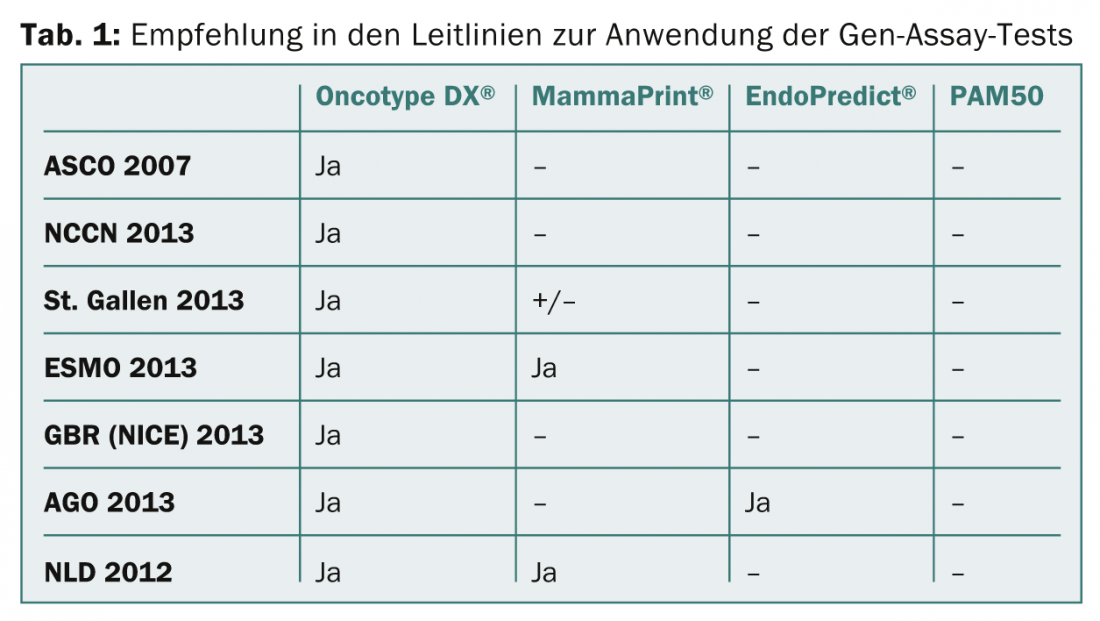
Nas directrizes AGO e S3 para o tratamento do carcinoma da mama, o Oncotype DX® e o teste EndoPredict®/EPclin são recomendados para utilização em casos individuais. Em particular, o Oncotype DX® encontra a mais ampla aceitação nas directrizes (ASCO 2007, NCCN2013, St. Gallen 2013, ESMO 2013, GBR [NICE] 2013) (Tab. 1).
Factores prognósticos e preditivos
Os factores prognósticos estimam o curso da doença do doente. Isto não leva em conta a terapia adjuvante e, portanto, apenas prevê quão boa ou má é a situação inicial do paciente. Todos os testes acima referidos são prognósticos.
São utilizados factores preditivos para avaliar a eficácia de uma determinada terapia adjuvante (resposta terapêutica). Os factores preditivos devem ajudar a decidir de que quimioterapia um paciente pode beneficiar.
Resumo
O prognóstico do carcinoma mamário precoce foi previamente determinado com base na análise imuno-histoquímica. O factor de proliferação Ki67 é decisivo para a classificação em subgrupos luminal A ou B. A determinação imuno-histoquímica do Ki67 é imprecisa, especialmente na gama intermédia. Isto foi demonstrado em testes interlaboratoriais. Aqui, os testes de ensaio de genes prometem uma melhor especificidade. O que é importante, contudo, é se estes testes são também preditivos e podem assim prever o benefício da quimioterapia. Os dados actuais mostram uma redução até 45% na quimioterapia primária planeada quando se utilizam os ensaios genéticos [11,12]. Os testes têm assim uma influência inequívoca na tomada de decisões dos médicos que os tratam. Um estudo multicêntrico prospectivo foi concluído no ano passado como parte do SAKK (SAKK26/10). Destina-se a mostrar a influência do Oncotype DX® na tomada de decisões do médico relativamente à terapia adjuvante. Os resultados são esperados em 2016.
Foram concluídos dois grandes ensaios aleatórios prospectivos com mais de 15 000 pacientes (TailorX, PlanB). Os primeiros resultados estarão disponíveis no final de 2015 ou 2013. disponível no início de 2016. Ambos os estudos fornecem dados sobre o valor preditivo do Oncotype DX®. O TailorX também fornecerá uma repartição da gama intermédia da pontuação de recorrência. Outro ensaio prospectivo aleatório (MINDACT) irá fornecer-nos dados sobre o valor preditivo do MammaPrint®.
Até que estes dados estejam disponíveis, a elegibilidade dos ensaios será apoiada por estudos retrospectivos. Desde o início de Janeiro de 2015, os custos têm sido cobertos pelas companhias de seguros de saúde na Suíça.
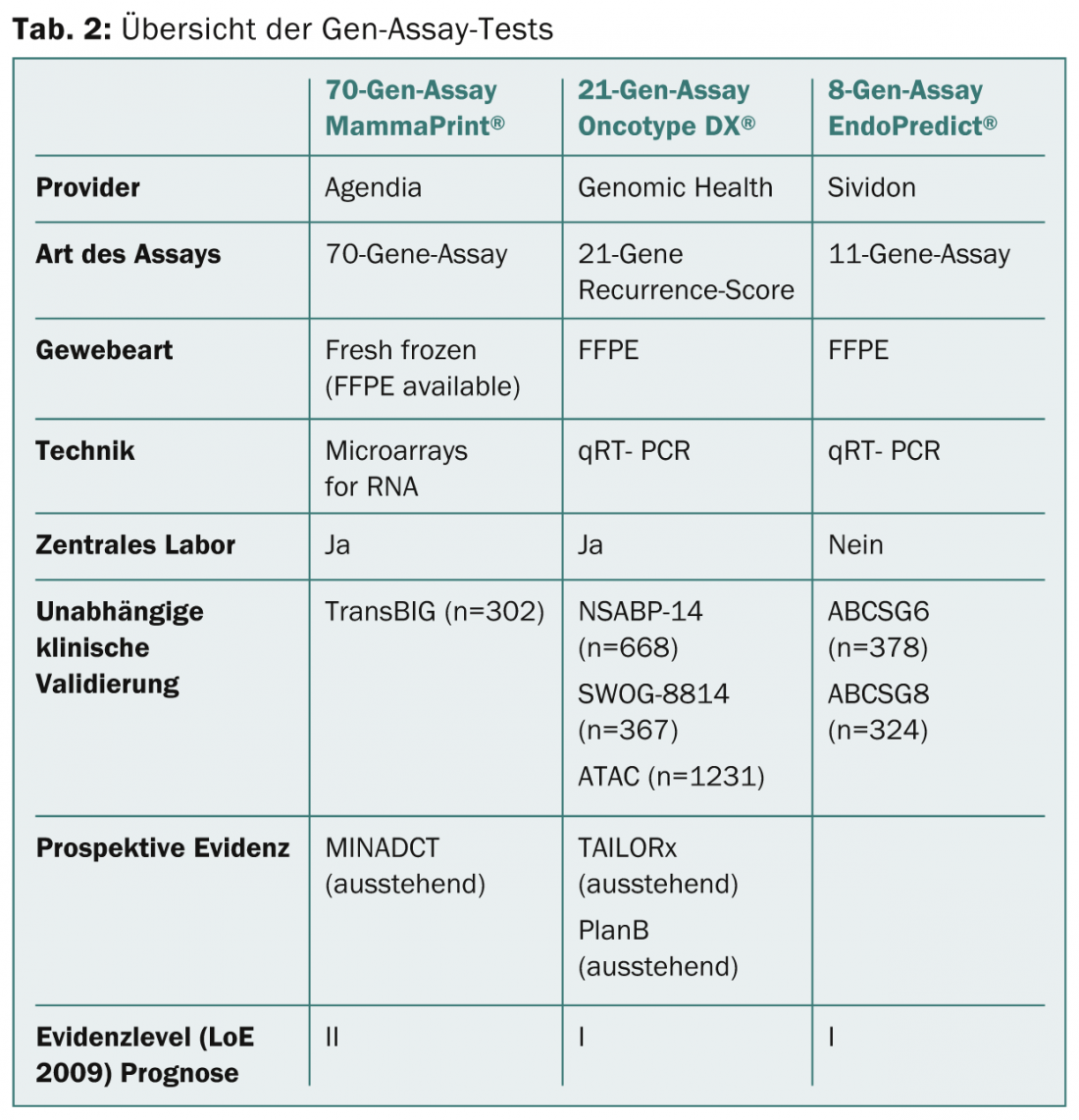
O quadro 2 fornece um resumo dos testes de ensaio de genes mencionados.
Literatura:
- Paik S, et al: Um ensaio multigene para prever a recorrência do cancro da mama tratado com tamoxifeno, node-negativo. N Engl J Med 2004; 351(27): 2817-2826.
- Albain KS, et al: Valor prognóstico e preditivo do ensaio do escore de recorrência de 21 genes em mulheres na pós-menopausa com cancro da mama positivo, estrogénio-receptor-positivo em quimioterapia: uma análise retrospectiva de um ensaio aleatório. The Lancet Oncology 2010; 11(1): 55-65.
- Dowsett M, et al.: Predição do risco de recidiva à distância usando o escore de recidiva de 21 genes em doentes pós-menopausa com cancro da mama tratados com anastrozol ou tamoxifeno: um estudo TransATAC. J Clin Oncol 2010; 28(11): 1829-1834.
- Klang SH, et al: Implicações económicas do ensaio de risco de cancro da mama de 21 genes, na perspectiva de uma organização de saúde gerida por Israel. Valor na saúde: a revista da Sociedade Internacional de Farmacoeconomia e Pesquisa de Resultados 2010; 13(4): 381-387.
- Kondo M, et al: Avaliação económica da assinatura de 21 genes (Oncotype DX) em nódulo linfático/negativo/positivo, receptor hormonal positivo de cancro da mama em fase inicial com base no estudo de validação japonês (JBCRG-TR03). Res Tratamento do Cancro da Mama 2011; 127(3): 739-749.
- Geffen DB, et al: O impacto do ensaio da pontuação de recorrência de 21 genes na tomada de decisões sobre quimioterapia adjuvante em cancro da mama em fase inicial do estrogénio-receptor-positivo numa prática oncológica com uma política de tratamento unificada. Ann Oncol 2011; 22(11): 2381-2386.
- Paik S, et al: Gene Expression and Benefit of Chemotherapy in Women With Node-Negative, Estrogen Receptor-Positive Breast Cancer. JCO Early Release, publicado online antes da impressão de 23 de Maio de 2006.
- Ettl J, et al.: Comparação prospectiva da pontuação uPA/PAI-1 e EndoPredict-clin em ER-positivo, HER2-negativo cancro da mama: Impacto na estratificação de risco e decisões de tratamento. J Clin Oncol 2013; 31 (suppl; abstr 581).
- Filipits M, et al.: Um novo preditor molecular de recidiva distante em cancro da mama com ER positivo, HER2-negativo, acrescenta informação independente aos factores de risco clínicos convencionais. Clin Cancer Res 2011; 17(18): 6012-6020.
- Buyse M, et al: Validação e utilidade clínica de uma assinatura prognóstica de 70 genes para mulheres com cancro da mama negativo com aceno. J Natl Cancer Inst 2006; 98(17): 1183-1192.
- Goodwin MCHJ, Diego M, Frazier TG: Impact of Oncotype DXTM recurrence score and tumour size on making qumotherapy decisions in breast cancer patients. Artigo apresentado no San Antonio Breast Cancer Symposium 2009.
- Guth AAFS, et al: Utilização do Oncotype DX para prever o uso de quimioterapia numa população incipiente. Artigo apresentado na Reunião Anual de 2011 da Sociedade Americana de Oncologia Clínica.
InFo ONCOLOGy & HEMATOLOGy 2015; 3(2): 5-8