O espectro do tratamento das dermatoses inflamatórias expandiu-se grandemente. A reaprovação de 2019 do risankizumab (psoríase) e dupilumab (dermatite atópica) são apenas alguns dos marcos importantes. Pode presumir-se que mais medicamentos novos serão lançados em breve no mercado.
A investigação sobre a função patogénica dos imunomoduladores constitui uma base importante para o desenvolvimento de novas substâncias activas específicas do alvo. O PD Dr. Robert Sabat, chefe do Centro de Investigação e Tratamento da Psoríase, Charité-Universitätsmedizin Berlin, deu uma visão actualizada das bases imunológicas com enfoque nas dermatoses inflamatórias mais comuns nos Dias de Formação Dermatológica de Zurique deste ano [1].
A psoríase como exemplo principal
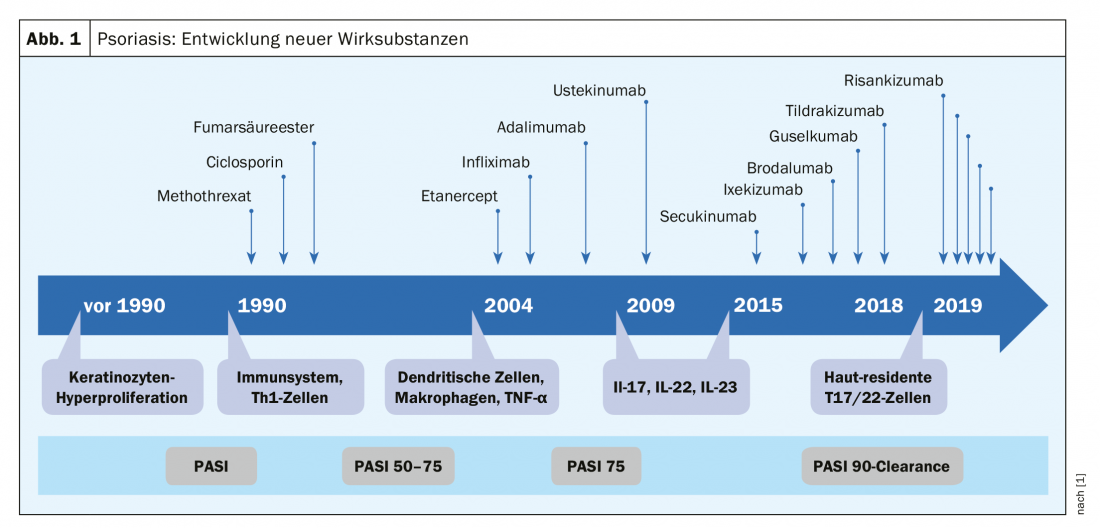
A neutralização de citocinas individuais – agentes patogénicos fundamentais de doenças inflamatórias da pele e alvos de terapias específicas – revolucionou as opções de tratamento de várias dermatoses. A psoríase é um bom exemplo disso: Nas últimas duas décadas, numerosas novas substâncias farmacoterapêuticas fizeram progressos, com os maiores avanços nos últimos anos (Fig. 1). Só em 2018, vários novos compostos entraram no mercado (ixekizumab, brodalumab, guselkumab, tildrakizumab). “A psoríase é um excelente exemplo de que a compreensão dos processos inflamatórios compensa realmente”, explica o orador. Segundo o Dr. Sabat, o patomecanismo da psoríase pode ser resumido como uma reacção excessiva dos tecidos a certas citocinas de certas células imunitárias. Actualmente, o foco está nas células Th17 e Th22 residentes na pele e o alvo da terapia é o PASI90 ou PASI100. Em relação à dermatite atópica, a nova aprovação do dupilumabe de anticorpos monoclonais em 2019, como o primeiro representante biológico para esta indicação, representa um marco [6].
Que a dermatite atópica e a psoríase são doenças de pele comuns é também demonstrado por novos números epidemiológicos. Relativamente à psoríase, o estudo prospectivo dinamarquês Skin Cohort publicado em 2019 refere uma prevalência ao longo da vida de 7,9% e uma prevalência de 5% numa amostra representativa da população em geral (n=3490) [2]. Em contraste com a dermatite atópica e a psoríase, sabe-se muito menos sobre os fenótipos exactos das células T relevantes para a doença em muitas outras doenças de pele imunomediadas (por exemplo líquen plano, acne inversa/hidradenite supurativa ou pênfigo) [3]. Mas também estão em curso intensos esforços de investigação a este respeito. Por exemplo, um estudo recente sobre perfis de citocinas da psoríase e da acne inversa mostra que os níveis cutâneos de IL-1β são significativamente mais elevados na acne inversa/hidradenite supurativa do que na psoríase [4].
Citoquinas como actores chave
As doenças de pele mediadas por células T, tais como psoríase, dermatite atópica, vitiligo e acne inversa, procedem de acordo com o seguinte esquema idêntico: fase de sensibilização celular, fase effector, sintomas clínicos. Na fase de sensibilização celular, há uma interacção entre a célula dendrítica e a célula T. Se algumas destas populações de células T estiverem sobreativadas, ocorrem doenças inflamatórias crónicas. Na psoríase, isto afecta as populações de células T Th17 e Th22, no vitiligo Th1, e na dermatite atópica principalmente as células Th2. Na psoríase, a secreção induzida por Th17 das citocinas IL-17, IL26, IL-29 e IL-29 é patogeneticamente relevante. a secreção das citocinas IL22 e TNFα induzida por Th22. A inibição destas citocinas-chave está subjacente às novas citocinas biológicas/bio-similares desenvolvidas nos últimos anos [1,6]:
TNFα inibidor: etanercerpt, infliximab, adalimumab, certolizumab pegol, golimumab. Com excepção do golimumab (apenas artrite psoriásica), todos os agentes acima mencionados são aprovados para a psoríase e a artrite psoriásica.
inibidor da IL17: secukinumab, ixekizumab. Ambos são também aprovados para a artrite psoriásica.
Inibidor da IL23: ustekinumab , guselkumab, tildrakizumab, risankizumab. Ustekinumab é aprovado para psoríase e artrite psoriásica, os outros apenas para psoríase.
Risankizumab (SKYRIZI™), aprovado em 2019 [5], pode ser utilizado para o tratamento da psoríase de placa moderada a grave em doentes adultos que tiveram uma resposta inadequada a outras terapias sistémicas, tais como a ciclosporina, o metotrexato (MTX) ou o PUVA (psoralen e UV-A), ou que têm uma contra-indicação ou intolerância a tais terapias [5].
No que respeita à dermatite atópica, a autorização de comercialização de 2019 do dupilumab (Dupixent®), como primeiro representante da biologia para esta indicação, é a evolução mais recente das opções de tratamento [6].
O Dr. Sabat salienta que a investigação em terapêutica farmacológica para dermatoses inflamatórias está longe de estar completa. Os ensaios das fases II e III estão actualmente em curso para uma série de substâncias activas e pode assumir-se que o espectro de opções terapêuticas irá expandir-se novamente num futuro próximo.
Literatura:
- Sabat R: Apresentação de slides: Curso de Actualização 3 – Dermatoses Inflamatórias. Patofisiologia da inflamação da pele: palestra panorâmica, PD Dr. Robert Sabat, 9th Zurich Dermatological Training Days, Zurique, 27. Junho 2019.
- Egeberg A, Andersen YMF, Thyssen JP: Prevalência e características da psoríase na Dinamarca: conclusões da coorte de pele dinamarquesa BMJ Open 2019; 9:e028116. doi: 10.1136/bmjopen-2018-028116.
- Sabat R, et al: Patologia das células T na inflamação da pele. Seminários em Imunopatologia 2019; 41 (3), 359-377.
- Witte-Händel E, et al: A via IL-1 é hiperactiva na Hidradenite Supurativa e contribui para a Infiltração e Destruição da Pele. J Invest Dermatol 2019; 139(6): 1294-1305. doi: 10.1016/j.jid.2018.11.018. Epub 2018 Dez 5.
- Compêndio Suíço de Drogas: SKYRIZI™. https://compendium.ch/, acedido pela última vez em 28 de Junho de 2019.
- Compêndio Suíço de Drogas: Dupixent®. https://compendium.ch/, acedido pela última vez em 28 de Junho de 2019.
DERMATOLOGIE PRAXIS 2019; 29(4): 32-33 (publicado 26.8.19, antes da impressão).