Estudos sugerem que a vigilância activa é uma opção de tratamento para tumores com baixo risco de progressão (tumores de baixo risco). A equipa de tratamento deve trabalhar com o doente para determinar estratégias de tratamento com base nas directrizes existentes e nas provas actuais. Na Vigilância Activa, o acompanhamento dos doentes e a monitorização regular são um factor crucial na estratégia de tratamento. Cada vez mais são diagnosticados carcinomas da próstata com base em medições de PSA. Cerca de 90% destes tumores são localizados. Uma grande proporção dos tumores diagnosticados não representa um risco para os doentes em causa; o risco de morbilidade das intervenções é maior para estes doentes do que o risco de morbilidade do tumor.
De acordo com as actuais directrizes (S3 Guideline DGU, EAU Guideline on Prostate Cancer), existem várias opções alternativas para o tratamento do cancro da próstata localizado de baixo risco: prostatectomia radical, radioterapia local, vigilância activa e, dependendo da idade, o conceito de espera vigilante. Vigilância activa (AS) significa o acompanhamento próximo de pessoas diagnosticadas com uma doença durante o seu curso. AS deve ser distinguido de Watchful Waiting (Espera vigilante). Isto inclui estratégias de tratamento sintomático de uma doença no seu curso sem o objectivo de transferir pacientes para a terapia curativa, por exemplo devido à idade avançada e/ou comorbilidades graves. AS deve também ser distinguido da vigilância clínica/de saúde pública, que visa a recolha, análise e interpretação de dados relacionados com a saúde de populações específicas [1].
Vigilância activa para cancros de baixo risco
A análise e interpretação de tratamentos oncológicos para doenças oncológicas seleccionadas em homens perseguiram recentemente o objectivo de evitar o tratamento excessivo com opções terapêuticas invasivas. Especialmente para o cancro da próstata e dos testículos, foram desenvolvidos critérios que não conduzem a nenhum tratamento imediato ou mesmo a nenhum tratamento. Para ambas as entidades, as directrizes de tratamento estipulam que, para além das opções de tratamento estabelecidas (prostatectomia, radioterapia, terapia tumoral baseada em medicamentos, ablação hormonal, orquiectomia), o AS para doenças de baixo risco está também disponível como outra opção de tratamento primário [2,3]. A decisão a favor ou contra o AS como estratégia de tratamento é determinada pela classificação do tumor como “de baixo risco”.
Utilizando o exemplo do carcinoma da próstata, as dificuldades práticas na escolha de um possível tratamento serão demonstradas a seguir. O facto de a classificação do cancro ser ainda – apesar de muitos anos de investigação – caracterizada por uma prática muito heterogénea é demonstrado em estudos actuais [4–11]. Por exemplo, a taxa de pacientes com um tumor de baixo risco caiu de 60% em 2004 para 27% em 2013 – com base nas definições revistas de tumores de baixo risco [12].
Epidemiologia e etiologia
O cancro da próstata é o cancro mais comum nos homens na Suíça [13]. Há uma incidência diferente em populações diferentes: nos EUA, as pessoas de pele escura são mais frequentemente afectadas do que os brancos e estes últimos mais frequentemente do que os asiáticos. Isto sugere uma predisposição genética para o desenvolvimento de carcinoma [9]. Presumivelmente, a predisposição genética é também influenciada e modificada por factores sociodemográficos [14–16]. Por exemplo, a incidência do cancro da próstata aumenta entre os asiáticos que imigram para os EUA. A incidência de cancro da próstata clinicamente não significativo é comparável em todo o mundo, mas existem diferenças para o cancro da próstata clinicamente relevante. Os homens com um parente de primeiro grau com cancro da próstata têm o dobro do risco de desenvolver também cancro da próstata. Se houver vários familiares de primeiro grau com a doença, o risco aumenta 5 a 11 vezes [10,17].
A maioria de todos os carcinomas da próstata surgem provavelmente devido a múltiplos polimorfismos genéticos [10]. A testosterona não é actualmente considerada um agente pré-cancerígeno, mas provavelmente desempenha um papel como promotor de tumores em tumores já progressivos. Os componentes dietéticos afectam o cancro da próstata de muitas maneiras [18]. As proteínas animais parecem favorecer o risco de desenvolvimento de cancro avançado da próstata. O oligoelemento selénio tem sido discutido há algum tempo em relação a um possível benefício protector. No entanto, o ensaio SELECT não pôde provar tal benefício e foi, portanto, terminado prematuramente em 2008. O tabagismo no momento do diagnóstico inicial aumenta o risco de tumor avançado, recidiva (38 vs. 26%) e morte por carcinoma (15,3 vs. 9,6/1000 anos-pessoa) [15]. A síndrome metabólica também aumenta o risco de cancro da próstata. Até agora não foi possível demonstrar uma ligação entre o risco de cancro da próstata e o consumo de álcool.
Elevada proporção de sobre-tratamento
Durante mais de 30 anos, a prostatectomia radical tem sido considerada a terapia padrão para o tratamento curativo do cancro da próstata; cerca de 70% dos pacientes com menos de 70 anos são submetidos à prostatectomia [8,12]. Esta estratégia é prosseguida sob o pressuposto de que o paciente é curado após a intervenção. Estas considerações devem ser cada vez mais colocadas em perspectiva: Numa estimativa de 30% dos homens que foram submetidos a cirurgia, a progressão do PSA ocorre no decurso da operação. Alguns dos pacientes têm tumores que não têm necessariamente de ser tratados com uma intervenção; estes pacientes não morreriam do tumor mesmo sem cirurgia ou radiação. Contudo, as possibilidades de avaliar a biologia tumoral individual são ainda hoje limitadas. Portanto, a equipa de tratamento e os pacientes escolhem frequentemente o caminho da intervenção, muitas vezes por preocupação de que o tumor possa evoluir para uma fase que já não pode ser tratada curativamente devido à rápida progressão.
A observação activa regular de pacientes com carcinomas de baixo risco clinicamente irrepreensíveis adequados para o AS pode prevenir morbidades relacionadas com a terapia (disfunção eréctil, incontinência, complicações relacionadas com cirurgias e radiações, etc.) e, portanto, o tratamento excessivo e é considerado seguro neste contexto. A carga psicológica sobre o doente e o parceiro sob a orientação de um urologista experiente é também considerada adequada [6,18]. O estudo ERSPC mostrou uma taxa de sobre-tratamento de 54%. Poupar a estes homens as morbidades da terapia intervencionista é o objectivo do AS [5].
Critérios para a Vigilância Activa
A actual directriz S3 sobre detecção precoce, diagnóstico e tratamento das diferentes fases do cancro da próstata inclui AS como uma estratégia de tratamento para carcinomas de baixo risco definidos que preenchem determinados critérios (Tab. 1).

A directriz define os seguintes critérios de decisão relevantes:
- Os pacientes com cancro da próstata localizado que são elegíveis para tratamento curativo local devem ser informados não só sobre procedimentos de tratamento como a prostatectomia radical, radioterapia e braquiterapia, mas também sobre o AS.
- Em pacientes com cancro da próstata localizado que são candidatos a tratamento curativo, os efeitos adversos e as consequências terapêuticas da prostatectomia radical, radioterapia percutânea e braquiterapia devem ser ponderados contra o risco de tratamento retardado no caso de uma estratégia AS.
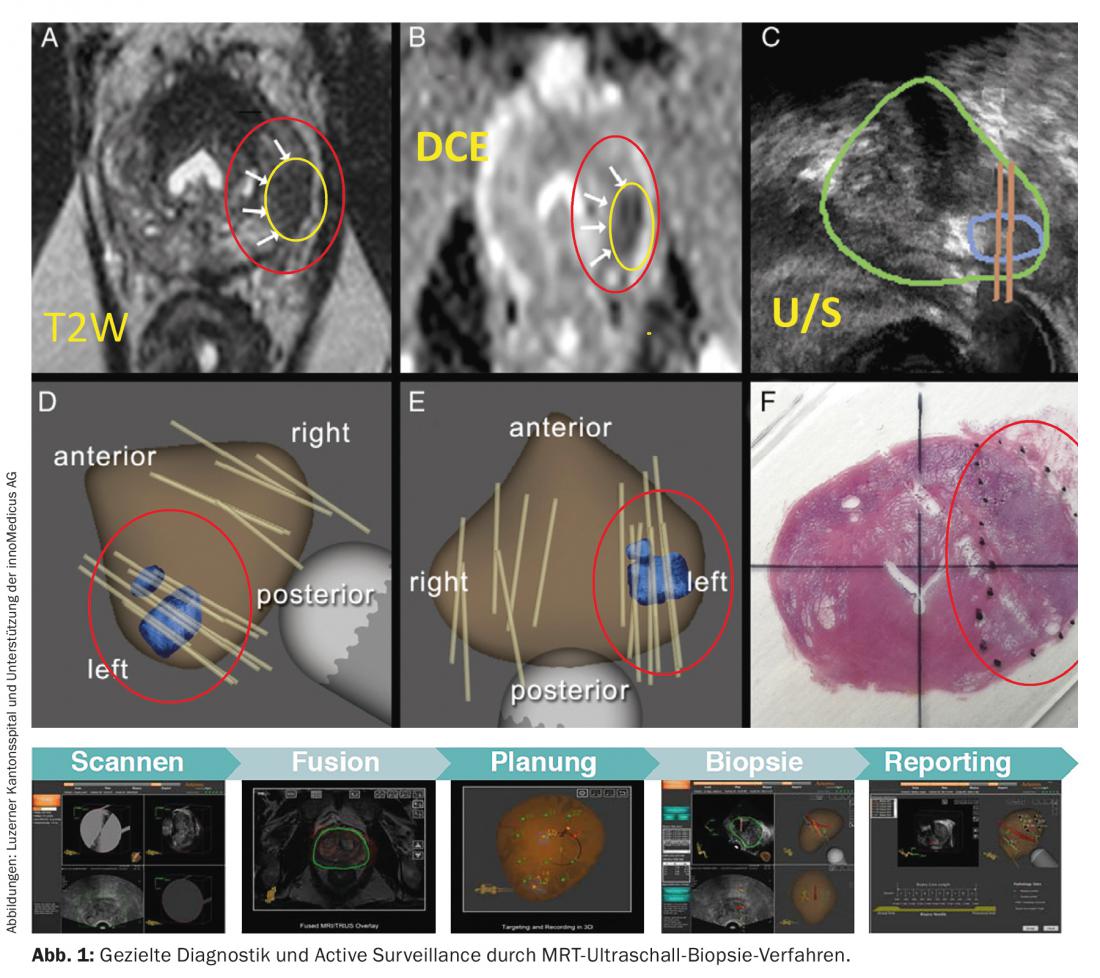
- O tumor deve ser monitorizado de três em três meses durante os primeiros dois anos após o diagnóstico, utilizando determinação de PSA e exame rectal digital. Se o valor do PSA permanecer estável, deverá ser verificado de seis em seis meses a seguir. As biópsias devem ser feitas a cada 12-18 meses. Novos métodos para aumentar a importância das biópsias de próstata estão actualmente a ser investigados (Fig. 1).
- O AS deve ser abandonado se o tempo de duplicação do PSA for reduzido para menos de três anos ou se o grau de malignidade se deteriorar para uma pontuação de Gleason >6.
A medida em que o tratamento deve ser adaptado no curso individual (por exemplo, prostatectomia radical ou radiação local) depende directamente da dinâmica individual do cancro. Cada paciente é informado sobre todas as opções terapêuticas e é-lhe principalmente oferecido um procedimento que lhe permite inicialmente passar mais anos da sua vida sem deficiências relacionadas com a terapia e com uma elevada qualidade de vida. Os centros de oncologia certificados ajudam comprovadamente a garantir a qualidade dos cuidados.
Conclusão para a prática
- Actualmente, o primeiro teste PSA de base é recomendado na Suíça entre os 40 e 45 anos de idade.
- Se o nível PSA for <1 ng/ml, recomenda-se a determinação PSA de três em três anos, para PSA ≥1 a <2 ng/ml de dois em dois anos e para PSA ≥2 a <3 ng/ml anualmente. O paciente deve ser previamente informado em pormenor.
- Medições excessivas de PSA provocam o diagnóstico de um número crescente de carcinomas da próstata que, de outra forma, não teriam sido detectados durante toda a vida numa determinada constelação etária, comorbilidades e/ou biologia tumoral favorável para os pacientes.
- Cerca de 90% dos doentes diagnosticados nos últimos anos localizaram o carcinoma da próstata.
- Estudos sugerem que o AS é uma opção de tratamento para tumores com baixo risco de progressão (tumores de baixo risco). Os pacientes devem ser informados sobre todas as opções de tratamento.
- A equipa de tratamento (médicos de clínica geral, urologistas, oncologistas de radiação, oncologistas) tem de definir e acompanhar as estratégias de tratamento juntamente com o paciente e os seus familiares, especialmente no caso de possíveis SA, com base nas directrizes existentes e nas provas actuais.
- A Sociedade Suíça de Urologia criou uma base de dados de vigilância activa (SIP-CAS) para assegurar e expandir continuamente a base de provas.
Literatura:
- OMS, Vigilância da saúde pública, 2015. www.who.int/topics/public_health_surveillance/en/.
- Kollmannsberger C, et al: Padrões de recidiva em doentes com cancro testicular em fase clínica I geridos com vigilância activa. J Clin Oncol 2015; 33(1): 51-57.
- Coursey Moreno C, et al: Tumores testiculares: o que os radiologistas precisam de saber – diagnóstico diferencial, encenação e gestão. Radiografias 2015; 35(2): 400-415.
- Loeb S, et al: Active Surveillance for Prostate Cancer: A Systematic Review of Clinicopathologic Variables and Biomarkers for Risk Stratification. Urologia Europeia 2015; 67(4): 619-626.
- Klotz L: Vigilância Activa do Cancro da Próstata: Debate sobre a Aplicação, Não o Conceito. European Urology 2015 Jan 24. doi: 10.1016/j.eururo.2015.01.007. [Epub ahead of print]
- Bellardita L, et al: Como é que a vigilância activa do cancro da próstata afecta a qualidade de vida? Uma Revisão Sistemática. European Urology 2015; 67(4): 637-645.
- Bangma CH, et al: Vigilância activa do cancro da próstata de baixo risco: desenvolvimentos até à data. European Urology 2015; 67(4): 646-648.
- Saman DM, et al: Uma revisão da epidemiologia actual e das opções de tratamento do cancro da próstata. Dis Mon 2014; 60(4): 150-154.
- Helfand BT, Catalona WJ: A epidemiologia e implicações clínicas da variação genética no cancro da próstata. Urol Clin North Am 2014; 41(2): 277-297.
- Eeles R, et al: A epidemiologia genética do cancro da próstata e as suas implicações clínicas. Nat Rev Urol 2014; 11(1): 18-31.
- Berman DM, Epstein J: Quando é que o cancro da próstata é realmente cancro? Urol Clin North Am 2014; 41(2): 339-346.
- Huland H, Graefen M: Tendências de mudança na gestão cirúrgica do cancro da próstata: O fim do tratamento excessivo? Eur Urol 2015 Fev. 27. doi: 10.1016/j.eururo. 2015.02.020. [Epub ahead of print]
- Instituto Federal de Estatística, 2015. www.bfs.admin.ch/bfs/portal/de/index/themen/14/02/05/key/01/02.html.
- Kasperzyk JL, et al: Espera vigilante e qualidade de vida entre os sobreviventes do cancro da próstata no Estudo de Saúde dos Médicos. J Urol 2011; 186(5): 1862-1867.
- Kenfield SA, et al: Fumar e cancro da próstata sobrevive e recidiva. JAMA 2011; 305(24): 2548-2555.
- Kenfield SA, et al: Actividade física e sobrevivência após o diagnóstico do cancro da próstata no estudo de acompanhamento dos profissionais de saúde. J Clin Oncol 2011; 29(6): 726-732.
- Bratt O: Cancro hereditário da próstata: aspectos clínicos. J Urol 2002; 168(3): 906-913.
- Masko EM, et al: A relação entre nutrição e cancro da próstata: é mais sempre melhor? Eur Urol 2013; 63(5): 810-820.
InFo ONCOLOGy & HEMATOLOGy 2015; 3(5): 8-11