A incidência anual de melanoma maligno tem aumentado de forma constante ao longo dos últimos 40 anos. Embora o prognóstico seja bom nas fases iniciais, deteriora-se com o aumento da fase do tumor. A terapia adjuvante utilizando inibidores de BRAF/MEK ou ponto de controlo teve um impacto duradouro na gestão de casos avançados e continua em curso.
A incidência anual de melanoma maligno tem aumentado constantemente nos últimos 40 anos, variando dentro da Europa de 3-5/100.000 nos países mediterrânicos para 12-35/100.000 nos países nórdicos. Neste contexto, 80% dos melanomas malignos são diagnosticados numa fase localizada. Para o melanoma da fase inicial, a ressecção cirúrgica é o tratamento padrão e está associada a um bom prognóstico a longo prazo. A taxa de sobrevivência global (SO) de cinco anos é de 65-100% para a doença nas fases I-II e diminui para os doentes com metástases locais (fase III) a 41-71% e em doentes com metástases distantes (fase IV) a 9-28% [1].
Classificação de melanoma e alterações genéticas moleculares
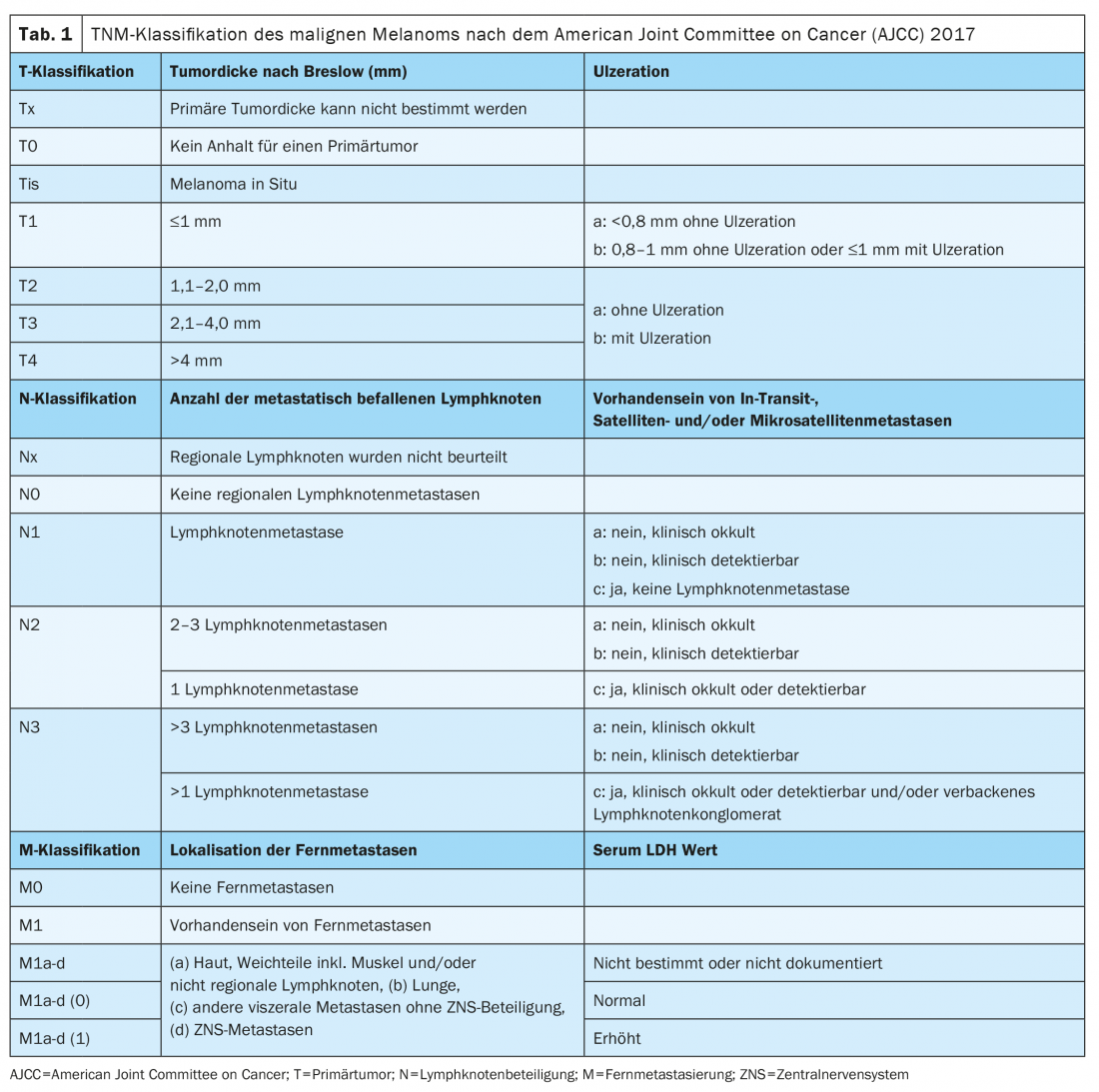
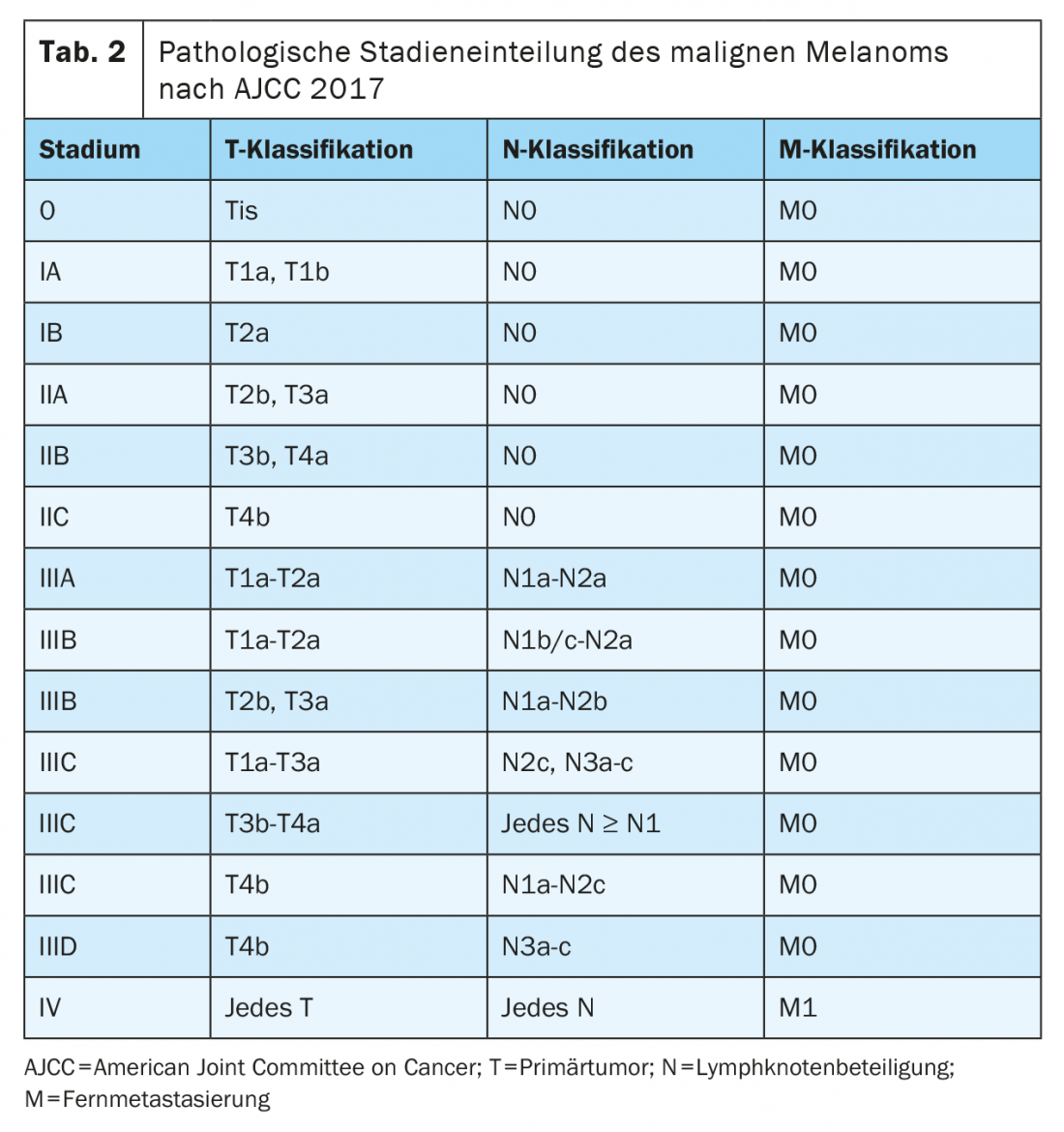
Desde Janeiro de 2018, o melanoma foi classificado de acordo com a 8ª edição do Manual de Encenação do AJCC (Tabelas 1 e 2) . A espessura do tumor vertical de acordo com Breslow é o factor prognóstico mais importante e é tomada em consideração ao determinar o tratamento posterior, incluindo as margens de segurança necessárias e a necessidade de uma biopsia do gânglio linfático sentinela. A presença de ulceração é outro marcador histopatológico relevante, que está associado a um pior prognóstico e que é registado na fase T da classificação TNM.
Os diagnósticos patológicos moleculares usando sequenciação da próxima geração (NGS) para determinar o estado de BRAF devem ser realizados em melanoma local avançado ou metastático das fases III e IV. O exame imunohistoquímico só permite a detecção de uma mutação V600E, enquanto que V600K e outras mutações atípicas não podem ser detectadas. A Classificação Genómica do Melanoma Cutâneo prevê uma divisão em quatro subtipos: Melanoma de mutação BRAF (50%); mutação N-Ras, K-Ras ou H-Ras (25%); mutação NF1 (15%) e melanoma do tipo triplo selvagem (10%) [2].
Apesar dos progressos significativos na compreensão da base genética do melanoma, a utilização de alterações genéticas para fins diagnósticos, prognósticos ou terapêuticos continua a ser limitada. O estado de mutação BRAFV600E/K é preditivo de tratamento com inibidores de BRAF. Embora não existam actualmente terapias específicas estabelecidas para as outras alterações genéticas, estas fornecem informações importantes para a inclusão no estudo, bem como potenciais abordagens terapêuticas futuras.
Terapia cirúrgica do tumor primário e dos gânglios linfáticos regionais
Se houver suspeita clínica de melanoma maligno, deve ser feita uma excisão in toto. Após confirmação histopatológica de um melanoma maligno, o tratamento primário é a excisão local com uma margem de segurança suficiente, dependendo da espessura do tumor de acordo com Breslow (0,5 cm para melanomas in situ, 1 cm para melanomas com uma espessura de tumor até 2 mm, 2 cm a partir de uma espessura de tumor de 2 mm). Uma margem de segurança suficiente está associada a uma redução na taxa de recorrência local sem melhorar a sobrevivência global [3]. Para localizações na área facial ou genital, a distância de segurança recomendada pode ser ajustada se for necessário assumir uma morbilidade significativa apesar da cirurgia reconstrutiva. Deve salientar-se que as distâncias de segurança não devem ser reduzidas por razões estéticas.
Uma biópsia do gânglio linfático sentinela (SLNB) é recomendada nas directrizes da OMPE para uma fase pT1b (ou seja, uma espessura de tumor de acordo com Breslow de >0,8 mm ou <0,8 mm com ulceração) de acordo com a 8ª edição da AJCC. O estudo prospectivo MSLT-I validou o valor prognóstico e a contribuição do gânglio linfático sentinela (SLK) para a encenação sem mostrar um benefício de sobrevivência para este procedimento [4]. Até 2017, a dissecção completa dos gânglios linfáticos para um gânglio sentinela positivo era considerada o tratamento padrão. Tanto o estudo alemão DeCOG-SLT como o estudo internacional MSLT-2 compararam o seguimento ultrassonográfico regular da área de drenagem linfática com a dissecção completa dos gânglios linfáticos (LND) para o SLK [5,6] positivo. Ambos os estudos encontraram um aumento da morbilidade (linfedema) mas nenhuma melhoria significativa na sobrevivência específica da melanoma. A partir de 2019, o LND para um gânglio linfático sentinela positivo já não é, portanto, recomendado nas directrizes da OMPE [7]. No entanto, o LND ainda é recomendado para o envolvimento de gânglios linfáticos macroscópicos. É de notar que ambos os estudos foram realizados antes da introdução das terapias sistémicas adjuvantes e que a dissecção dos gânglios linfáticos foi realizada nas populações estudadas das terapias adjuvantes [8–10].
Terapia de sistema adjuvante
Após uma ressecção completa com uma margem de segurança suficiente e liberdade de tumores, os pacientes com melanoma nas fases IIB, IIC, III e IV têm um risco significativo de recidiva. Nestas fases do tumor, a terapia sistémica adjuvante deve ser considerada para reduzir o risco de recorrência local e metástases distantes e para melhorar a sobrevivência global. Os inibidores de ponto de controlo imunitário e as terapias orientadas estão actualmente aprovados nos EUA e Europa para o tratamento adjuvante de melanoma completamente ressecado nas fases III e IV e reduzem o risco de recidiva em cerca de 50%. As indicações e as aprovações diferem em função dos critérios de inclusão no estudo. É de notar que a encenação destas populações do estudo se baseia na 7ª Edição de 2009 do AJCC.
Terapia orientada adjuvante com inibidores de BRAF e MEK
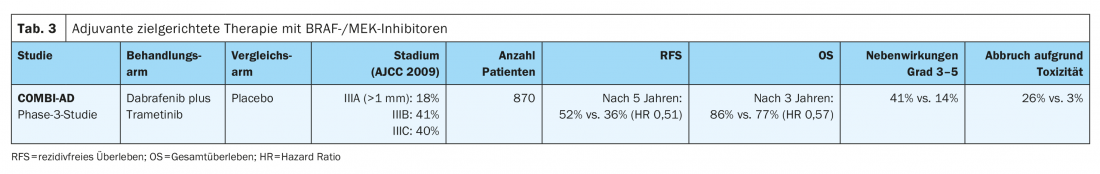
No ensaio COMBI-AD fase III (Tab. 3) , pacientes com melanoma completamente ressecado com uma mutação de BRAFV600E/K nas fases IIIA (metástase SLK >1 mm), IIIB e IIIC foram tratados durante 12 meses com terapia peroral orientada com os inibidores BRAF e MEK dabrafenib e trametinib ou placebo. Num seguimento mediano de cinco anos, foi demonstrada uma melhoria significativa na sobrevivência sem recorrência (RFS) (hazard ratio HR 0,51) e também na sobrevivência sem metástases (HR 0,55) para esta terapia adjuvante em comparação com o placebo. A combinação também melhorou a sobrevivência global (OS) após três anos (HR 0,57). O benefício foi documentado em todos os subgrupos [8,11]. Subsequentemente, a terapia orientada com dabrafenibe e trametinibe recebeu aprovação a nível da UE em Agosto de 2018 para o tratamento adjuvante do melanoma maligno linfogénico metastático com mutação BRAFV600E/K.
O ensaio BRIM8 comparou a monoterapia adjuvante com o inibidor de BRAF vemurafenibe ao placebo na fase de ressecção do melanoma IIC-III. O ponto final primário de prolongar a sobrevivência sem doenças não foi atingido no estudo, pelo que a monoterapia com um inibidor de BRAF no ambiente adjuvante não é uma opção de tratamento.
Imunoterapia adjuvante
No estudo CheckMate-238 (Tab. 4) A terapia intravenosa adjuvante com o anticorpo monoclonal anti-PD-1 nivolumab (3 mg/kg) mostrou uma melhoria significativa na sobrevivência sem recorrência (HR 0,71) e na sobrevivência sem metástases (HR 0,79) após quatro anos para melanomas de fase IIIB/C e IV completamente ressecados, em comparação com a dose elevada de anticorpo anti-CTLA4 ipilimumab (10 mg/kg). A sobrevivência global após quatro anos foi comparável nos dois ramos de tratamento (HR 0,87). Além disso, em comparação com a alta dose de ipilimumabe, ocorreram significativamente menos eventos adversos graves (grau 3-5) com interrupção consecutiva do tratamento com nivolumabe (9,7% vs. 42,6%). Os resultados em termos de toxicidade tardia foram semelhantes nos dois ramos de tratamento (1% vs. 2%) [10,12]. Nivolumab foi aprovado em toda a UE em 2018 para a terapia adjuvante do melanoma maligno nas fases III e IV, após metastasectomia completa.
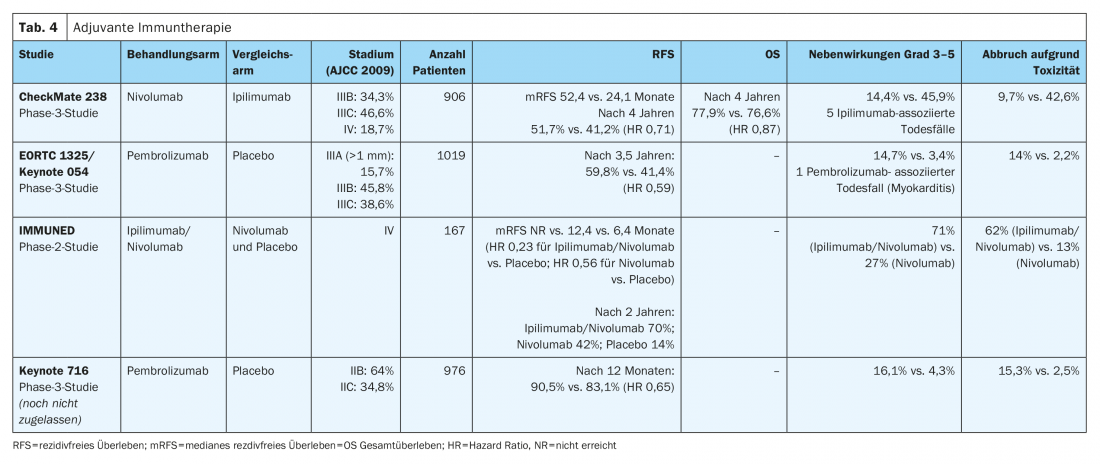
A eficácia do anticorpo anti-PD-1 pembrolizumab foi demonstrada no ensaio fase III EORTC1325/Keynote-54 em doentes com melanoma de fase IIIA completamente ressecado (metástase do gânglio linfático sentinela >1 mm), IIIB ou IIIC (sem metástases em trânsito) foram demonstradas (Tabela 4). Com um seguimento médio de três anos, o pembrolizumab foi associado a uma sobrevivência sem recaídas significativamente mais longa do que o placebo na população total (HR 0,56). Acontecimentos adversos graves (grau 3-5) foram observados mais frequentemente com pembrolizumab do que com placebo (14% vs. 3%) [9]. Pembrolizumab recebeu a aprovação da UE para esta indicação em Janeiro de 2019.
O efeito positivo em termos de melhoria da sobrevivência sem recaídas foi observado em todos os subgrupos predefinidos, tanto no ensaio EORTC1325/Keynote-054 como no ensaio CheckMate-238. Em ambos os estudos, o inibidor do ponto de controlo imunitário foi administrado durante um período total de um ano de terapia.
Os resultados preliminares do ensaio aleatório da fase III CheckMate 915 (Tab. 4) não mostram qualquer melhoria na sobrevivência sem recidivas de pacientes com melanoma de fase IIIB-D ou IV avançado e ressecado, recebendo terapia adjuvante com nivolumab (240 mg a cada 2 semanas) em combinação com ipilimumab (1 mg/kg a cada 6 semanas) durante uma duração total de tratamento de 12 meses em comparação com a monoterapia nivolumab (480 mg a cada 4 semanas). Estes resultados diferem significativamente dos resultados do estudo da fase II do adjuvante IMMUNED (Tab. 4). Este estudo demonstrou uma clara superioridade da terapia de combinação adjuvante com nivolumab (1 mg/kg) e ipilumab (3 mg/kg) durante 4 ciclos de 3 em 3 semanas em monoterapia com nivolumab (3 mg/kg) de 2 em 2 semanas ou placebo em doentes com melanoma maligno de fase IV sem evidência de doença após cirurgia. A razão de perigo para a recorrência foi de 0,23 no grupo nivolumab/ipilimumab em comparação com o grupo placebo e 0,56 no grupo nivolumab em comparação com o grupo placebo. Os eventos adversos associados à terapia de qualquer grau levaram à interrupção do tratamento em 62% dos doentes do grupo nivolumab/ipilimumab e em 13% dos participantes no estudo que receberam tratamento nivolumab [13].
Com base nestes resultados, os pacientes com melanoma maligno de fase IV sem evidência de doença devem receber imunoterapia combinada adjuvante após cirurgia ou radioterapia, independentemente do estado de mutação do BRAFV600. Para pacientes com contra-indicações à imunoterapia combinada com nivolumab e ipilumumab, um ano de terapia adjuvante com nivolumab como monoterapia deve ser dado nesta situação, análogo ao estudo CheckMate 238. Esta terapia tem um perfil de toxicidade mais controlável e é aprovada para o tratamento de pacientes com doença de fase IV completamente ressecada [10].
Imunoterapia adjuvante em fases IIB e IIC
Os doentes com um melanoma ressecado e uma espessura de tumor segundo Breslow de >4 mm ou >2 mm na presença de ulceração sem envolvimento dos gânglios linfáticos (fase IIB ou IIC segundo AJCC 8ª edição) têm um risco acrescido de recorrência. O risco de recorrência e mortalidade é comparável ao dos doentes com melanoma de fase IIIA ou IIIB. Os dados do ensaio da fase aleatória III Keynote-716 foram apresentados no Congresso da OMPE de 2021. Estes mostram uma melhoria significativa na sobrevivência sem recidivas em doentes com melanoma IIB ou IIC em fase completamente ressecada com 12 meses de tratamento adjuvante com o anticorpo anti-PD1 pembrolizumab em comparação com placebo (HR 0,65). O Pembrolizumab ainda não está aprovado para esta indicação.
Valor da terapia sistémica adjuvante na fase IIIA
O prognóstico na fase IIIA do tumor (segundo a 8ª edição da AJCC) é muito bom com uma taxa de sobrevivência de 88% após 10 anos. Este facto levou ao debate se a terapia do sistema adjuvante é um tratamento excessivo para este grupo de pacientes. Pesar o risco de toxicidade grave e possivelmente irreversível contra o benefício potencial é particularmente importante nos doentes com melanoma de fase IIIA.
O ensaio CheckMate-238 não incluiu doentes com melanoma AJCC fase IIIA (7ª edição) [12]. Em contraste, o ensaio EORTC1325/Keynote-54 incluiu doentes com melanoma AJCC fase IIIA (7ª edição) com metástase de gânglios linfáticos superior a 1 mm. No subgrupo de doentes com doença AJCC estágio IIIA (7ª edição), a sobrevivência livre de recaída a um ano foi de 89,8% com terapia pembrolizumab em comparação com 76,8% com placebo (HR 0,32, intervalo de confiança de 99% 0,09 -1,23; p=0,0217). Após reclassificação dos pacientes de acordo com o melanoma AJCC 8ª edição, 8% dos pacientes tiveram um melanoma na fase IIIA do tumor. Em relação à sobrevivência sem recaídas, observou-se um efeito positivo comparável em todos os subgrupos. Note-se que o tempo de seguimento foi muito limitado e que o intervalo de confiança para pacientes com tumores de fase IIIA, de acordo com a 8ª edição da AJCC, foi muito grande [14]. O estudo COMBI-AD também incluiu pacientes com estado tumoral IIIA (AJCC 8ª edição) com metástases de gânglios linfáticos sentinela de >1 mm. Também neste estudo, foi documentado um efeito positivo no que respeita à sobrevivência sem recorrência em todos os subgrupos, mas também com um resultado menos claro para esta fase [8].
Perfil de efeito colateral
Para a terapia adjuvante do melanoma BRAFV600-mutado fase III, estão disponíveis tanto os inibidores do ponto de controlo imunitário nivolumab e pembrolizumab como o tratamento direccionado com os inibidores de BRAF/MEK dabrafenib e trametinib. Os perfis dos efeitos secundários das terapias visadas e dos inibidores do ponto de controlo imunitário diferem significativamente. Embora os efeitos secundários reversíveis sejam mais comuns com terapias específicas, os raros efeitos secundários mediados por imunidade podem ser duradouros e irreversíveis com inibidores do ponto de controlo imunitário [15]. Estes efeitos secundários imuno-mediados podem afectar qualquer órgão. As endocrinopatias estão entre os efeitos secundários imuno-mediados mais comuns e, em contraste com as outras toxicidades, são geralmente irreversíveis. Por conseguinte, requerem uma terapia de substituição vitalícia. As complicações endócrinas mais comuns são a distireose (30%), hipofisitos (5,6 -11%), diabetes mellitus tipo 1 (0,2-2%) e insuficiência adrenal (0,7%), embora também tenham sido descritos casos raros de hipoparatiroidismo. Além disso, os dados limitados disponíveis sugerem que o hipogonadismo primário imunizado devido à orquite, ou o hipogonadismo secundário no contexto da hipofisite, representam riscos potenciais para a infertilidade posterior [16]. Metade de todos os doentes com melanoma de uma coorte nacional dinamarquesa que foram submetidos a terapia adjuvante com nivolumab interromperam prematuramente o tratamento planeado de um ano devido a toxicidade ou recaída. Além disso, foi documentada uma deterioração temporária na qualidade de vida [17].
Toxicidades de grau 3 – 4 associadas à terapia ocorreram em 41% dos pacientes no braço de tratamento (dabrafenib em combinação com trametinib) no estudo COMBI-AD, enquanto que isto só foi visto em 14% dos pacientes do grupo placebo. A pirexia é a razão mais comum para a modificação da dose e descontinuação do tratamento direccionado.
Além disso, os pacientes mostram frequentemente sintomas gerais não específicos, tais como fadiga ou efeitos secundários gastrointestinais no sentido de náuseas. Os efeitos secundários cardíacos (disfunção ventricular esquerda, prolongamento do intervalo QT) ocorrem raramente, embora seja indicado um acompanhamento cardiológico regular. Em geral, deve notar-se que quando ocorrem reacções adversas a medicamentos, muitas vezes é suficiente reduzir a dose de um ou ambos os medicamentos. Os efeitos secundários são geralmente completamente reversíveis após a interrupção da terapia de combinação.
Selecção de terapia de sistema adjuvante na vida quotidiana
Há muito poucos dados sobre toxicidade e taxas de descontinuação de tratamentos da prática diária. Num estudo holandês, foi demonstrado que um total de 93% dos pacientes que se qualificaram para terapia adjuvante receberam tratamento adjuvante anti-PD-1. Estes dados mostraram uma taxa de toxicidade mais elevada com descontinuidades de tratamento prematuras consecutivas mais frequentes. A sobrevivência sem recorrência foi comparável à dos ensaios cruciais [18].
Para pacientes com melanoma do tipo selvagem BRAF, o bloqueio PD-1 é a terapia adjuvante de escolha. Para doentes com BRAFV600E/K-mutated melanoma, o risco de eventos adversos persistentes mediados por imunidade com imunoterapia deve ser considerado ao escolher o tratamento adjuvante, uma vez que a razão de perigo para a sobrevivência sem recorrência é comparável nos três ensaios de tratamento adjuvante. A escolha da terapia deve, portanto, ser discutida com os pacientes e feita em conjunto.
Mensagens Take-Home
- A espessura do tumor vertical de acordo com Breslow e a presença de ulceração são os factores prognósticos mais importantes.
- Os diagnósticos patológicos moleculares usando sequenciação da próxima geração (NGS) para determinar o estado do BRAF devem ser efectuados a partir da fase III.
- Uma biópsia do gânglio linfático sentinela (SLNB) é recomendada para uma fase pT1b (ou seja, uma espessura de tumor de acordo com Breslow de >0,8 mm ou <0,8 mm com ulceração) de acordo com a 8ª edição do AJCC. A dissecção dos gânglios linfáticos é indicada no caso de envolvimento de gânglios linfáticos macroscópicos, mas não é recomendada no caso de um gânglio linfático sentinela positivo.
- A terapia sistémica adjuvante com um anticorpo monoclonal anti-PD-1 ou inibidores de BRAF/MEK é recomendada a partir da fase IIIA com metástase de gânglios linfáticos sentinela >1 mm.
- A escolha da terapia do sistema adjuvante é baseada na indicação, bem como na aprovação, tendo em conta o estado de mutação BRAF e o perfil de efeito secundário.
Literatura:
- Siegel RL, Miller KD, Jemal A: Estatísticas do cancro, 2018. A Cancer Journal for Clinicians 2018; 68(1): 7-30.
- Akbani R, et al: Genomic Classification of Cutaneous Melanoma. Célula 2015; 161(7): 1681-1696.
- Hayes AJ, et al: margens de excisão amplas versus estreitas para melanomas cutâneos primários de alto risco: acompanhamento a longo prazo da sobrevivência num ensaio aleatório. The Lancet Oncology 2016; 17(2): 184-192.
- Morton DL, et al: Relatório final do julgamento da Biópsia do Nó Sentinela versus Observação Nodal em Melanoma. New England Journal of Medicine 2014; 370(7): 599-609.
- Leiter U, et al: Análise Final do Ensaio DeCOG-SLT: Sem Benefício de Sobrevivência para a Dissecção Completa do Nódulo Linfático em Pacientes com Melanoma com Nódulo Sentinela Positivo. J Clin Oncol 2019; 37(32): 3000-3008.
- Faries MB, et al: Completion Dissection or Observation for Sentinel-Node Metastasis in Melanoma. N Engl J Med 2017; 376(23): 2211-2222.
- Michielin O, et al: Cutaneous melanoma: ESMO Clinical Practice Guidelines for diagnosis, treatment and follow-updagger. Ann Oncol 2019; 30(12): 1884-1901.
- Dummer R, et al: Five-Year Analysis of Adjuvant Dabrafenib plus Trametinib in Stage III Melanoma. N Engl J Med 2020; 383(12): 1139-1148.
- Eggermont AMM, et al: Adjuvant pembrolizumab versus placebo em melanoma de fase III ressecado (EORTC 1325-MG/KEYNOTE-054): resultados de sobrevivência sem metástases à distância de um ensaio de fase 3 duplo-cego, aleatorizado, controlado. The Lancet Oncology 2021; 22(5): 643-654.
- Ascierto PA, et al: Adjuvant nivolumab versus ipilimumab na fase IIIB-C ressecada e melanoma da fase IV (CheckMate 238): resultados de 4 anos de um ensaio multicêntrico, duplo-cego, aleatorizado, controlado, fase 3. A Lancet Oncologia. 2020. 21(11): 1465-1477.
- Long GV, et al: Adjuvant dabrafenib mais trametinib na fase IIIBRAF-mutated melanoma. New England Journal of Medicine 2017; 377(19): 1813-1823.
- Weber J, et al: Adjuvant nivolumab versus ipilimumab na fase III ou IV do melanoma ressecado. New England Journal of Medicine 2017; 377(19): 1824-1835.
- Zimmer L, et al: Adjuvant nivolumab plus ipilimumab ou nivolumab monotherapy versus placebo em doentes com melanoma de fase IV ressecado sem evidência de doença (IMMUNED): um ensaio aleatório, duplo-cego, controlado por placebo, fase 2. The Lancet 2020; 395(10236): 1558-1568.
- Eggermont AMM, et al: Valor prognóstico e preditivo da encenação do AJCC-8 na fase III EORTC1325/KEYNOTE-054 ensaio de pembrolizumab vs placebo em melanoma ressecado de alto risco da fase III. European Journal of Cancer 2019; 116: 148-157.
- Ghisoni E, et al: Acontecimentos adversos relacionados com imunodeficiências tardias e duradouras dos inibidores do ponto de controlo imunitário: Um aspecto negligenciado na imunoterapia. Eur J Cancro. 2021. 149: 153-164.
- Ozdemir BC: Hipogonadismo e infertilidade relacionados com o ponto de controlo imunitário: uma questão negligenciada na imuno-oncologia. J Immunother Cancer 2021; 9(2).
- Ellebaek EEA: Um estudo a nível nacional, da vida real dos resultados e da qualidade de vida após a introdução da imunoterapia adjuvante para doentes dinamarqueses com melanoma. ESMO Abstract 1071P, 2021.
- De Meza MEA: Tratamento adjuvante do melanoma na prática clínica: ensaio versus realidade. ESMO Abstract 1070P, 2021.
InFo ONCOLOGy & HEMATOLOGy 2021; 9(6): 10-15