Estão disponíveis dois tipos de terapia baseada em células T para o linfoma difuso de grandes células B (DLBCL) refratário ou recidivante: Células T CAR e anticorpos biespecíficos. Embora as células T CAR tenham revolucionado a medicina individualizada até certo ponto, os anticorpos biespecíficos genericamente disponíveis também oferecem vantagens. O tratamento com anticorpos rapidamente disponíveis confirmou agora o seu perfil de eficácia duradouro no seguimento de 2 anos do estudo EPCORE NHL-1.
O DLBCL é a forma mais comum de linfoma não Hodgkin heterogéneo e agressivo. Enquanto os doentes que respondem à terapêutica de primeira linha têm boas hipóteses de cura ou sobrevivência, os doentes refractários e recidivantes (R/R) que não são elegíveis para um transplante de células estaminais têm um mau prognóstico de apenas cerca de 6,3 meses, em média [1]. Estão atualmente disponíveis várias abordagens terapêuticas baseadas em células T para DLBCL R/R agressivo após dois pré-tratamentos sistémicos [1].
Células T CAR e anticorpos biespecíficos
A terapia com células T CAR utiliza células T geneticamente modificadas para reconhecer antigénios de superfície sobre-expressos nas células cancerígenas e atacá-las especificamente. Esta tecnologia é utilizada em centros especializados e revolucionou o panorama terapêutico em várias indicações hemato-oncológicas, incluindo o DLBCL. É personalizada para cada doente e conduz a uma resposta muito boa nos doentes [2,3]. Os possíveis efeitos secundários do tratamento com células T CAR a que deve ser dada especial atenção são a síndrome de libertação de citocinas (SRC) e a síndrome de neurotoxicidade associada às células imunitárias efectoras (ICANS) [2]. Se os doentes não forem elegíveis para a terapêutica com células T CAR, por exemplo, porque a progressão rápida da doença impossibilita o período de espera ou porque já foi tentada a terapêutica com células T CAR, o anticorpo biespecífico epcoritamab também pode ser utilizado para o DBCLC R/R após pré-tratamento sistémico em, pelo menos, duas linhas de terapêutica. Este anticorpo genérico liga-se tanto a um epítopo de CD20, que se encontra na maioria das células B de um linfoma de células B, como a CD3, que é expresso nas células T. A ligação simultânea de células tumorais que expressam CD20 e células T endógenas que expressam CD3 medeia a ativação específica das células T [4]. Para além da pirexia e da neutropenia, a SRC é também considerada um efeito secundário potencialmente grave desta opção de tratamento [1].
Alternativa eficaz para doentes com DLBCL
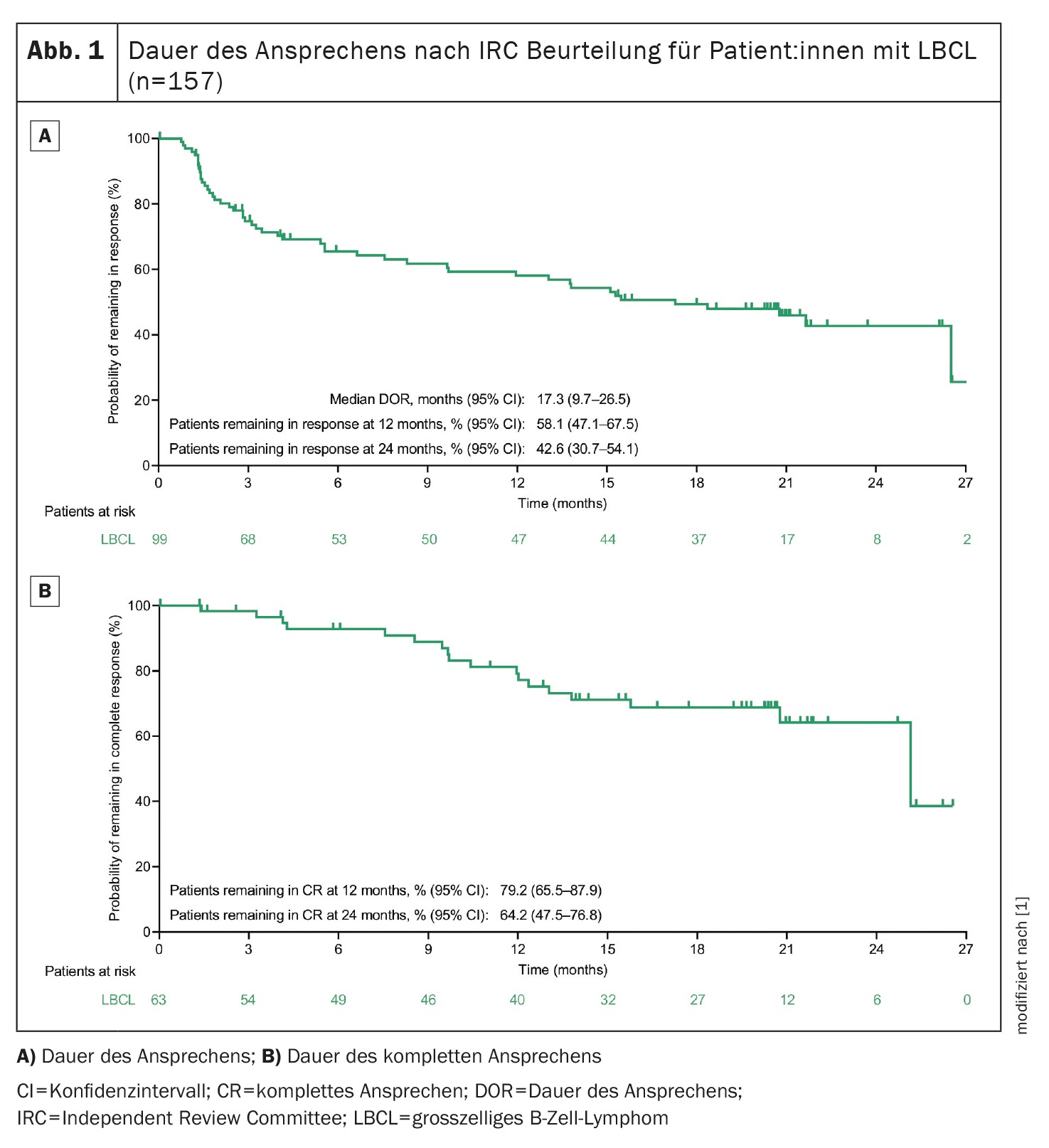
O seguimento de 2 anos do ensaio EPCORE NHL-1 de fase 1/2 em curso, que está a investigar o anticorpo biespecífico epcoritamab em doentes com R/R (D)LBCL, acaba de ser publicado [1]. Foram incluídos 157 doentes com (D)LBCL em monoterapia com epcoritamab e a análise primária já tinha mostrado uma taxa de resposta global (ORR) de 63,1% e uma taxa de resposta completa (CR) de 38,9%. Além disso, 45,8% dos doentes analisados relativamente à doença residual mínima (DRM) obtiveram negatividade da DRM [5]. Após um seguimento mediano de 25,1 meses (95% CI, 24,0-26,0), 63,1% dos doentes responderam ao tratamento (ORR, n/N=99/157; 95% CI, 55,0-70,6) e 40,1%** (n/N=63/157; 95% CI, 32,4-48,2) alcançaram uma RC na análise atual do estudo. A taxa estimada de sobrevivência sem progressão (PFS) aos 2 anos foi de 27,8% e a taxa estimada de sobrevivência global (OS) foi de 44,6% [1]. O seguimento mediano para a duração da resposta (DOR) foi de 20,8 meses (IC 95%, 20,1-21,2) e a DOR mediana foi de 17,3 meses (IC 95%, 9,7-26,5) (Fig. 1) [1]. Estima-se que 64,2% dos pacientes com RC também a apresentaram após 2 anos. A taxa de RC foi consistente com a população geral, independentemente dos subgrupos (por exemplo, idade, estado ECOG, número de tratamentos anteriores, terapia prévia com células CAR T, refractária à última terapia anti-CD20, DLBCL de novo vs. transformado) [1]. A negatividade de MRD foi detectada em 54 dos 119 doentes avaliáveis por MRD (45,4%; IC 95%, 36,2-54,8). A RC e a negatividade da MRD foram associadas a PFS e OS a longo prazo [1].
** por Comité Independente de Revisão (IRC) com base nos critérios de Lugano
Os efeitos secundários mais comuns com o anticorpo biespecífico epcoritamab foram a SRC (51,0%), a pirexia (24,8%), a fadiga (24,2%) e a neutropenia (23,6%). A fadiga foi mais comum durante as primeiras 8 semanas de tratamento do que nas fases posteriores, enquanto a ocorrência de neutropenia foi consistente ao longo do período de tratamento [1]. Os acontecimentos adversos relacionados com o tratamento que levaram à sua interrupção ocorreram em 23 doentes (14,6%). Não foram registados novos casos de ICANS, SRC ou síndrome de lise tumoral clínica (SLT) durante o período de acompanhamento [1].
Conclusão
Embora a terapia com células T CAR tenha revolucionado o panorama do tratamento para algumas indicações hemato-oncológicas, há doentes que não são elegíveis para esta terapia ou que apresentam progressão após o tratamento personalizado. Os doentes com DLBCL podem beneficiar da opção tolerável e genericamente disponível do anticorpo biespecífico epcoritamab [1,3,4]. A resposta duradoura em doentes com DLBCL R/R com mau prognóstico foi confirmada no seguimento de 2 anos recentemente publicado do estudo EPCORE-NHL-1 [1].
Literatura:
- Thieblemont C, et al: Epcoritamab no linfoma de grandes células B recidivante/refratário: seguimento de 2 anos do ensaio principal EPCORE NHL-1. Leucemia 2024.
- Chohan KL, Siegler EL, Kenderian SS: Terapia celular CAR-T: o equilíbrio entre eficácia e toxicidade. Curr Hematol Malig Rep 2023; 18(2): 9-18.
- Neelapu SS, et al: O acompanhamento de cinco anos do ZUMA-1 apoia o potencial curativo do axicabtagene ciloleucel no linfoma refratário de grandes células B. Sangue 2023; 141(19): 2307-2315.
- Informação actualizada para profissionais de saúde Tepkinly® (epcoritamab); www.swissmedicinfo.ch.
- Thieblemont C, et al: Epcoritamab, um novo anticorpo subcutâneo CD3xCD20 biespecífico para células T, no linfoma de grandes células B recidivante ou refratário: Expansão da dose num ensaio de fase I/II. J Clin Oncol 2023; 41(12): 2238-2247.
InFo ONKOLOGIE & HÄMATOLOGIE 2024; 12(6): 28-29
Imagem da capa: Micrografia de um linfoma difuso de grandes células B, abreviado DLBCL. Amostra de FNA de gânglio linfático. Coloração de campo. © Nephron, wikimedia