Pequenas alterações feitas na actualização de 2022 BCLC podem ter grande impacto na terapia local de doentes com CHC fase 0 a C. As terapias combinadas e outras medidas interdisciplinares mostram melhorias curativas. Que pacientes são adequados para que tipos de terapia em que fase da doença se explica com base nas possibilidades, limitações e perspectivas futuras das terapias locorregionais no HCC.
Uma extensão actual da representação do algoritmo BCLC na norma BCLC de 2022 [1] dá lugar a discussão. Os tipos de terapias e vias de tratamento do carcinoma hepatocelular (HCC) aí delineados foram apenas complementados por pequenas diferenças. Mas são precisamente estes “passos laterais” que representam oportunidades interessantes e boas, explicou o Professor Dr Roman Klöckner da Clínica e Policlínica de Diagnóstico e Radiologia Intervencionista do Centro Médico da Universidade de Mainz (D) [2].
Para a fase muito precoce (0) e precoce (A) do HCC, as opções terapêuticas até agora têm sido a ablação, a ressecção e, se necessário, o transplante. A escolha certa para o paciente individual depende, por exemplo, dos conhecimentos do centro, das opções de radiologia interventiva, da opção de transplante e da experiência do cirurgião hepático. Um desafio especial, porém, são os próprios pacientes, cujos quadros clínicos são conhecidos por serem altamente complexos e com processos tumorais muito heterogéneos. O próprio facto de se ter de lidar sempre com dois quadros clínicos simultâneos – com cirrose hepática, por um lado, e HCC, por outro. Devido às muitas imagens diferentes de tumores e a uma gama de opções de intervenção, a discussão interdisciplinar de cada paciente individual no quadro tumoral é, portanto, essencial, diz o Prof. Klöckner. Estes pacientes devem ser discutidos intensivamente, não apenas uma vez, mas antes de cada nova medida ou ciclo.
Uma possível terapia local curativa para o carcinoma hepatocelular muito precoce e precoce é “cozinhá-lo” de forma minimamente invasiva por meio da ablação e do uso de micro ou ondas de rádio. O Professor Klöckner referiu-se à chamada “Técnica Sem Toque” como um exemplo, que não perfura directamente no tumor mas sim imediatamente junto a ele. Esta abordagem goza de muito bons resultados e tem também três vantagens, como explicou o perito:
- Redução do risco de proliferação de células tumorais
- Risco de ruptura de tumores em focos exóticos praticamente nulo
- Complicação da fístula biliopleural sob controlo
Embora as taxas de recidiva sejam mais elevadas do que na cirurgia em todos os estudos, não se traduzem numa taxa de sobrevivência mais baixa, pelo que a ablação pode certamente ser considerada aqui equivalente à cirurgia.
Combinação poderosa: Ablação + TACE
A combinação com a quimioembolização percutânea trans-arterial (TACE) torna possível a ablação de tumores até um corte de 7 cm. Isto porque o fluxo sanguíneo chega a um impasse no tumor bem embolizado. O próprio arrefecimento do tumor é assim eliminado, o resultado é uma propagação mais homogénea do calor e, portanto, zonas de ablação um pouco maiores. Se for necessário, abater com duas agulhas e de várias posições ou sobreposição.
Mesmo nesta fase, que até há pouco tempo era mais ou menos terapeuticamente dominada pelos radiologistas, há mudanças. A terapia do sistema significativamente melhorado já oferece uma alternativa completa à radiologia em alguns pacientes, e também aqui a discussão interdisciplinar abre o caminho para colocar o paciente no caminho da terapia. Hoje em dia, segundo o Prof. Klöckner, já não se deve cometer o erro de colocar o paciente numa “TACE interminável” uma vez. Os desafios, especialmente com o BCLC B, são mais complexos do que poderiam aparecer num fluxograma S3, e muitos deles não são mapeados na directriz. Estes incluem a diferente carga tumoral e função hepática, o padrão de crescimento e localização do tumor, o fornecimento vascular, etc. Nem todos os doentes respondem igualmente bem ao TACE e por vezes beneficiam mais, por vezes menos desta terapia.
Muitos factores determinam os prós e os contras da terapia locorregional (visão geral 1), incluindo, por exemplo, problemas vasculares: se um paciente tem um stent de canal biliar, isto argumenta contra o TACE e a favor da terapia do sistema ou da radioembolização. Esta última não conduz a necrose directa e, portanto, não conduz a qualquer risco de infecção, como pode acontecer com TACE, mas decompõe lentamente o tumor.

Pequenos passos laterais – grande efeito
A classificação em pró e contra TACE mostra a dimensão dos pequenos passos laterais nos tipos de terapia mencionados no início: os casos classificados como “contra TACE” e que são classificados na fase intermédia na directriz teriam sido embolizados mais cedo. Hoje em dia, eles são, de qualquer forma, tratados principalmente com terapia sistémica e podem também ser tratados com sucesso locoregionalmente se a resposta for boa.
É possível destruir uma carga tumoral elevada com TACE. No entanto, uma vez que a resposta do TACE demonstrou estar ligada ao tamanho do tumor, sabemos que tais tumores não respondem tão bem. Existe também um risco de síndrome grave pós-embolização se a carga tumoral for elevada.
A invasão macrovascular é frequentemente negligenciada pelo radiologista, e no entanto afecta um terço dos doentes durante o curso da doença. Mesmo aqueles que são formalmente classificados como BCLC C e que seriam assim claramente “candidatos à terapia do sistema” podem agora possivelmente ser tratados locoregionalmente. Alguns dados, especialmente do Japão, mostram uma abordagem curativa mesmo para intervenções cirúrgicas nesta fase para pequenas infiltrações. Devido à situação de dados muito pobre, a última palavra ainda não foi dita. O Prof. Klöckner vê o TACE criticamente aqui, se, então, ele ainda trataria com SIRT.
SIRT: apenas adequado para alguns – mas depois realmente bom
Devido à má situação dos dados causada pelo fracasso dos estudos SARAH e SIRveNIB, o SIRT foi mais ou menos anulado. Na fase avançada, com poucas excepções, já não é um problema, especialmente porque também é caro e necessita de uma boa justificação. No entanto, existem também aqui pequenos nichos onde SIRT fornece resultados valiosos na opinião do Prof. Klöckner.
Em pacientes que não querem ser operados devido a hipertensão ou que não querem ser abortados devido à proximidade do tumor ao canal biliar ou ao vaso, pode-se ter sucesso com SIRT super-selectivo – pelo menos ao nível segmentar ou ainda mais selectivo. É necessária uma dosimetria correspondentemente individualizada. Com min. 210 Dose tumoral cinzenta até à gama de quatro dígitos em alguns casos, o segmento tipicamente triangular é tratado. Neste caso, o SIRT é curativo, embora não de um dia para o outro.
Uma última alteração diz respeito à inclusão do Conceito de Migração em Etapa de Tratamento na actualização do BCLC. Isto é importante porque permite aos terapeutas alterar a terapia normalmente pretendida no caminho de orientação, dando boas razões. Por exemplo, para tratar um paciente que tenha respondido excelentemente à terapia do sistema com uma terapia locoregional. O Prof. Klöckner sublinhou mais uma vez a importância de um bom intercâmbio entre todas as disciplinas a fim de fazer justiça a estes pacientes complexos.
TACE/SIRT plus imunoterapia – novo incêndio para o sistema?
A combinação de TACE e TKI demonstrou ser negativa em vários estudos, em última análise a toxicidade era demasiado elevada e, por conseguinte, a conformidade era fraca. Isto contrasta com a combinação de TACE/SIRT mais imunoterapia, que tem um perfil de efeito secundário mais favorável e pode, portanto, ser combinada muito melhor (Fig. 1) [3].
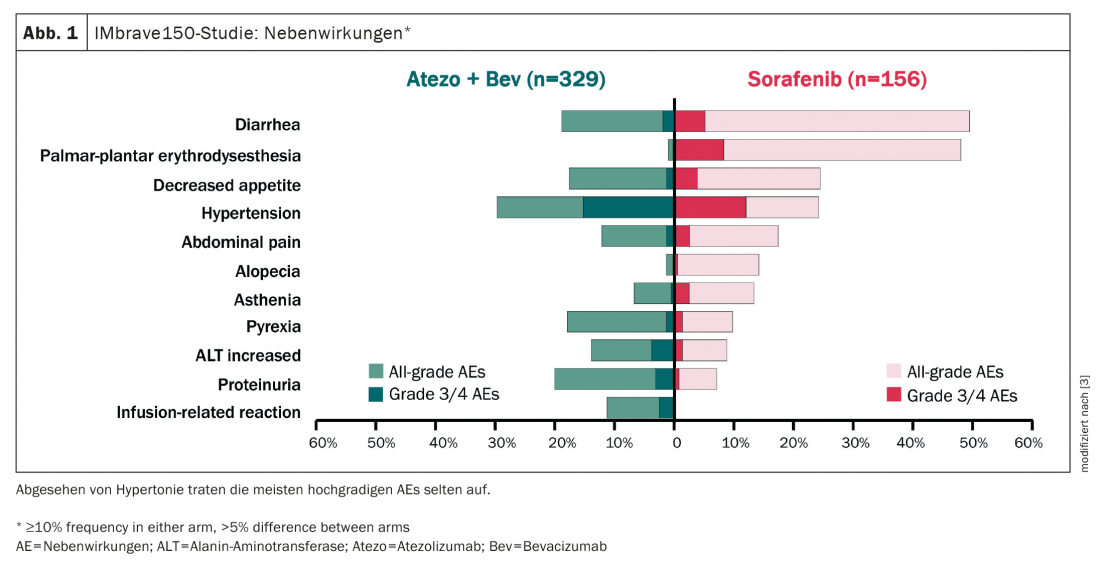
Uma tal combinação também tem a esperança de estimular o sistema imunitário com a terapia combinada. A resposta à imunoterapia, por si só, era ainda fraca, com 27%. No entanto, juntamente com o TACE/SIRT, espera-se uma maior taxa de resposta através da via de destruição de tumores, libertação de TAAs, estimulação do sistema imunitário e, espera-se, uma resposta mais forte da imunoterapêutica contra o HCC. No caso terapêutico ideal, ocorre não só um aditivo mas até mesmo um efeito sinergético.
Congresso: GI-Oncologia 2022
Literatura:
- Reig M, Forner A, Rimola J, et al: Estratégia BCLC para previsão de prognóstico e recomendação de tratamento: A actualização de 2022. J Hepatol 2022; 76(3): 681-693; doi: 10.1016/j.jhep.2021.11.018.
- GI-Oncologia 2022 – 18ª Actualização Interdisciplinar; Evento em sala de aula em 11.6.2022 em Wiesbaden (D)
- Galle PR, Finn RS, Qin S, et al: ASCO GI 2020; Abstr 476; doi: 10.1200/JCO.2020.38.4_suppl.476.
InFo ONCOLOGY & HEMATOLOGY 2022; 10(4): 28-29