Que medicamentos são adequados para a radiochemoterapia neoadjuvante? Se houver uma resposta clínica completa, devemos esperar ou operar? E que pacientes beneficiam de tratamento adjuvante? Estas foram algumas das questões discutidas no EORTC GICC em St. Gallen no início de Março.
(rs) “Em até 30% das pessoas com cancro rectal distal avançado, a radiochemoterapia pré-operatória (neoadjuvante) (RCT) pode alcançar uma resposta patológica (pCR) e clínica completa (cCR), evitando potencialmente a cirurgia radical”, disse a Prof. Angelita Habr-Gama, MD, São Paulo, no EORTC GICC em St Gallen. Com o objectivo de padronizar o procedimento no diagnóstico de tumores, o Prof. Habr-Gama e colegas definiram critérios clínicos e endoscópicos para a resposta clínica e, com base nisto, o procedimento posterior [1]. Para além do procedimento normalizado, o calendário da avaliação do tumor também desempenha um papel importante. “Vários estudos mostram que a avaliação deve ter lugar no mínimo sete a oito semanas após o fim do neoadjuvante RCT”, disse o Prof. Ela referiu-se a um estudo de Kalady et al. que mostrou que um intervalo de tempo de mais de oito semanas entre o fim do RCT neoadjuvante e a cirurgia estava associado a um pCR significativamente mais elevado [2]. A sobrevivência global (OS) ou sem doenças (DFS) não foi afectada pela avaliação retardada de tumores em estudos.
“Vigiar e Esperar” ou operar imediatamente?
O pré-requisito para o protocolo “Vigiar e Esperar” apresentado pelo Prof. Habr-Gama e utilizado desde 1991 é uma resposta clínica completa após a RCT neoadjuvante (Fig. 1) .
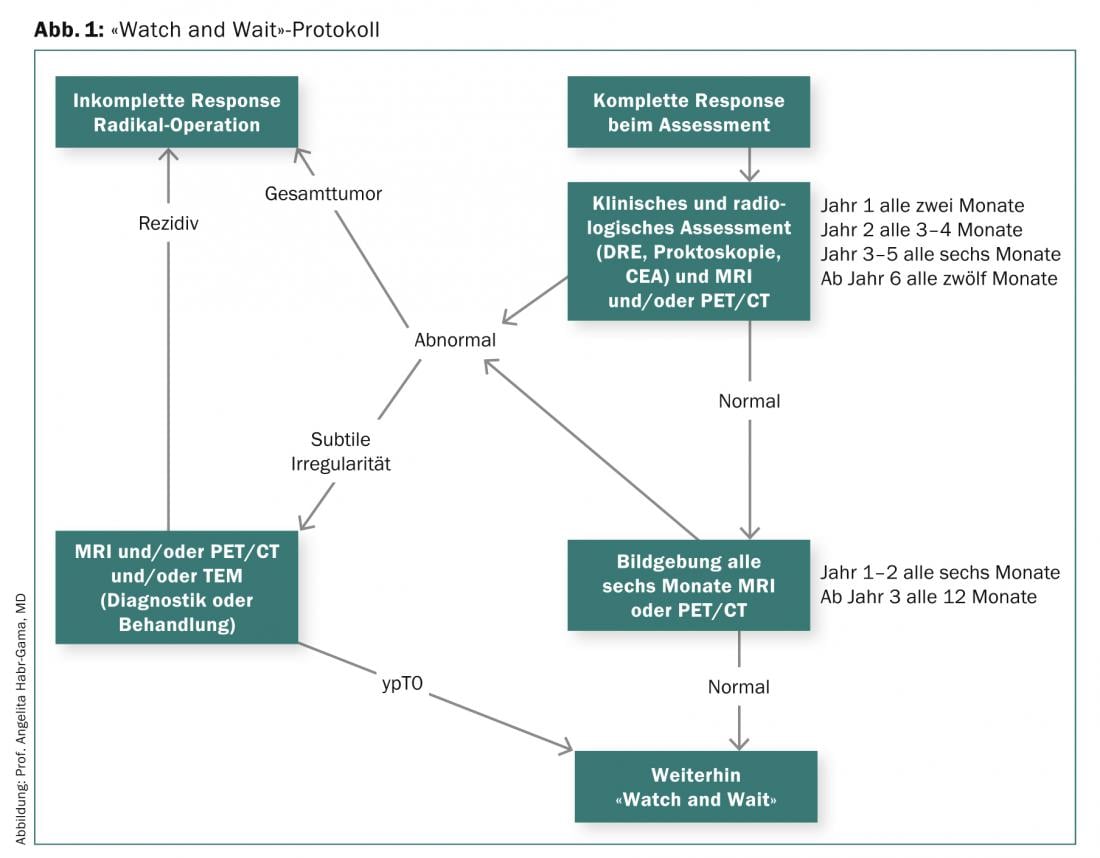
Como mostram os resultados a longo prazo de um estudo de 265 pacientes com cancro rectal distal que foram submetidos a cirurgia radical (resposta incompleta) ou a seguimento (cCR) após a TCR neoadjuvante, a taxa de sobrevivência global e sem doença foi de 84 vs. 97,7%. Após cinco anos, a taxa de sobrevivência global foi de 88 no grupo de ressecção e 100 no grupo de observação, e a taxa de sobrevivência sem doenças foi de 83 e 92%. Para aumentar o número de pacientes em que a cirurgia radical pode ser evitada, o Prof. Habr-Gama e colegas investigaram o impacto da TCR neoadjuvante prolongada com doses de radiação mais elevadas, ciclos de quimioterapia mais frequentes e um intervalo mais longo até à avaliação do tumor [3]. O regime terapêutico investigado conduziu inicialmente ao cCR em 68% dos pacientes. Nos primeiros doze meses, 17 e no curso (>12 meses) mais 10% desenvolveram uma recorrência local. Metade dos 70 pacientes incluídos não necessitaram de cirurgia a longo prazo (seguimento médio de 56 meses).
Parceiros ideais para o neoadjuvant RCT
A resposta à questão de qual quimioterapia é mais adequada para combinação com radioterapia no tratamento adjuvante do cancro rectal localmente avançado é complicada pela diferente administração das fluoropiramidinas. “Sabemos através de estudos pós-operatórios que o 5-FU mais a radioterapia é um tratamento activo e que a administração contínua de i.v. durante a radioterapia é superior às injecções de bolus”, disse o Prof. Hans-Joachim Schmoll, MD, da Universidade Alemã de Halle. O Prof. Schmoll respondeu se a capecitabina 5-FU oral é preferível à forma i.v. de 5-FU no tratamento perioperatório com base numa publicação de Hofheinz e colegas. Isto mostrou uma vantagem de sobrevivência significativa para a capecitabina após cinco anos (76 vs. 67% p=0,0004) [4]. Os resultados do ensaio NSABP-R-04 publicado na ASCO 2013, que investigou o tratamento com capecitabina mais radioterapia (RT) em dois dos quatro braços e um RCT com infusão contínua de baixa dose de 5-FU, mostraram um resultado comparável [5]. “Os resultados do estudo mostram um tratamento comparativamente eficaz”, disse o Prof. Schmoll. “No entanto, devido à sua administração mais fácil, a capecitabina deve ser preferida à 5-FU”.
A questão da TCR à base de fluoropiramidina mais oxaliplatina para a TCR neoadjuvante em cancro do cólon localmente avançado foi investigada utilizando cinco ensaios: STAR, ACCORD/Prodige2, NSABP R-04, ARO/CAO/AIO 04, PETACC-6. Apenas o ensaio ARO/CAO/AIO-04 mostrou um pCR significativamente mais elevado (17 vs. 13%, p=0,038) [6]. Todos os outros estudos foram negativos a este respeito. No entanto, tal como demonstrado pelo referido ensaio NSABP-R-04, que investigou um RCT neoadjuvante com fluoropyrimidinas mais oxaliplatina nos dois braços restantes, a toxicidade aumentou significativamente com a combinação.
Um RCT neoadjuvante com capecitabina e irinotecan foi investigado em ensaios mais pequenos. Estes mostraram taxas de pCR entre 9 e 27% e uma elevada taxa de ressecção R0. A combinação com o inibidor VEGF bevacizumab pareceu inicialmente promissora. “Os resultados dos estudos das fases I e II com taxas de pCR entre 16 e 36% não sugerem que a combinação com bevacizumab contribua significativamente para um resultado melhorado”, disse o Prof. Schmoll. O mesmo se aplica ao inibidor EGFR cetuximab.
Quimioterapia adjuvante
A questão da quimioterapia pós-operatória (adjuvante) no tratamento do cancro rectal foi muito menos clara. Embora haja um consenso generalizado de que a quimioterapia adjuvante é benéfica em doentes de alto risco. No entanto, esta conclusão indirecta é retirada de estudos mais antigos com doentes que, na sua maioria, não tinham recebido terapia neoadjuvante. Em contraste, sabe-se pelos ensaios da EORTC que os pacientes que responderam bem à terapia neoadjuvante beneficiam mais da TC adjuvante [7]. Para tratamento adjuvante, é recomendada uma terapia de seis meses com 5-FU ou capecitabina. A informação sobre a combinação com oxaliplatina no adjuvante CT será fornecida pelos resultados iniciais dos ensaios PETACC-6 e ARO/CAO/AIO-04. Espera-se que estes sejam apresentados na ASCO 2014.
Fonte: “Issues in combined modality treatment for rectal cancer”,2nd St. Gallen EORTC (European Organisation for Research and Treatment of Cancer) Gastrointestinal Cancer Conference (GICC) 2014, 7 de Março de 2014, St.
Literatura:
- Habr-Gama A, et al.: Resposta clínica completa após quimiorradiação neoadjuvante para cancro rectal distal: caracterização de achados clínicos e endoscópicos para normalização. Dis Colon Rectum 2010; 53(12): 1692-1698.
- Kalady MF, et al: Factores preditivos de resposta patológica completa após quimiorradiação neoadjuvante para o cancro rectal. Ann Surg 2009; 250(4): 582-589.
- Habr-Gama, et al: Vigiar e esperar pela abordagem de quimiorradiação neoadjuvante prolongada para o cancro rectal distal: estamos a aproximar-nos da gestão do cancro anal? Dis Colon Rectum 2013; 56(10): 1109-1117.
- Hofheinz RD, et al: Quimioradioterapia com capecitabina versus fluorouracil para cancro rectal localmente avançado: um ensaio aleatório, multicêntrico, não-inferioritário, fase 3. Lancet Oncol 2012; 13(6): 579-588.
- Roh MS, et al: The impact of capecitabine and oxaliplatin in the pre-operative multimodality treatment in patients with carcinoma of the rectum: NSABP R-04. J Clin Oncol 29: 2011 (suppl; abstr 3503).
- Rödel C, et al: Quimioterapia pré-operatória e quimioterapia pós-operatória com fluorouracil e oxaliplatina versus fluorouracil apenas em cancro rectal localmente avançado: resultados iniciais do ensaio alemão CAO/ARO/AIO-04 fase 3 aleatorizada. Lancet Oncol 2012; 13(7): 679-687.
- Collette L, et al: Pacientes com ressecção curativa do cancro rectal cT3-4 após radioterapia pré-operatória ou radiochemoterapia: alguém beneficia de quimioterapia adjuvante à base de fluorouracil? Um ensaio da Organização Europeia de Investigação e Tratamento da Oncologia por Radiação Cancro. J Clin Oncol 2007; 25(28): 4379-4386.
InFo ONCOLOGy & HEMATOLOGy 2014; 2(4): 25-27











