Uma melhor compreensão da patogénese das doenças psoriásicas contribuiu para uma nova geração de biólogos nos últimos anos. Os representantes modernos actualmente aprovados deste grupo de terapêuticas de sistemas interagem todos com a resposta imunitária Th17. Devido à multiplicidade de opções de terapia sistémica, a escolha do tratamento individualmente adequado tornou-se mais desafiante.
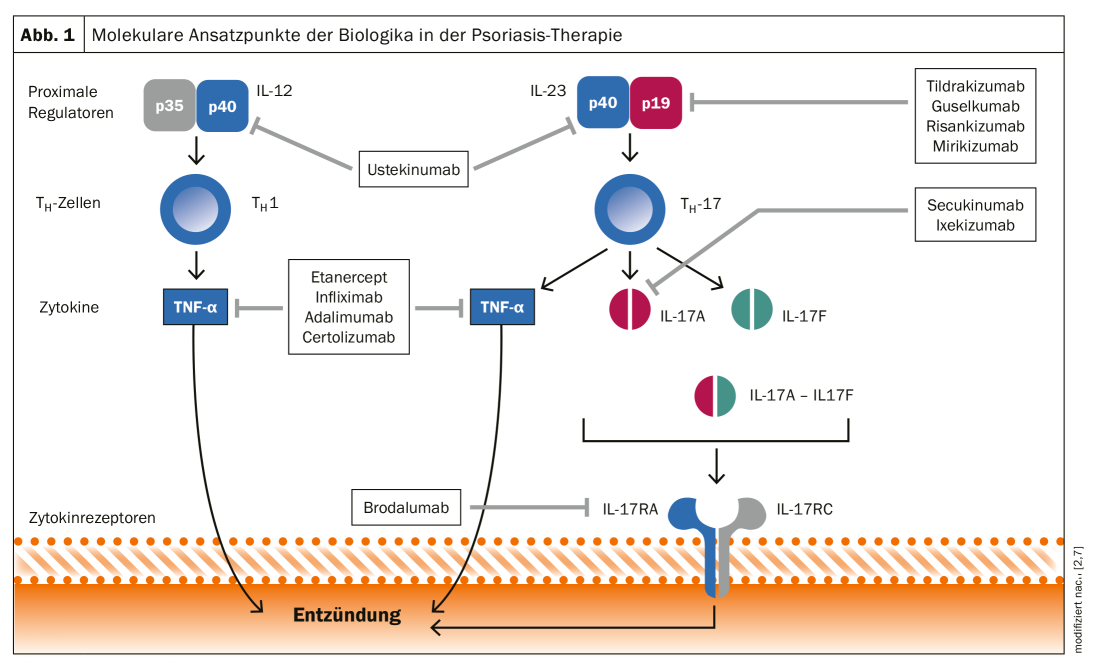
A gama de substâncias activas sistemicamente aplicáveis expandiu-se significativamente nas últimas duas décadas. Enquanto o espectro para o tratamento da psoríase de placa moderada a grave* estava inicialmente limitado às terapias do sistema oral metotrexato, ciclosporina, acitretina, fumarato de dimetilo e apremilast, um grande número de biólogos e biosimilares mais modernos estão agora disponíveis para além dos inibidores de TNF-α. Este desenvolvimento baseia-se numa compreensão cada vez mais diferenciada da base patogénica da psoríase. Como é agora conhecido, a resposta imunitária Th17 em particular, com as suas citocinas IL23 e IL17, desempenha um papel central [10]. Esta é a base para a nova geração de biólogos que interagem com a resposta imunitária Th17 (Fig. 1) [2].
* BSA = Área de superfície corporal >10%, PASI = Área de psoríase e índice de gravidade >10, DLQI = Índice de qualidade de vida dermatológica >10
De acordo com o entendimento actual, a psoríase é considerada como uma doença sistémica em que existe uma desregulação geneticamente determinada do sistema imunitário e ocorre uma auto-imunidade contra os antigénios da pele do próprio corpo. Também ocorrem frequentemente perturbações comorbidas. Na artrite psoriásica, as queixas articulares reumáticas são características, para além das manifestações cutâneas. Além disso, doenças intestinais, obesidade, diabetes e doenças cardiovasculares são frequentemente relatadas comorbidades. Além disso, a prevalência de doenças mentais, tais como distúrbios de ansiedade e depressão, é também aumentada na psoríase. Enquanto o PASI-50 ou PASI-75 costumavam ser objectivos realistas para o tratamento da psoríase, actualmente o PASI-90 e o PASI-100 estão dentro do reino das possibilidades [3]. Contudo, com tantos biólogos disponíveis, a escolha do tratamento individual óptimo para a psoríase moderada a grave torna-se um desafio.
Terapia adaptada ao paciente
Os factores de decisão para a terapia do sistema podem ser divididos em quatro grupos (Visão Geral 1): Critérios clínicos, características dos medicamentos, características dos doentes, aprovação e regulamentação [8]. Como base para a selecção do tratamento, devem ser clarificados outros critérios em casos individuais, para além das recomendações baseadas em provas das actuais directrizes. São necessários mais estudos para melhor compreender factores como a eficácia a longo prazo, duração da resposta, segurança e impacto sobre as comorbilidades. Dados empíricos válidos podem facilitar a oferta de uma terapia individualmente apropriada que se caracteriza por uma pele sem aparência a longo prazo, longa sobrevivência do medicamento e elevados índices de satisfação do paciente [9]. É também importante ter em conta as preferências dos pacientes. Em geral, a rápida melhoria dos sintomas cutâneos e a ausência de lesões estão entre os critérios mais importantes para o sucesso [1]. De acordo com dados da Rede Suíça de Dermatologia de Terapias Orientadas (SDTT), a idade e o sexo são factores estratificantes no que diz respeito às necessidades dos doentes. Enquanto que os pacientes com mais de 65 anos de idade têm uma menor frequência de consultas médicas, uma boa tolerância da medicação, bem como a qualidade do sono e a confiança na terapia como importantes, os pacientes mais jovens são mais susceptíveis de considerar importante que a sua vida social não seja restringida [1].

Perda de impacto como um desafio
Um dos maiores desafios no desenvolvimento futuro da terapêutica da psoríase sistémica relaciona-se com a perda secundária da eficácia da biologia [3]. Após um certo período de tratamento, o efeito terapêutico diminui com a consequência de que é utilizada uma substância activa diferente. Neste contexto, fala-se também de “sobrevivência da droga”, ou seja, a duração desde o início de uma terapia até à sua descontinuação [4,11]. Os preditores de sobrevivência das drogas podem ser úteis na escolha entre diferentes biólogos [11]. Uma meta-análise publicada em 2019 identificou vários preditores (incluindo género, obesidade e artrite psoriásica) que foram considerados relevantes para a interrupção ou continuação do tratamento com base em dados de 16 estudos de coorte [12].
Há também uma componente psicológica: Para os doentes com psoríase que já foram submetidos a vários tratamentos biológicos diferentes, o conhecimento de uma possível perda de eficácia renovada pode sobrepor-se aos índices de satisfação dos doentes. O que se espera no futuro é um tratamento sistémico cuja eficácia se prolongue por dez anos ou mais. A evidência de resultados de tratamentos duradouros de estudos a longo prazo aproxima-nos deste objectivo.
Alvos moleculares de diferentes biólogos
A psoríase é uma doença inflamatória mediada por linfócitos T. O sistema imunitário é activado e as células T helper (Th) produzem várias citocinas na pele, que actuam sobre os queratinócitos epidérmicos e levam à proliferação excessiva e diferenciação anormal dos queratinócitos característicos da psoríase, bem como à infiltração com células inflamatórias [2]. As 17 células, que produzem vários mensageiros mediadores da inflamação, desempenham um papel fundamental [5]. Os factores desencadeantes externos causam interacção entre queratinócitos residentes na pele, linfócitos Th17 e células dendríticas dérmicas e macrófagos [6]. A activação de linfócitos Th17 induz a libertação de citocinas pró-inflamatórias como a IL-17A, IL-17F, IL-22 e o factor de necrose tumoral(TNF)-α. Estes, por sua vez, actuam sobre queratinócitos e contribuem para hiperplasia epidérmica, acantose e hiperparaceratose, bem como activação endotelial, levando a um maior recrutamento de células pró-inflamatórias, tais como granulócitos neutrófilos em tecido cutâneo [6].
A estimulação por factores desencadeantes como o stress, infecções ou tabagismo pode desencadear a produção de IL-6 e IL-23 em indivíduos geneticamente predispostos, o que promove a diferenciação das células T CD4+ produtoras de IL-17A (células Th17). Por outro lado, estão envolvidas células Th1, que produzem principalmente interferon-γ, o que entre outras coisas resulta na destruição de queratinócitos da camada basal [5].
Os diferentes pontos de ataque de vários representantes do grupo de biólogos são mostrados esquematicamente na Figura 1 [2]. Entretanto, estão disponíveis anticorpos anti-IL12/23 (ustekinumab), inibidores da IL17A (secukinumab, ixekizumab) e bloqueadores dos receptores da IL17 (brodalumab), bem como antagonistas da IL23 (risankizumab, guskumab, tildrakizumab), além de antagonistas da TNF-α (adalimumab, certolizumab, etanercept e infliximab) [6]. Enquanto o inibidor ustekinumab da IL12/IL23 se liga à subunidade p40 das citocinas IL12 e IL23, os novos inibidores da IL23 (risankizumab, guselkumab, tildrakizumab) inibem a subunidade p19 da IL23.
Literatura:
- Maul JT, et al: O sexo e a idade determinam significativamente as necessidades dos doentes e os objectivos de tratamento na psoríase – uma lição para a prática. J Eur Acad Dermatol Venereol 2019, 33(4): 700-708.
- Sator P: Estado da Arte: Terapia da Psoríase Vulgaris. Foco: Pele e reumatismo, FdR 01|2019, 16.04.2019
- Yawalkar N: Psoríase sem Sintomas – a Nova Esperança para os Doentes. Reunião Anual da SGDV, Basileia 20.09.2019.
- Egeberg A, Bryld LE, Skov L: Sobrevivência de secukinumab e ixekizumab para psoríase em placas moderada a grave. J Am Acad Dermatol 2019; 81(1): 173-178.
- Eyerich K: Psoríase – Para onde estamos a ir? Key Lecture 3, apresentação de slides, Prof. Dr. med. Kilian Eyerich, TU München, SGDV Reunião Anual, Basileia 20.09.2019.
- Wild J, Wegner J, Karbach S: Desde a pele ao sistema vascular – psoríase e risco cardiovascular. Cardiologia 2020; 14, 205-211.
- Bartlett HS, Million RP: Alvejando o caminho IL-17-T(H)17. Nat Rev Drug Discov 2015; 14(1): 11-12.
- Augustin M: S09/04 Differentiation factors in therapy decision-making, JDDG 2019, https://onlinelibrary.wiley.com/doi/10.1111/ddg.13793
- Kamata M, Tada Y : Eficácia e Segurança dos Biólogos para a Psoríase e Artrite Psoriática e o seu Impacto nas Comorbilidades: Uma Revisão da Literatura. Int J Mol Sci 2020; 21(5): 1690.
- Volc S, Ghoreschi K: Base fisiopatológica das terapias sistémicas na psoríase. JDDG 2016. DOI: 10.1111/ddg.13050, https://onlinelibrary.wiley.com/doi/pdf/10.1111/ddg.13050_g
- Mourad A, et al: Factores que prevêem a persistência de drogas biológicas na psoríase: uma revisão sistemática e uma meta-análise. Br J Dermatol 2019; 181: 450-458.
- Yiu ZZN: Sobrevivência às drogas adalimumab, ustekinumab e secukinumab em doentes com psoríase: um estudo de coorte prospectivo da Associação Britânica de Dermatologistas Biólogos e Imunomoduladores Registo (BADBIR). BJD 2020; 183(2): 294-302.
PRÁTICA DA DERMATOLOGIA 2020; 30(5): 30-32