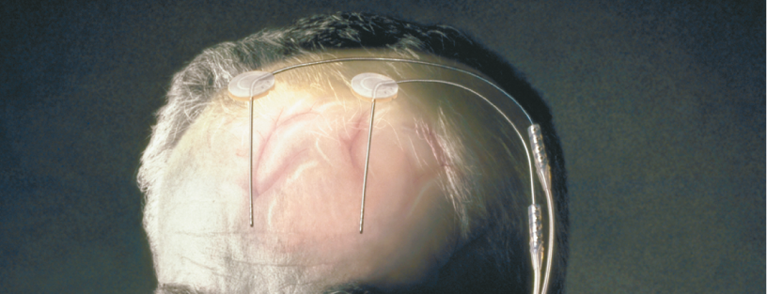
O tratamento com levodopa na doença de Prakinson leva frequentemente a flutuações motoras e discinesias. Para pacientes seleccionados em fases avançadas, a estimulação cerebral profunda, que funciona através da aplicação de impulsos de alta frequência em áreas específicas do cérebro, provou ser o padrão de ouro. As flutuações, em particular, podem ser bem tratadas desta forma, mas também sintomas não motores, tais como dor que responde à levodopatia. Em geral, a estimulação cerebral profunda, que só é oferecida por alguns centros na Suíça como parte da medicina altamente especializada, deve ser considerada para pacientes com DP que não podem ser tratados suficientemente bem com métodos de terapia medicamentosa, ou seja, para quem os sintomas motores ou a qualidade de vida não podem ser satisfatoriamente melhorados por terapias orais. A indicação deve ser verificada logo que ocorram as primeiras flutuações em vigor, à medida que a relação risco-recompensa piora à medida que a doença progride.
Juntamente com a doença de Alzheimer, a doença de Parkinson (ou: síndrome de Parkinson idiopática) é uma das doenças neurodegenerativas mais comuns, com a evolução demográfica e o facto associado de as pessoas estarem a envelhecer e a contribuir significativamente para o facto de a prevalência continuar a aumentar. A doença de Parkinson manifesta-se não só com sintomas motores, mas também com uma variedade de sintomas não motores.
O tratamento dos sintomas motores clássicos de bradicinesia, rigor e tremor baseia-se principalmente na substituição de substâncias que visam os receptores estribais de dopamina, levando a uma reconstituição parcial da função normal dos gânglios basais. No início da terapia, esta estratégia leva a um controlo muito bom dos sintomas na maioria dos pacientes com DP, embora o tremor – se presente – não responda à medicação dopaminérgica em todos os pacientes. A longo prazo, o tratamento com substâncias dopaminérgicas, mas especialmente com preparações de levodopa, leva frequentemente a flutuações motoras e discinesias. Isto leva a uma deterioração da independência e da qualidade de vida das pessoas afectadas.
Hoje em dia, há várias escaladas de tratamento possíveis para estes pacientes em fases avançadas, e a estimulação cerebral profunda estabeleceu-se agora como um excelente padrão de ouro baseado em evidências para pacientes cuidadosamente seleccionados (Tabelas 1 e 2).


Já em 1987 foi demonstrado que a modulação eléctrica de alta frequência da actividade neuronal no núcleo subthalâmico leva a uma melhoria reversível dos sintomas de Parkinson, o que foi confirmado nos primeiros estudos clínicos [1–3]. Entretanto, existem grandes estudos randomizados que testaram a eficácia da estimulação cerebral profunda contra o melhor tratamento medicamentoso [4, 5]. A eficácia está assim claramente comprovada, assim como a influência positiva na qualidade de vida, o que explica por que razão mais de 100.000 pacientes foram tratados com este método em todo o mundo até à data.
Função e efeito
A estimulação cerebral profunda funciona através da aplicação de impulsos de alta frequência em áreas cerebrais definidas, em que os eléctrodos são ligados ao estimulador real (“pacemaker cerebral”) por meio de cabos subcutâneos e modulam a função dos neurónios, as suas ligações e assim a transmissão do sinal nos gânglios basais na área alvo central correspondente (Fig. 1).
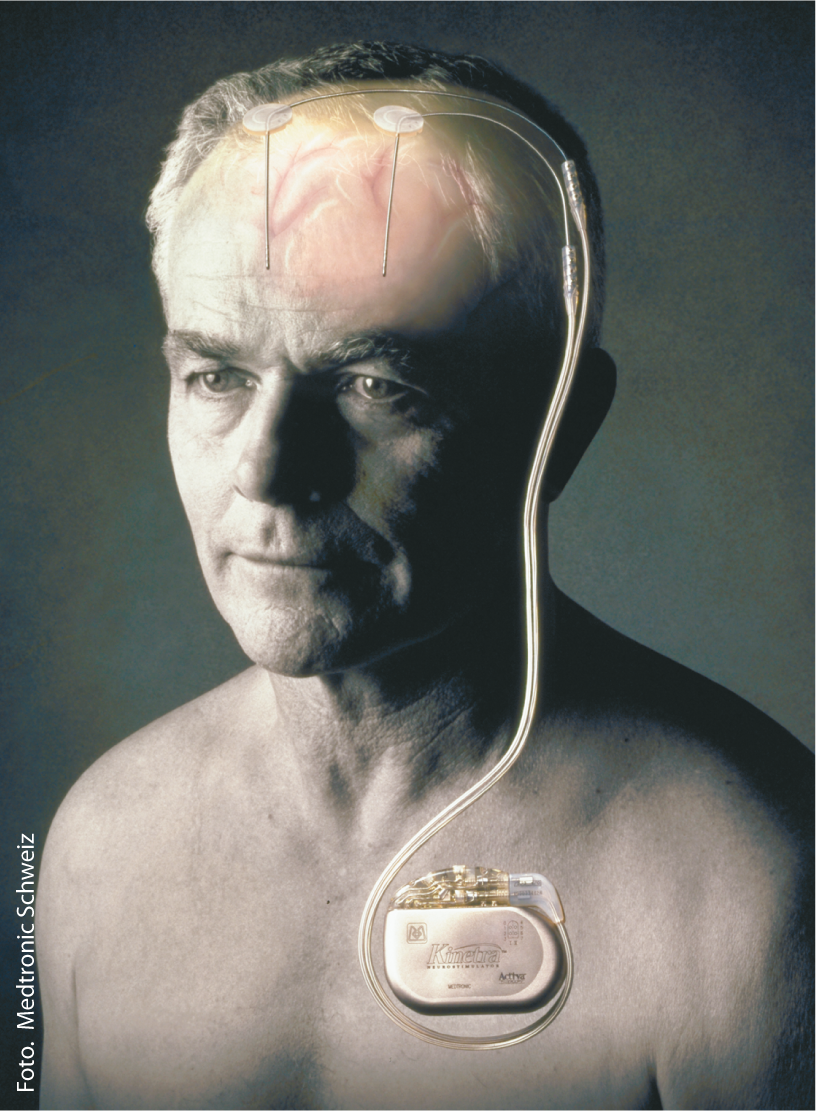
Fig. 1: Eléctrodos e estimulador
A terapia melhora tanto os sintomas motores como especialmente as flutuações: Os pacientes estão num bom estado motor durante mais tempo e menos hipocinéticos ou discinéticos [4, 5]. Em princípio, quanto melhor o rigor e a bradicinesia responderem à levodopa, maior será a eficácia da estimulação. O Tremor também responde, aqui também na ausência de resposta a medicamentos dopaminérgicos. Sintomas axiais tais como instabilidade postural ou disfunção postural, por outro lado, não respondem à medicação ou estimulação cerebral profunda. O efeito dura anos, embora seja possível uma decomposição parcial sob estimulação no globus pallidus. Com estimulação subthalâmica, a medicação pode ser reduzida no pós-operatório.
A estimulação cerebral profunda também tem efeitos terapêuticos sobre os sintomas não motores, especialmente sobre a dor que reage à levodopatia, que pode remeter sob estimulação subtalâmica [6]. Possivelmente devido à co-estimulação das partes límbicas do núcleo subthalâmico, pode ocorrer uma clarificação do estado de espírito, até um estado hipomaníaco.
A redução da dose diária de drogas em doentes estimulados subthalâmicos pode reduzir os efeitos secundários induzidos por drogas, tais como, em particular, distúrbios de controlo de impulsos ou sonolência diurna excessiva. A redução demasiado rápida dos medicamentos dopaminérgicos, por outro lado, pode levar à apatia e à depressão.
Efeitos secundários e complicações
Efeitos secundários tais como perturbações da marcha, disartria, hipomania, distúrbios oculomotores ou discinesia podem ocorrer dependendo do local e intensidade da estimulação e podem ser minimizados tanto quanto possível, por um lado, através de testes na sala de operações em pacientes acordados e, por outro lado, ajustando a estimulação nas primeiras semanas a meses após a operação, mas nem sempre podem ser evitados. Complicações específicas do dispositivo, tais como quebra de cabos ou dislocações ocorrem ocasionalmente, mas especialmente após traumatismos.
Os riscos cirúrgicos são pequenos, mas a hemorragia intracraniana e as infecções não podem ser completamente excluídas mesmo com a melhor preparação e execução possíveis. A duração da bateria é de 2-7 anos, dependendo da intensidade da estimulação, e a mudança da própria bateria é descomplicada.
Qual o ponto-alvo no cérebro?
O tema de discussão é a questão de qual é o ponto-alvo no cérebro mais eficaz e melhor tolerado para os doentes com Parkinson. Tanto o núcleo subthalâmico como o globus pallidus interno são regularmente utilizados como alvos, com a maioria dos peritos a interpretar o núcleo subthalâmico como a estrutura alvo mais eficaz, embora esta discussão não possa ser considerada fechada [7, 8]. Por outro lado, a estimulação no globus pallidus tem vantagens no que diz respeito à tolerância neuropsiquiátrica, razão pela qual o procedimento óptimo deve ser decidido separadamente para cada paciente. Outras possíveis áreas alvo estão actualmente a ser discutidas na literatura, mas não podem ser abordadas nesta breve panorâmica.
Hora do início da terapia
Até recentemente, as pessoas tinham tendência a esperar demasiado tempo antes de usar a estimulação cerebral profunda. Os pacientes eram frequentemente operados apenas quando os sintomas não-motores já tinham prejudicado maciçamente a qualidade de vida. Um estudo germano-francês recentemente publicado mostrou que a estimulação cerebral profunda é superior ao tratamento medicamentoso, mesmo no curso anterior da doença [9]. Neste estudo, a idade média dos pacientes foi de 52 anos e o curso médio da doença foi de sete anos e meio. Por analogia, a análise (não publicada) dos nossos próprios dados mostrou que os pacientes com o curso mais curto da doença responderam mais claramente não só em termos de qualidade de vida, mas também em termos de redução dos sintomas motores.
Literatura:
- Bergman H, Wichmann T, DeLong MR: Reversão do parkinsonismo experimental por lesões do núcleo subthalâmico. Ciência 1990; 249: 1436-1438.
- Benabid AL, et al: Efeitos agudos e a longo prazo da estimulação do núcleo subthalâmico na doença de Parkinson. Stereotact Funct Neurosurg 1994; 62: 76-84.
- Limousin P, et al: Efeito dos sinais e sintomas parkinsonianos da estimulação bilateral do núcleo subthalâmico. Lancet 1995; 345: 91-95.
- Deuschl G, et al: Um ensaio aleatório de estimulação cerebral profunda para a doença de Parkinson. N Engl J Med 2006; 355: 896-908.
- Weaver FM, et al: Bilateral deep brain stimulation vs best medical therapy for patients with advanced Parkinson disease: a randomized controlled trial. JAMA 2009; 301: 63-73.
- Sürücü O, et al: Estimulação subtalâmica profunda do cérebro versus a melhor terapia médica para a dor de reacção à l-dopa na doença de Parkinson. Dor 2013; 154: 1477-1479.
- Weaver FM, et al: Ensaio aleatório de estimulação cerebral profunda para a doença de Parkinson: resultados de trinta e seis meses. Neurologia 2012; 79: 55-65.
- Grupo de Estudo da Estimulação Profunda do Cérebro para a Doença de Parkinson: Estimulação Profunda do Cérebro do núcleo subthalâmico ou o pars internacional do globus pallidus na doença de Parkinson. N Engl J Med 2001; 345: 956-963.
- Schuepbach WM, et al: Neurostimulation for Parkinson’s disease with early motor complications. N Engl J Med 2013; 368: 610-622.
- Directrizes da Sociedade Alemã de Neurologia, www.dgn.org.
- Lhommée E, et al: Estimulação subtalâmica na doença de Parkinson: restabelecendo o equilíbrio de comportamentos motivados. Cérebro 2012; 135: 1463-1477.