Les approches translationnelles ont révolutionné les possibilités de traitement du psoriasis. Les nouvelles découvertes dans le domaine de l’immunopathologie épidermique constituent la base de l’optimisation de substances très efficaces. La nouvelle génération de thérapies systémiques donne d’excellents résultats et la commodité est également en constante amélioration. De nombreuses recherches sont actuellement en cours, comme le concept de “T-cells de la mémoire résidente” et la réduction des comorbidités cardiovasculaires comme effet secondaire du traitement.
Au cours des vingt dernières années, d’énormes progrès ont été réalisés dans le domaine de la compréhension physiopathologique des maladies dermatologiques. Cela s’est traduit par le développement d’applications cliniques de pointe. “Les produits biologiques et les petites molécules ont apporté une révolution dans la façon dont nous pouvons traiter les maladies inflammatoires graves”, a déclaré le professeur Kristian Reich de l’UKE de Hambourg (Allemagne) [1]. Dans son exposé, cet immunologiste confirmé et expert en psoriasis montre comment jeter un pont entre la recherche fondamentale en immunologie et les options thérapeutiques systémiques.
Crossstalk entre les cellules dendritiques et les cellules T
Le décryptage des bases moléculaires du psoriasis est en train d’évoluer rapidement [2]. Les modèles postulés il y a dix ans ont été améliorés et il est difficile de prévoir quelles connaissances seront dépassées dans cinq ans. D’après les connaissances actuelles, l’interaction des cellules dendritiques avec les lymphocytes T joue un rôle central dans le mécanisme pathologique du psoriasis et donc comme point de départ de thérapies efficaces. Les cellules dendritiques sont des composants de l’immunité innée et possèdent des récepteurs Toll-like.

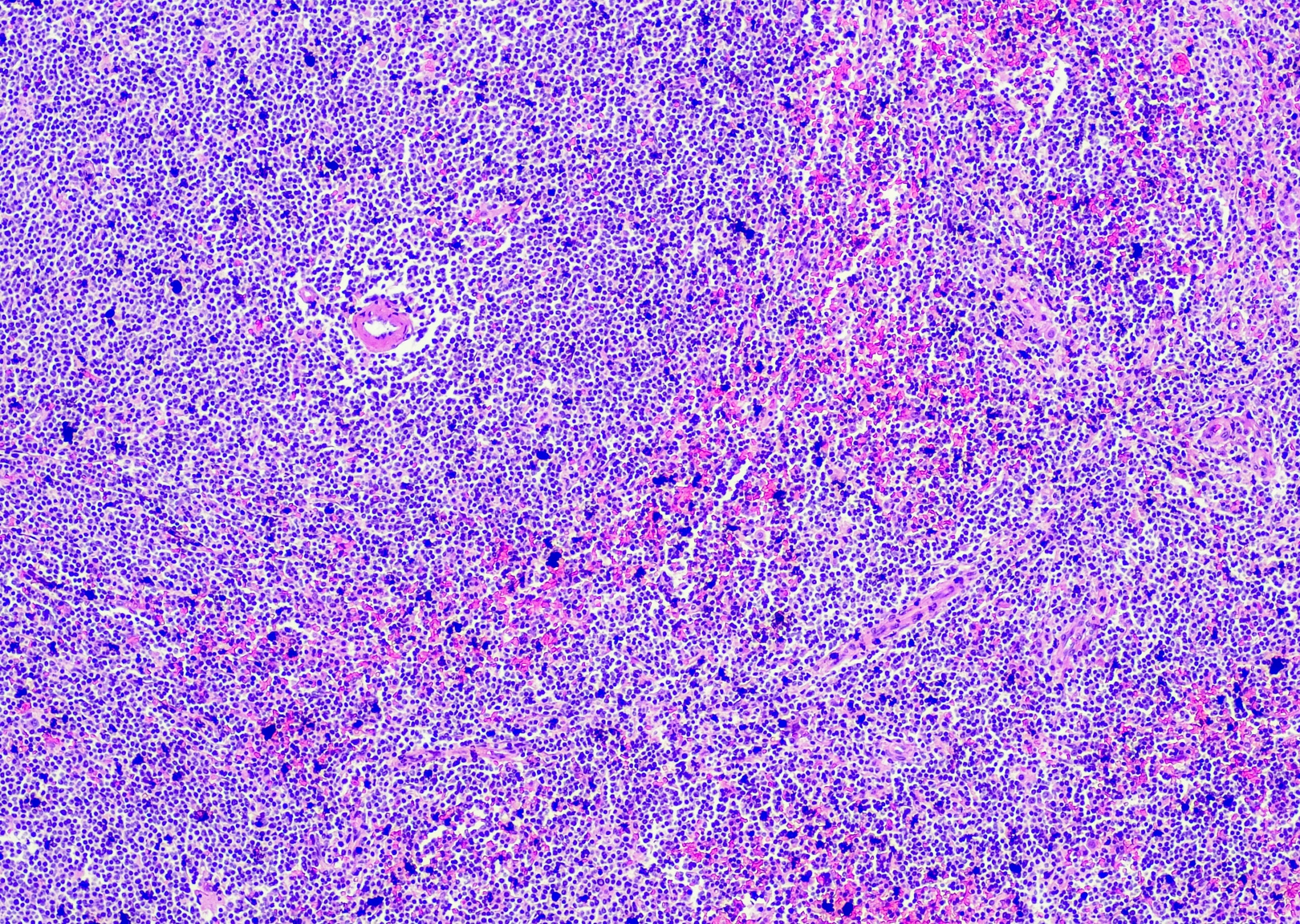
Les “Pathogen Molecular Associated Patterns” (PAMPS), qui sont liés par les récepteurs Toll-like des cellules dendritiques et des kératinocytes, font également partie de l’immunité innée. Une réponse antimicrobienne directe peut alors être déclenchée, accompagnée de la production de substances antibiotiques propres à la peau, comme la bêta-défensine-2 humaine. Les messagers attirent d’autres cellules immunitaires telles que les granulocytes neutrophiles ou les cellules de l’immunité spécifique (cellules CD) dans la peau. Les cellules T peuvent être activées par un contact avec les cellules dendritiques, ce qui a une signification immunopathologique (aperçu 1). Cela entraîne la production d’IL23, suivie de l’activation de Th17 et de la sécrétion d’IL17. Ce dernier est responsable de la pathologie kératinocytaire (Fig. 1) comme l’hyperkératose et la parakératose, mais aussi de la formation de nombreux neurotransmetteurs dans les kératinocytes. “Les granulocytes neutrophiles, en tant qu’élément de l’immunité innée, et les lymphocytes T, en tant que composante de l’immunité acquise, jouent un rôle très important dans les maladies inflammatoires”, résume l’orateur.

Les approches translationnelles optimisent les thérapies hautement efficaces
Les kératinocytes sont des cellules immunitaires très actives qui produisent des cytokines et qui sont au cœur des maladies inflammatoires de la peau. Il existe non seulement un mécanisme d’alimentation en amont sous la forme d’une activation de l’épiderme par le système immunitaire, mais également une réponse en aval, les kératinocytes maintenant l’activation du système immunitaire.
“Ce cercle vicieux est probablement responsable de la chronicité du psoriasis”, explique le professeur Reich [1]. Dans le groupe des cytokines IL17, les IL17A et IL17F sont essentielles pour le psoriasis. Bien qu’il y ait beaucoup plus d’IL17F dans la peau, l’IL17A est beaucoup plus puissante pour induire des réactions inflammatoires. Des études in vitro montrent qu’un amorçage des kératinocytes par le TNF est nécessaire pour une activation élevée des kératinocytes par l’IL17F. Les inhibiteurs de l’IL17, le sécukinumab et l’ixekizumab, bloquent l’IL17A. Le bimekizumab, un inhibiteur d’IL17A/F actuellement en cours d’évaluation clinique, a permis d’obtenir une rémission complète (PASI100) chez plus des deux tiers des patients après une période de 16 semaines dans l’étude de phase III BE READY, ce qui est un résultat très remarquable, explique le conférencier. Les évaluations actuelles des études de phase II indiquent également une efficacité élevée dans l’arthrite psoriasique. Il semble donc que l’inhibition supplémentaire de l’homodimère IL17F soit associée à une amélioration des taux de réponse, ce qui suggère que cette sous-unité joue un rôle inflammatoire supplémentaire. Une partie des cellules IL17 a toutefois une fonction physiologique importante. En cas de déficit génétique de l’IL17 dans le cadre d’un déficit immunitaire rare, des infections graves à Candida résistantes au traitement apparaissent, explique le conférencier. Cela explique pourquoi le traitement par les inhibiteurs de l’IL17 peut entraîner des infections à Candida comme effet secondaire [1].
Effets thérapeutiques durables grâce à l’élimination des “T-cells de la mémoire résidente
Dans l’étude IMMhance [3], un “retrait randomisé” d’un traitement par inhibiteur de l’IL23 (risankizumab) a été effectué. Il s’est avéré que plusieurs mois après l’arrêt du traitement de 28 semaines, la peau restait exempte d’apparence ou en grande partie exempte d’apparence, les effets du traitement étant pour ainsi dire préservés. Il s’agissait d’une période cinq fois plus longue que la demi-vie, ce qui signifie qu’après cette longue période, la substance avait disparu de l’organisme depuis longtemps après l’arrêt du traitement. Il s’agit d’un effet très surprenant qui s’explique probablement par les “T-cells de la mémoire résidente”, selon le professeur Reich. Il s’agit de cellules de l’épiderme qui jouent un rôle important dans la mémoire immunologique. Plus le psoriasis persiste, plus il est probable qu’un pool de cellules inflammatoires se forme dans la peau, formant une mémoire de l’inflammation.
Le traitement par inhibiteurs de l’IL23 élimine probablement cette mémoire de l’inflammation, c’est-à-dire le pool de “T-cells à mémoire résidente”, chez un sous-groupe de patients répondeurs. L’analyse des biopsies réalisées dans le cadre de l’étude ECLIPSE [4] a montré que le nombre de “T-cells de la mémoire résidente” était réduit après le traitement par guselkumab. Cliniquement, cela signifie qu’il y a probablement un sous-groupe de patients qui répondent au traitement et qui restent sous contrôle de la maladie avec une injection par an. Cela signifie qu’en dermatologie, il existe aussi une thérapie “Disease modifying”, explique le professeur Reich.
Les plaques d’athérosclérose comorbides sont réduites
Le psoriasis et l’arthrite psoriasique sont souvent accompagnés d’une comorbidité cardiovasculaire, qui entraîne également une augmentation de la mortalité. “Nous avons de plus en plus de preuves que nos thérapies très efficaces traitent également les comorbidités”, souligne le conférencier. Certaines études montrent que les plaques d’athérosclérose sont considérablement réduites sous traitement par des agents biologiques très efficaces [5]. Les effets bénéfiques sur les comorbidités cardiovasculaires sont l’un des arguments en faveur de l’utilisation précoce des médicaments biologiques au cours de la maladie. Une “rémission précoce” est très importante dans les maladies immunologiques, souligne le conférencier.
Résumé
- Les thérapies systémiques modernes hautement efficaces disponibles aujourd’hui, issues des groupes des produits biologiques et des petites molécules, reposent sur le décryptage des mécanismes immunopathologiques du psoriasis.
- Une proportion élevée de patients atteint le PASI-90 ou le PASI-100 et l’amélioration de la commodité est associée à des niveaux élevés de satisfaction des patients.
- Actuellement, l’accent est mis sur la question de l’efficacité à long terme. “Resident Memory T-cells” forment une sorte de mémoire de l’inflammation et sont des cibles potentielles d’un traitement modificateur de la maladie.
- Pour obtenir une “rémission précoce” et augmenter ainsi les chances d’une absence de lésions à long terme, il existe globalement de nombreux arguments en faveur d’une thérapie systémique hautement efficace mise en œuvre tôt dans l’évolution de la maladie.
- Des études récentes montrent qu’un traitement systémique anti-inflammatoire avec des produits biologiques de dernière génération entraîne également une réduction des comorbidités cardiovasculaires.
Source : SGDV 2020
Littérature :
- Reich K : Mise à jour sur le psoriasis. Prof. Kristian Reich, UKE Hambourg (D). SGDV 2020, livestream, 17.09.2020.
- Hawkes JE, et al : J Allergy Clin Immunol 2017 ; 140 : 645-653.
- Blauvelt A, et al : Efficacité et sécurité d’un traitement continu par risankizumab contre un traitement continu chez les patients atteints de psoriasis en plaques modéré à sévère. Un essai clinique randomisé de phase 3. JAMA Dermatol. 2020;156(6):649-658. doi:10.1001/jamadermatol.2020.0723
- Muñoz-Elías E, et al. : Impact différentiel du blocage de l’IL-23 vs IL-17 sur les cytokines sériques, l’expression des gènes et les sous-types de cellules immunitaires dans la peau psoriasique : Résultats de l’étude ECLIPSE. Abstract D3T01.1D. Congrès de l’EADV, 9-13 Octobre, 2019.
- Elnabawi YA, et al : Increasing evidence for a protective effect of anti-inflammatory therapy. Cardiovasc Res 2019 ; 115(4) : 721-728.
- Giang J, et al : Activation du complément dans les maladies inflammatoires de la peau. Frontiers in Immunology 2018 ; 9. DOI:10.3389/fimmu.2018.00639. ISSN 1664-3224.
DERMATOLOGIE PRAXIS 2020 ; 30(5) : 36-38 (publié le 9.10.20, ahead of print)