Les malformations congénitales se présentent sous un spectre clinique hétérogène. Ils peuvent être classés en fonction du type de vaisseau, de l’efficacité hémodynamique et du degré de développement embryologique. Le diagnostic de base repose sur l’anamnèse, l’état clinique, l’échographie duplex, l’IRM et les D-dimères. Un plan de traitement individuel et interdisciplinaire doit être établi en fonction de la sévérité de la maladie.
Les malformations vasculaires congénitales (malformations vasculaires congénitales [KVM], angiodysplasie) se présentent sous la forme d’un spectre clinique hétérogène. Il n’est pas rare que le cas individuel se caractérise par différentes combinaisons de ces malformations. Bien que les MCV ne fassent pas partie, par définition, des maladies rares de l’enfant et de l’adulte, il existe un manque de soins médicaux. Outre l’anamnèse et l’état clinique, l’examen de base comprend une échographie duplex, une imagerie par résonance magnétique et une détermination des D-dimères. Les traitements sont souvent longs et complexes et nécessitent un plan de traitement interdisciplinaire qui doit inclure des aspects diagnostiques, chirurgicaux, peu invasifs et psychosomatiques. Seuls quelques centres d’excellence dans le monde sont en mesure d’offrir l’interdisciplinarité nécessaire, non seulement en termes de traitement, mais aussi sur l’ensemble du spectre d’âge des patients. Souvent, les malades vivent une véritable odyssée de médecin en médecin. Non seulement de nombreux patients sont ainsi déstabilisés, mais ils sont parfois traumatisés à vie par des traitements inadéquats.
Malformations vasculaires congénitales
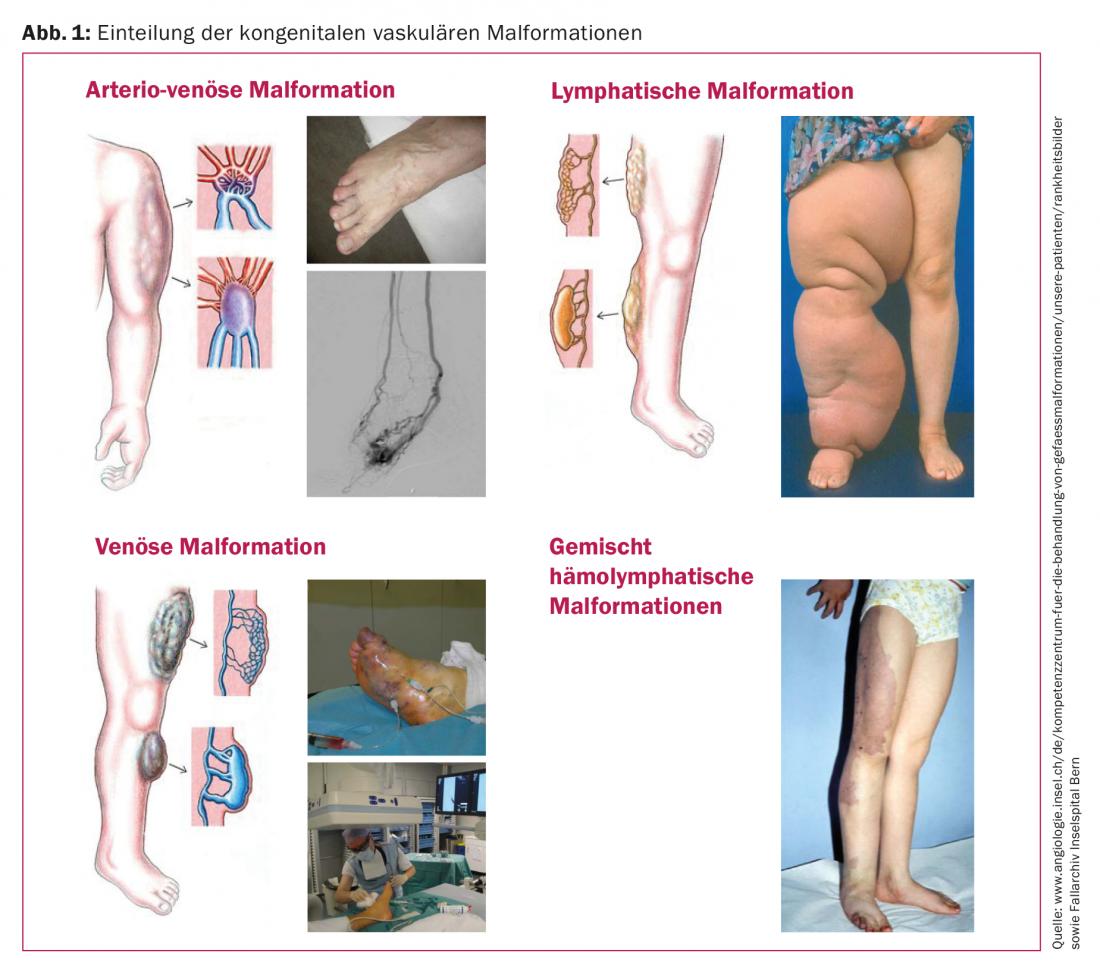
Une MVC est une malformation d’un ou plusieurs vaisseaux sanguins ou lymphatiques [1]. Il s’agit notamment des courts-circuits veino-artériels (AVM), des malformations veineuses (VM), des malformations lymphatiques (LM), des malformations capillaires (CM), souvent mixtes, et des tableaux syndromiques tels que le syndrome de Klippel-Trenaunay (Fig. 1).
La prévalence est d’environ 1,5% de la population, avec des variations selon la région géographique (tableau 1). On estime qu’il y a en Suisse environ 1000 à 1500 patients atteints de MCV nécessitant un traitement. Ce chiffre est multiplié par deux si l’on inclut les malformations vasculaires viscérales, spinales et intracrâniennes. Une source de données sur la prévalence existante en Suisse est la statistique CIM des hôpitaux (Office fédéral de la statistique). Ainsi, environ 700 cas de malformations potentielles sont recensés pour l’année 2010. Cela correspond à environ 88 cas par million d’habitants par an. Comme il faut supposer des erreurs de codage en raison de la sémantique diagnostique confuse, on peut probablement estimer à 100 le nombre de cas de traitement potentiels pour 1 million d’habitants.

Cause et complications
Les MVK sont attribuées à une malformation embryonnaire. Il reste des résidus du réseau capillaire embryonnaire qui peuvent entraîner des problèmes médicaux. La majorité absolue se développe à partir de segments de vaisseaux embryologiquement immatures (malformation vasculaire extratroncale), qui conservent après la naissance un potentiel de croissance similaire à celui des tumeurs. Dans le cas de ces MCV extratroncales embryologiquement immatures, une stimulation, par exemple une exposition aux hormones pendant la grossesse ou un traitement inadéquat, peut entraîner une progression incontrôlée. Outre le système vasculaire, le système squelettique est le plus souvent touché, avec une croissance disproportionnée. Les hémorragies chez les patients présentant une coagulopathie intravasculaire localisée associée, l’insuffisance cardiaque en cas de malformations artério-veineuses importantes, les états douloureux chroniques en cas de malformations veineuses étendues ainsi que les lymphœdèmes avec infections et fistules lymphatiques chroniques ne sont que quelques-unes des principales facettes des manifestations généralement complexes de la maladie.
Classification
siècle a été remplacée par une classification logique, qui a notamment contribué à optimiser les concepts de traitement. En raison de leur large présentation clinique et afin de planifier un traitement, les MCV sont généralement évalués dans un premier temps selon les critères suivants :
- correspondance anatomique du type de vaisseau (AM, VM, LM, CM) [2].
- Hémodynamique (high flow [AVM] ou low flow [VM, LM, CM]) [3]
- morphologique, attribution embryonnaire (MCT tronculaire ou extratronculaire) [4]
Une classification biologique des MCV a été publiée pour la première fois en 1982 par Mulliken et Glowacki. Suivie de la classification systématisante de Hambourg, qui a été largement intégrée dans la classification de l’International Society for the Study of Vascular Anomalies (ISSVA) [4]. Dans la classification de Hambourg, les MCV ont été différenciées pour la première fois en fonction du type de vaisseau anatomique et du degré de maturité embryologique, ce qui a permis de simplifier considérablement la sémantique (tab. 2).

La classification de l’ISSVA (International Society for the Study of Vascular Anomalies) (tab. 3) distingue, parmi les anomalies vasculaires, les malformations vasculaires congénitales et les hémangiomes [2,5]. Les hémangiomes sont considérés comme des tumeurs vasculaires précoces (“angiomes”) et font partie des anomalies vasculaires, mais doivent être différenciés des MCV en termes de pathophysiologie et de traitement.

Traitement
Parmi le grand nombre de MCV, les cas qui se distinguent sont ceux qui présentent un grave préjudice esthétique, fonctionnel ou une menace vitale pour la santé. Il n’existe pas de parcours de soins standardisés et fondés sur des preuves pour le traitement. Chaque patient doit être traité individuellement et un plan de traitement, qui s’étend souvent sur plusieurs années, doit être élaboré avec lui. La plupart du temps, des interventions par cathéter et/ou des opérations en plusieurs étapes sont nécessaires pour obtenir une amélioration pour le patient avec un risque acceptable d’effets secondaires.
La plupart des MCV ont des conséquences anatomiques, physiopathologiques et hémodynamiques qui, en l’absence de traitement, peuvent entraîner une atteinte importante de différents systèmes d’organes chez le jeune adulte. L’accent est mis sur les méthodes de traitement interventionnel peu invasives, en particulier l’embolisation endovasculaire et percutanée à l’alcool à 96% [6]. Lorsqu’elle est utilisée de manière ciblée, l’embolisation à l’alcool offre de bons résultats thérapeutiques durables avec un risque de complications acceptable. L’embolisation à l’alcool peut être complétée par l’utilisation de divers autres embolisats et coils. Il est essentiel de disposer d’une expertise suffisante en matière de traitement et d’effectuer des interventions échelonnées. Plus récemment, des résultats prometteurs ont été rapportés à plusieurs reprises dans le traitement des MCV complexes avec le sirolimus®, un inhibiteur de mTOR [7].
Les études prospectives ou randomisées font défaut. Diverses études de traitement centrées sur des systèmes d’organes spécifiques ont un niveau de preuve B et C. L’indication de traitement peut être résumée comme suit, indépendamment de l’organe concerné :
- Les MCV, qu’elles soient déjà symptomatiques ou asymptomatiques, doivent être éliminées par embolisation ou par chirurgie en raison de leur mauvais pronostic à court et moyen terme, si les chances de traitement sont jugées bonnes.
- Pour les MCV symptomatiques, l’indication d’un traitement est généralement acceptée. En règle générale, la priorité est aujourd’hui donnée aux procédures endovasculaires.
Le traitement des MCV extratroncales, qui représentent de loin la majorité des MCV, doit être laissé à des spécialistes expérimentés. Pour les MCV à haut débit, c’est-à-dire les malformations artério-veineuses, il existe pratiquement toujours une indication de traitement en raison de la progression liée au flux. Pour la classification clinique de Schobinger des malformations artério-veineuses, voir le tableau 4 [8].

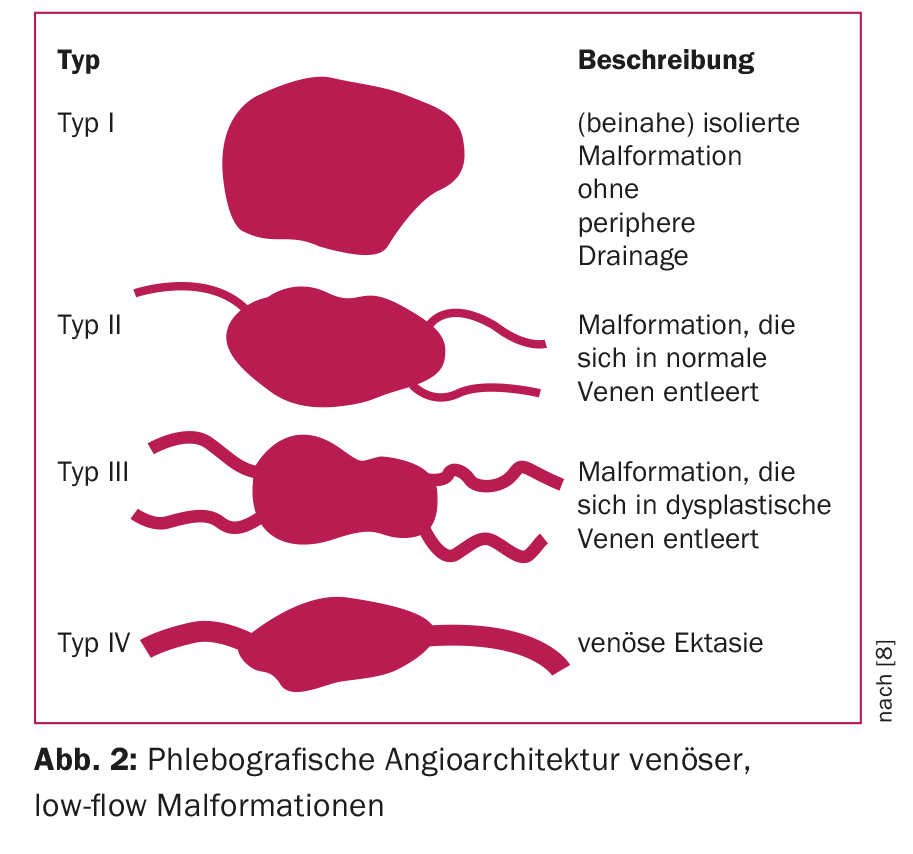
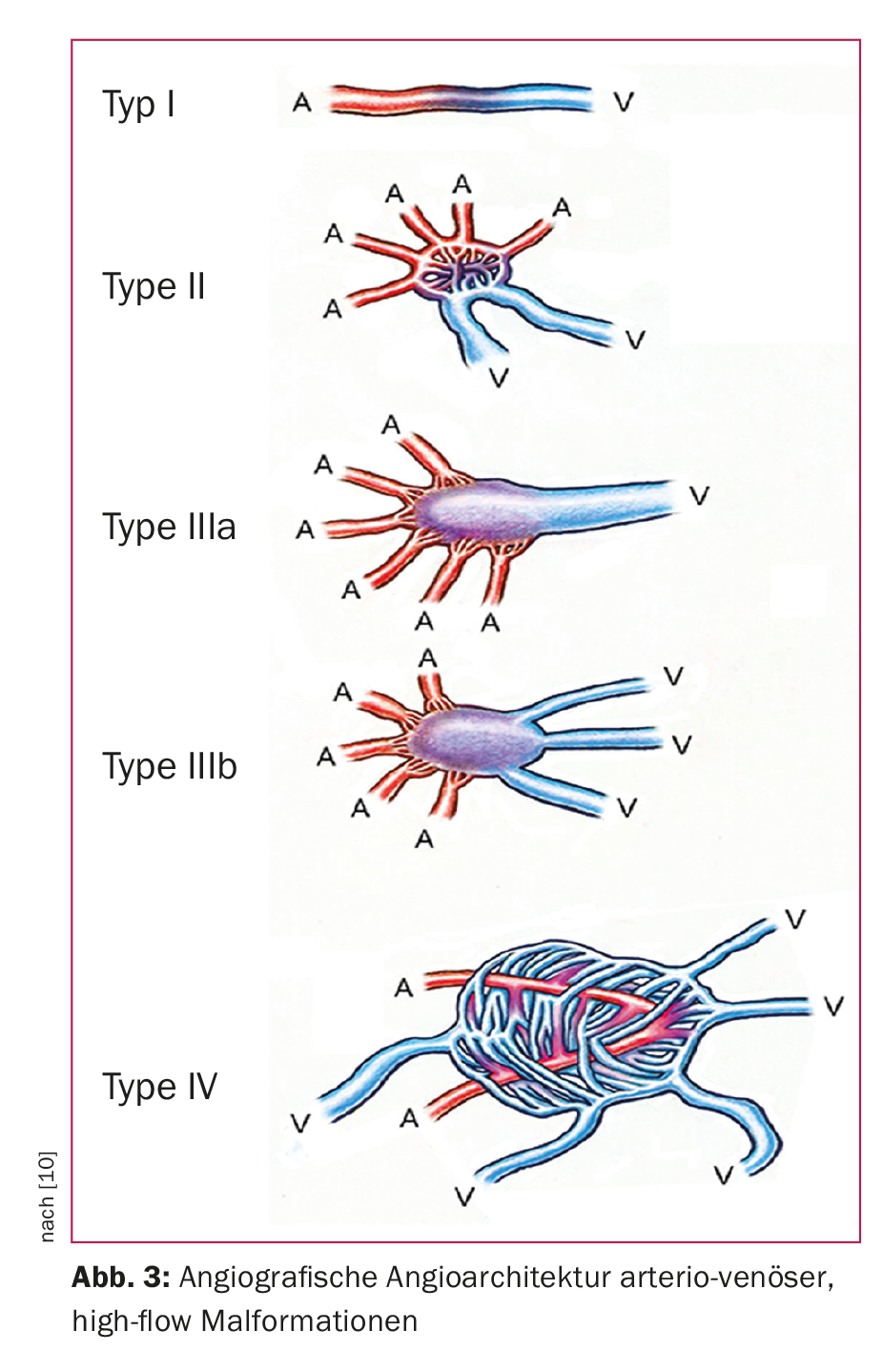
Une sous-classification supplémentaire en fonction de l’angiographie (angioarchitecture) s’est avérée utile pour la planification du traitement. Ainsi, les malformations veineuses à bas débit sont classées en quatre types (Fig. 2), une classification qui correspond à la fois au degré de difficulté et au risque de complications d’un traitement par embolisation [8]. Pour les malformations artério-veineuses à haut débit, la classification de Wayne-Yakes (Fig. 3) s’est imposée, qui est également étroitement liée à la technique spécifique à l’intervention et aux risques de complications [10].
Messages Take-Home
- En principe, la classification des malformations congénitales se fait selon les critères suivants : Type de vaisseau, efficacité hémodynamique, degré de développement embryologique (classification ISSVA)
- Le diagnostic de base repose sur l’anamnèse, l’état clinique, l’échographie duplex, l’imagerie par résonance magnétique et la détermination des D-dimères.
- Une stimulation, par exemple une exposition aux hormones pendant la grossesse ou un traitement inadéquat, peut entraîner une progression incontrôlée.
- Les manifestations sont multiples : système squelettique (croissance disproportionnée), thrombose/hémorragie (coagulopathie intravasculaire localisée), insuffisance cardiaque (malformations artério-veineuses), douleurs chroniques (malformations veineuses), lymphœdème avec infections et fistules lymphatiques chroniques.
- Un plan de traitement individuel et interdisciplinaire doit être établi. La majorité des méthodes de traitement interventionnel peu invasives sont utilisées et une approche en plusieurs étapes est recommandée pour minimiser les complications.
Littérature :
- Mulliken JB, Glowacki J : Hemangiomas and vascular malformations in infants and children : a classification based on endothelial characteristics. Plast Reconstr Surg 1982 ; 69 : 412-422.
- Wassef M, et al : Classification des anomalies vasculaires : Recommandations de la Société internationale pour l’étude des anomalies vasculaires. Pediatrics 2015 ; 136 : e203-214.
- Frey S, et al : Caractérisation hémodynamique des malformations artério-veineuses périphériques. Ann Biomed Eng 2017 ; 45 : 1449-1461.
- Lee BB, et al : Terminology and classification of congenital vascular malformations. Phlébologie 2007 ; 22 : 249-252.
- Dasgupta R, Fishman SJ : Classification ISSVA. Semin Pediatr Surg 2014 ; 23 : 158-161.
- Do YS, et al : Embolization à l’éthanol des malformations artérioveineuses : résultats intermédiaires. Radiologie 2005 ; 235 : 674-682.
- Triana P, et al : Le sirolimus dans le traitement des anomalies vasculaires. Eur J Pediatr Surg 2017 ; 27 : 86-90.
- Puig S, et al : Malformations vasculaires à bas débit chez les enfants : concepts actuels pour la classification, le diagnostic et le traitement. Eur J Radiol 2005 ; 53 : 35-45.
- Lee BB, et al : Document de consensus de l’Union internationale d’angiologie (IUA)-2013. Concept actuel sur la gestion de l’artériopathie veineuse. Int Angiol 2013 ; 32(1) : 9-36.
- Yakes W, Baumgartner I : Traitement interventionnel des malformations artério-veineuses. Chirurgie vasculaire 2014 ; 19 : 325-330.
CARDIOVASC 2017 ; 16(5) : 21-24