Le diagnostic à un stade précoce de la maladie est une condition préalable pour pouvoir utiliser la fenêtre d’opportunité d’un traitement modificateur de la maladie (DMARD) d’une efficacité optimale. Cela permet non seulement de réduire la douleur et l’inflammation, mais aussi de stopper la destruction progressive des articulations et les limitations fonctionnelles qui en découlent. L’activité de la maladie est objectivable au moyen du score DAS28.
Les taux d’incidence de la polyarthrite rhumatoïde (PR) sont les plus élevés dans les groupes d’âge de 55 à 75 ans [1,2]. Les caractéristiques de cette maladie rhumatismale inflammatoire sont une atteinte symétrique des articulations métacarpophalangiennes et interphalangiennes périphériques, avec une atteinte des articulations métatarsophalangiennes à un stade précoce. L’inflammation des articulations qui est à l’origine de la PR n’entraîne pas seulement des douleurs, des gonflements et des limitations fonctionnelles, elle peut aussi évoluer vers une destruction progressive des articulations si elle n’est pas traitée correctement [3]. L’inflammation est un facteur déterminant de l’évolution de la maladie, tant en ce qui concerne le maintien des fonctions physiques que les comorbidités et la mortalité [4].
“Windows of opportunity” à ne pas manquer
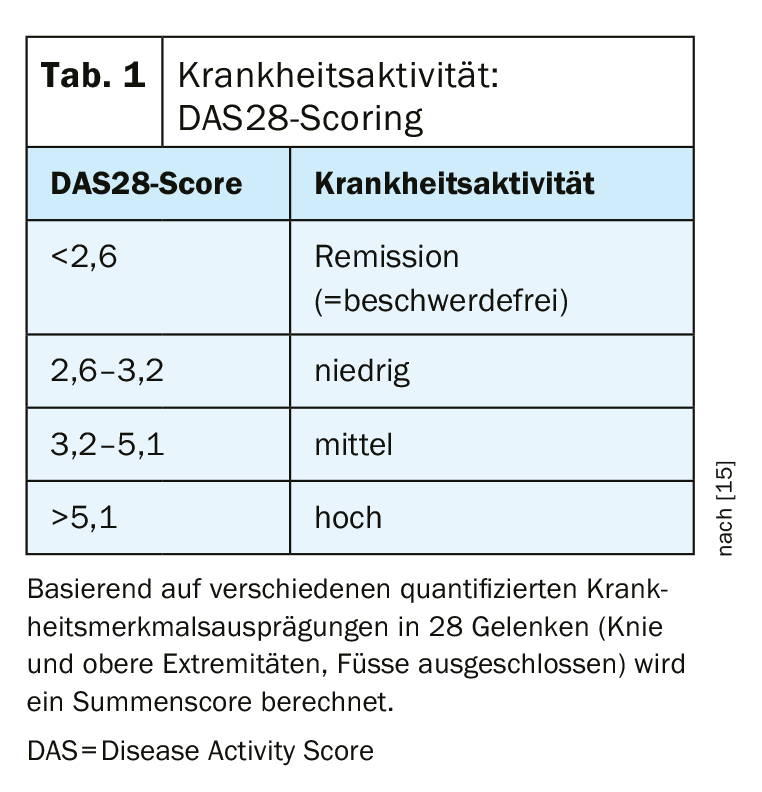
Il est empiriquement prouvé qu’un contrôle rapide de l’activité de la maladie par le début précoce d’un traitement avec des substances modifiant la maladie est décisif pour le pronostic ultérieur [3]. Les lignes directrices S3 mises à jour en 2019 proposent donc d’initier un traitement modificateur de la maladie (DMARD) en présence d’une PR dans les trois mois suivant le début des symptômes. Pour que le diagnostic soit posé au stade le plus précoce possible, il faut une prise en charge interdisciplinaire coordonnée qui garantisse que l’indication d’un traitement modificateur de la maladie soit examinée et que les personnes concernées soient adressées rapidement à un rhumatologue [4]. Les critères de classification ACR/EULAR visent à promouvoir l’introduction la plus précoce possible d’un traitement modificateur de la maladie et la prévention des conséquences irréversibles de la maladie [5,6,14] . Un score total est calculé sur la base de certains critères (tableau 1). Si le score est égal ou supérieur à 6, le diagnostic de polyarthrite rhumatoïde peut être posé. Les manifestations cliniques fréquentes de la PR sont la raideur matinale, la crépitation des tendons et l’atrophie interosseuse [7]. Les diagnostics de laboratoire incluent un facteur rhumatoïde et un ACPA positifs. La ligne directrice S3 actuelle propose un algorithme de diagnostic pour faciliter le diagnostic de la PR. Selon le guide S3, “l’arthrite se caractérise par un gonflement palpable, mou et “élastique” d’une articulation, dû à un épanchement et/ou à un épaississement inflammatoire de la muqueuse articulaire (synovite, synoviite), accompagné de douleurs et d’une raideur articulaire”. [3,4].
“Treat-to-target” au moyen de DMARDs
Pour objectiver le succès du traitement, il existe le système de scoring DAS28 (DAS=Disease Activity), qui sert à évaluer l’activité de la maladie selon certains paramètres cliniques et biologiques [15]. Un score global est calculé sur la base de la quantification des caractéristiques de la maladie dans 28 articulations (genoux et membres supérieurs, pieds exclus), une valeur de <2,6 étant considérée comme un critère de rémission (tab. 1). Il a été démontré à plusieurs reprises que les restrictions en matière de santé physique et mentale sont positivement corrélées à une activité élevée de la maladie [6,14]. Il est également apparu que le risque d’une opération de remplacement articulaire était associé à l’ampleur de l’activité de la maladie. De plus, il est apparu clairement qu’à long terme, le risque d’une opération de remplacement articulaire était positivement corrélé au niveau d’activité de la maladie. Disease-modifying anti-rheumatic drug (DMARD), peuvent ralentir la progression de la polyarthrite rhumatoïde en intervenant dans le processus de la maladie. Les médicaments antirhumatismaux modificateurs de la maladie comprennent, outre les produits biologiques et les biosimilaires (bDMARD) et les substances synthétiques conventionnelles (csDMARD), les représentants synthétiques ciblés (tsDMARDS), auxquels appartiennent les inhibiteurs de Januskinase. Contrairement aux produits biologiques qui inhibent certains messagers extracellulaires du système immunitaire, comme le TNF ou les interleukines, le principe d’action des inhibiteurs de Janus kinase (JAK-inhibiteurs) repose sur l’interruption de la transduction intracellulaire du signal des Janus kinases. Cela permet d’obtenir un effet anti-inflammatoire. En janvier 2020, Upadacitinib (Rinvoq®), un inhibiteur de JAK, a été autorisé pour la première fois en Suisse pour le traitement de la polyarthrite rhumatoïde [12,13].
Littérature :
- Zink A, Albrecht K : Zeitschrift fur Rheumatologie 2016;75 : 346-353.
- Hense S, et al : Zeitschrift fur Rheumatologie 2016;75 : 819-827.
- Schneider M, et al. : Guide interdisciplinaire sur la prise en charge de la polyarthrite rhumatoïde précoce. AWMF 060/002, S3, 4ème édition revue et augmentée, 2019
- Combe B, et al : Annales des maladies rhumatismales 2017 ; 76 : 948-959.
- Aletaha D, et al : Annals of the rheumatic diseases 2010;69 : 1580-1588.
- Radner H, et al : Remission in rheumatoid arthritis : benefit over low disease activity in patient-reported outcomes and costs. Arthritis Research & Therapy 2014 ; 16 : Article number : R56.
- Erni S : DD de rhumatologie, Dr. med. Stephan Erni, RehaClinic AG, Bad Zurzach, présentation de transparents, FOMF Bâle, 30.01.2020
- Lindqvist E, et al : Annals of the rheumatic diseases 2002 ; 61 : 1055-1059.
- van Zeben D, et al : The Journal of rheumatology 1994 ; 21 : 1620-1625.
- Wiles NJ, et al. Arthrite et rhumatisme 2001 ; 44 : 1033-1042.
- Fleischmann RM, et al : Annals Rheum Dis 2019 ; 78 : 1454-1462.
- Alten R, et al. : Patient Prefer Adherence 2016 ; 10 : 2217-2228.
- Information professionnelle actuelle RINVOQ® (upadacitinib). www.swissmedicinfo.ch
- Radner H, et al : Annales des maladies rhumatismales 2014 ; 73 : 114-123.
- Wells G, et al : Ann Rheum Dis 2009 ; 68(6) : 954-960.
PRATIQUE DU MÉDECIN DE FAMILLE 2020, 15(9) : 28