“Noi non siamo i nostri geni!”. Con questa affermazione, la Prof.ssa Katharina Domschke di Friburgo si è riferita all’importanza delle influenze ambientali – e di come queste influenzino la nostra salute mentale attraverso i processi epigenetici. Questo meccanismo è particolarmente importante nei disturbi d’ansia e potrebbe aprire nuove opzioni terapeutiche.
Un momento saliente del simposio per l’anniversario della Società Svizzera per l’Ansia e la Depressione (SGAD) di quest’anno è stata la conferenza della Prof. Dr. Dr. med. Katharina Domschke, Direttore medico del Dipartimento di Psichiatria e Psicoterapia dell’Ospedale Universitario di Friburgo (D). Ha richiamato l’attenzione sulla dimensione epigenetica dei disturbi d’ansia. Perché: i disturbi d’ansia, in particolare, sono ampiamente determinati dai nostri geni.
Frequenti, onerosi e costosi
I disturbi d’ansia sono i disturbi più comuni nella specialità neuropsichiatrica e colpiscono il 14% delle persone in Europa. Sono due volte più comuni della depressione unipolare o dell’insonnia, che sono i gruppi successivi più numerosi in termini di frequenza. A causa della loro elevata cronicità, i disturbi d’ansia sono anche malattie molto costose: Dopo i disturbi affettivi, la demenza e i disturbi psicotici, i disturbi d’ansia sono al quarto posto in termini di costi: . Questo onere per chi ne soffre, per i familiari e per il sistema sanitario è aggravato dal fatto che i disturbi d’ansia spesso portano a malattie psicologiche e/o somatiche. L’ansia predispone allo sviluppo di un successivo episodio depressivo o di un disturbo depressivo [1].
L’epigenetica come interprete tra ambiente e genetica
In questo contesto, la comprensione dell’eziologia è di grande importanza. I disturbi d’ansia sono poligenici, cioè sono formati da un gran numero di geni. Nel 30-60% di tutti i pazienti, esiste già una disposizione genetica per un disturbo d’ansia. Tuttavia, questa disposizione non determina direttamente la forma della malattia, ma attraverso una catena di fattori: il cambiamento dei sistemi di messaggeri nervosi e delle reti neuronali, determinate impostazioni psicofisiologiche (ad esempio, lasensibilità alla CO2 e le reazioni fisiologiche corrispondenti), nonché fattori ambientali come noxae, traumi ed eventi della prima infanzia o prenatali (Fig. 1).

L’epigenetica svolge il ruolo di mediatore tra i fattori ambientali e la genetica. Questo è molto importante per la psichiatria, che si basa sul modello di vulnerabilità allo stress. In questo modello, si presuppone la vulnerabilità individuale, che è determinata geneticamente e da fattori ambientali scatenanti. L’epigenetica assume la “funzione di interprete”, per così dire, tra il livello dei fattori ambientali e quello della genetica. L’epigenetica si riferisce ai processi biochimici che modificano la funzione di alcuni geni alterando il DNA e la sua struttura spaziale. “Questo contraddice il modello deterministico”, spiega il Prof. Domschke. “Siamo effettivamente co-determinati dai nostri geni, ma: non siamo i nostri geni!”. Quindi, i geni possono essere modificati tramite l’epigenetica – ma come?
Come l’epigenetica modella la nostra salute
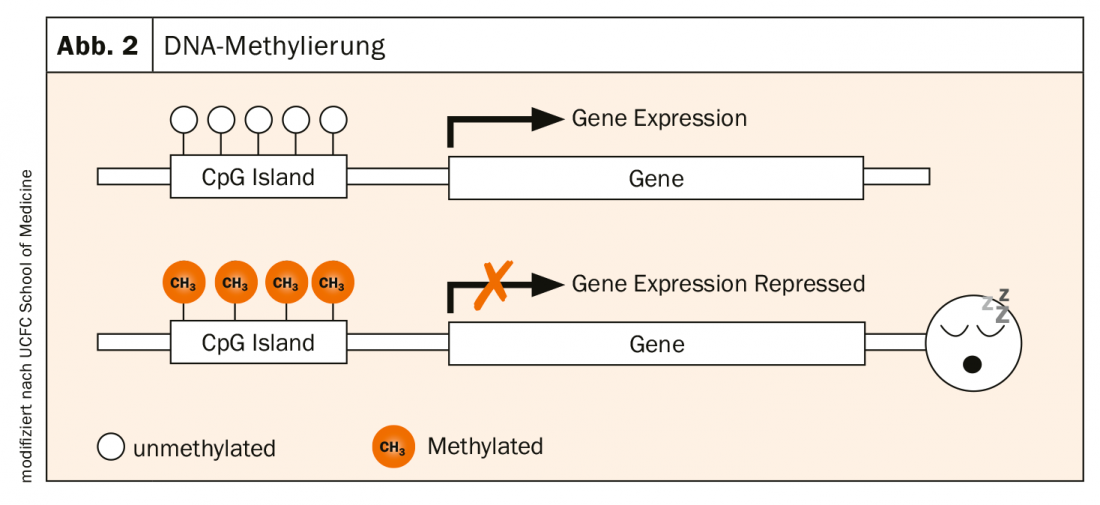
L’attività dei geni è determinata da vari processi. Uno molto centrale è la metilazione del DNA: l’attacco enzimatico di gruppi metilici (-CH3) alle basi nucleiche (isole CpG) del DNA. Si tratta di una modifica naturale causata dalle influenze ambientali. Le isole CpG si trovano spesso nella regione del promotore dei geni. Se questa regione non è metilata, il gene è attivo e può essere trascritto. Se è metilato, cioè se un gruppo CH3 vi si aggancia, il gene in questione non è più espresso. Si “addormenta” ( Fig. 2).
Un gene di rischio per i disturbi d’ansia e la depressione è la monoamino ossidasi A (MAOA). Si rompe la serotonina, la noradrenalina e la dopamina. L’enzima è ben noto nella pratica quotidiana attraverso l’uso degli inibitori MAO. In uno studio, il Prof. Domschke e colleghi sono riusciti a dimostrare che la metilazione di MAOA porta a una riduzione della funzione del gene – una scoperta significativa per la terapia delle malattie legate all’attività di questo gene [2]. Questa metilazione periferica influisce sui processi neuronali: Più bassa è la metilazione MAOA periferica, più alta è l’attività MAOA nel cervello. Ad esempio, il Prof. Domschke e colleghi hanno trovato una correlazione tra l’ipometilazione del promotore MAOA e il disturbo di panico [3]. Quindi, la metilazione della MAOA sembra essere un biomarcatore per l’ansia e la depressione.
Il Prof. Domschke e i suoi colleghi hanno esaminato se l’epigenetica può anche aiutare a prevedere la risposta alla terapia in uno studio di sei settimane. Hanno confrontato la risposta alla somministrazione di SSRI nei pazienti con alta metilazione MAOA rispetto ai pazienti con bassa metilazione MAOA. Questo ha dimostrato che i pazienti con un’elevata metilazione MAOA rispondono significativamente meglio agli SSRI. Sono ancora necessari ulteriori studi per comprendere meglio il meccanismo. Ma una conseguenza pratica di questa scoperta potrebbe essere che i pazienti che hanno comunque una bassa metilazione MAOA dovrebbero essere trattati con un SNRI o un inibitore MAOA piuttosto che con un SSRI.
Prevenire la malattia mentale attraverso l’epigenetica?
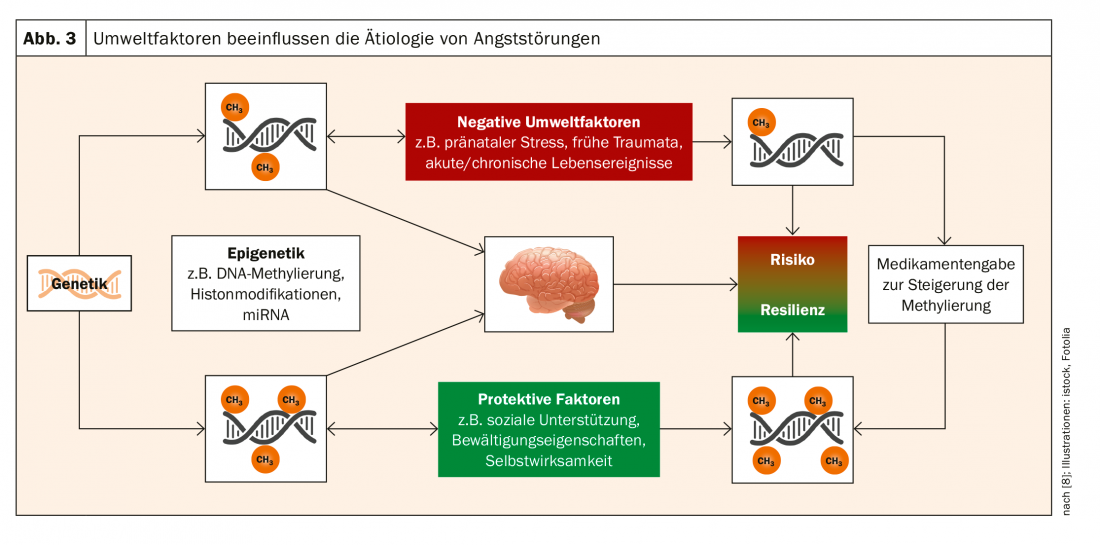
“L’aspetto entusiasmante non è solo questo meccanismo patogenetico-funzionale, ma anche il fatto che esiste una bidirezionalità”, sottolinea il Prof. Domschke. “La genetica è immutabile. Ma l’epigenetica, la metilazione, è dinamica. Risponde alle influenze ambientali”. Gli eventi di vita soggettivamente negativi contribuiscono alla riduzione della metilazione di MAOA. Il trauma può quindi portare a uno stato di rischio epigenetico. La buona notizia al contrario: gli eventi positivi sono correlati positivamente con la metilazione della MAOA. Le misure di promozione della resilienza possono contribuire alla profilassi della malattia mentale (Fig. 3).
In questo contesto, è stato esaminato anche il ruolo della psicoterapia. È stato dimostrato che la psicoterapia porta anche a una normalizzazione della metilazione e quindi a un miglioramento dei sintomi. A medio termine, la comprensione epigenetica dei meccanismi d’azione della psicoterapia potrebbe portare al suo aumento con farmaci che innalzano i pazienti con bassa metilazione MAOA al livello di quelli altamente metilati, dice il Prof. Domschke.
Nel complesso, secondo le conoscenze attuali, l’epigenetica rappresenta una possibilità di prevedere la risposta terapeutica individuale nel senso di una farmacoterapia personalizzata e – eventualmente – di spiegare i meccanismi d’azione della psicoterapia.
Cosa c’è di nuovo nella farmacoterapia?
Le fobie specifiche non vengono trattate con i farmaci, ma con la terapia cognitivo-comportamentale. Per la fobia sociale, il disturbo di panico e il disturbo d’ansia generalizzato, gli SSRI e gli SNRI sono il trattamento di scelta. Secondo uno studio pubblicato nel 2017, l’agomelatina sembra essere efficace non solo nella depressione, per la quale è approvata, ma anche nel trattamento del disturbo d’ansia generalizzato [4]. Off-label, l’agomelatina è quindi un buon integratore. La quetiapina, approvata per la schizofrenia e il disturbo bipolare, ha anche dimostrato un’efficacia significativa come monoterapia nel trattamento del disturbo d’ansia generalizzato [5]. L’estratto di olio di lavanda, indicato per i disturbi dell’ansia e dell’umore, ha dimostrato negli studi di essere efficace anche nel trattamento del disturbo d’ansia generalizzato [6].
Una parola sul pregabalin: sebbene questa sostanza abbia una chiara efficacia e una corrispondente evidenza Ia, è sospettata di creare dipendenza. Pertanto, attualmente esiste solo una raccomandazione B per il pregabalin. Lo stesso vale per il gabapentin. Tuttavia, va sottolineato che il rischio di queste sostanze è il più basso rispetto ad altri principi attivi con potenziale di dipendenza. Inoltre, la dipendenza da gabapentinoidi è regolarmente associata ad altre dipendenze, in particolare alla dipendenza da oppio e alla politossicomania. Ne consegue che né il pregabalin né il gabapentin dovrebbero essere dispensati dalla terapia – tranne che nel trattamento di persone già dipendenti. Invece, la somministrazione di benzodiazepine dovrebbe essere evitata. Gli (endo)cannabinoidi, ampiamente discussi, non hanno attualmente prove sufficienti, per cui non rappresentano nemmeno un’opzione terapeutica.
Fonte:10° Forum Svizzero per i Disturbi dell’Umore e dell’Ansia
Letteratura:
- Meier SM, et al: Depressione secondaria nei disturbi d’ansia gravi: uno studio di coorte basato sulla popolazione in Danimarca. Lancet Psychiatry 2015; 2(6): 515-523.
- Ziegler C, Domschke K: Firma epigenetica dei geni MAOA e MAOB nei disturbi mentali. J Neural Transm 2018; 125(11): 1581-1588.
- Domschke K, et al.: Ipometilazione del DNA del gene della monoamino ossidasi A – un fattore di rischio per il disturbo di panico? Int J Neuropsychopharmacol 2012; 15(9): 1217-1228.
- Stein DJ, et al: Efficacia e sicurezza dell’agomelatina (10 o 25 mg/die) in pazienti esterni non depressi con disturbo d’ansia generalizzato: uno studio di 12 settimane, in doppio cieco, controllato con placebo. Eur Neuropsychopharmacol 2017; 27(5): 526-537.
- Maneeton N, et al: La monoterapia con quetiapina nel trattamento acuto del disturbo d’ansia generalizzato: una revisione sistematica e una meta-analisi di studi controllati randomizzati. Drug Des Devel Ther 2016; 10: 259-276.
- Kasper S, et al: Il preparato all’olio di lavanda Silexan è efficace nel disturbo d’ansia generalizzato – un confronto randomizzato, in doppio cieco con placebo e paroxetina. Int J Neuropsychopharmacol 2014; 17(6): 859-869.
- Domschke K: Fattori predittivi nei disturbi d’ansia. Neurologist 2014; 85(10): 1263-1268.
- Ziegler C, Schiele M, Domschke K: Patho- und Therapieepigenetik psychische Erkrankungen. Neurologist 2018; 89: 10.1007/s00115-018-0625-y.
InFo NEUROLOGIA & PSICHIATRIA 2019; 17(3): 24-29.











