Secondo le attuali linee guida dell’ESH, la pressione arteriosa aortica è un importante biomarcatore del rischio cardiovascolare. Una determinazione non invasiva è possibile attraverso l’analisi delle onde del polso.
“La pressione arteriosa sistolica aortica determina il postcarico cardiaco”, ha spiegato il Prof. Dr. med. Martin Middeke, Facoltà di Medicina dell’Università Ludwig-Maximilians e Centro per l’Ipertensione di Monaco [1]. Il metodo di misurazione della pressione arteriosa mediante un bracciale superiore è stato considerato standard per molti decenni. Secondo le ultime scoperte, tuttavia, l’analisi dell’intera curva pressoria consente una diagnosi più precisa e permette una decisione terapeutica ottimale e personalizzata [2].
Base per la stratificazione del rischio e la terapia personalizzata
I valori estremi sono misurati nella determinazione auscultatoria della pressione arteriosa, in uso da molto tempo. Prima dell’invenzione di questo metodo, era comune la misurazione dell’intera curva di pressione. Lo stato attuale delle conoscenze suggerisce la rinnovata inclusione dell’intera curva pressoria nella diagnostica dell’ipertensione, ha detto il relatore. Le linee guida ESH 2013 elencano i seguenti due argomenti principali per la raccomandazione di misurare la pressione arteriosa centrale/aortica: 1) valore predittivo per gli eventi cardiovascolari, 2) Importanza per la terapia antipertensiva [3]. È ormai noto che la pressione arteriosa aortica è correlata al rischio cardiovascolare e la sua determinazione permette di regolare con precisione la terapia antipertensiva [4]. La misurazione tradizionale mediante un bracciale superiore del braccio è, tra l’altro, una base insufficiente per interpretare se un aumento del valore sistolico sia il risultato di un’amplificazione dell’onda del polso anterograda e quindi innocuo o il risultato di un aumento dell’onda riflessa con un aumento della rigidità vascolare; è necessaria l’analisi dell’intera curva pressoria [2].
Misurazione mediante analisi dell’onda di polso
Utilizzando la moderna analisi delle onde del polso, la pressione arteriosa aortica può essere determinata in modo non invasivo [1,5]. L’analisi delle onde di polso consente di misurare altri importanti biomarcatori, come la velocità delle onde di polso e l’indice di incremento (Fig. 1) per caratterizzare l’elasticità o la rigidità vascolare e il carico cardiaco [1,5]. Le onde del polso vengono registrate oscillometricamente e la pressione arteriosa aortica e altri parametri della rigidità dei vasi arteriosi (velocità delle onde del polso, indice di aumento) vengono calcolati tramite una funzione di trasferimento [2,6]. Secondo Baulman et al. la traduzione in un’età del vaso biologico è una forma adeguata di interpretazione dei risultati della misurazione [6]. Se, ad esempio, si misura una velocità dell’onda di polso di 10 m/s in una persona di 60 anni, dopo il confronto con i valori standard si otterrà un’età vascolare biologica di 70 anni. Questo paziente avrebbe quindi avuto un sistema vascolare arterioso significativamente pre-invecchiato e, inoltre, avrebbe già sviluppato un danno manifesto agli organi finali (≥10 m/s), secondo Baulman et al. [6]. L’esperienza ha dimostrato che la comunicazione dei risultati degli esami ai pazienti in questa forma chiara ha un effetto positivo sulla compliance.
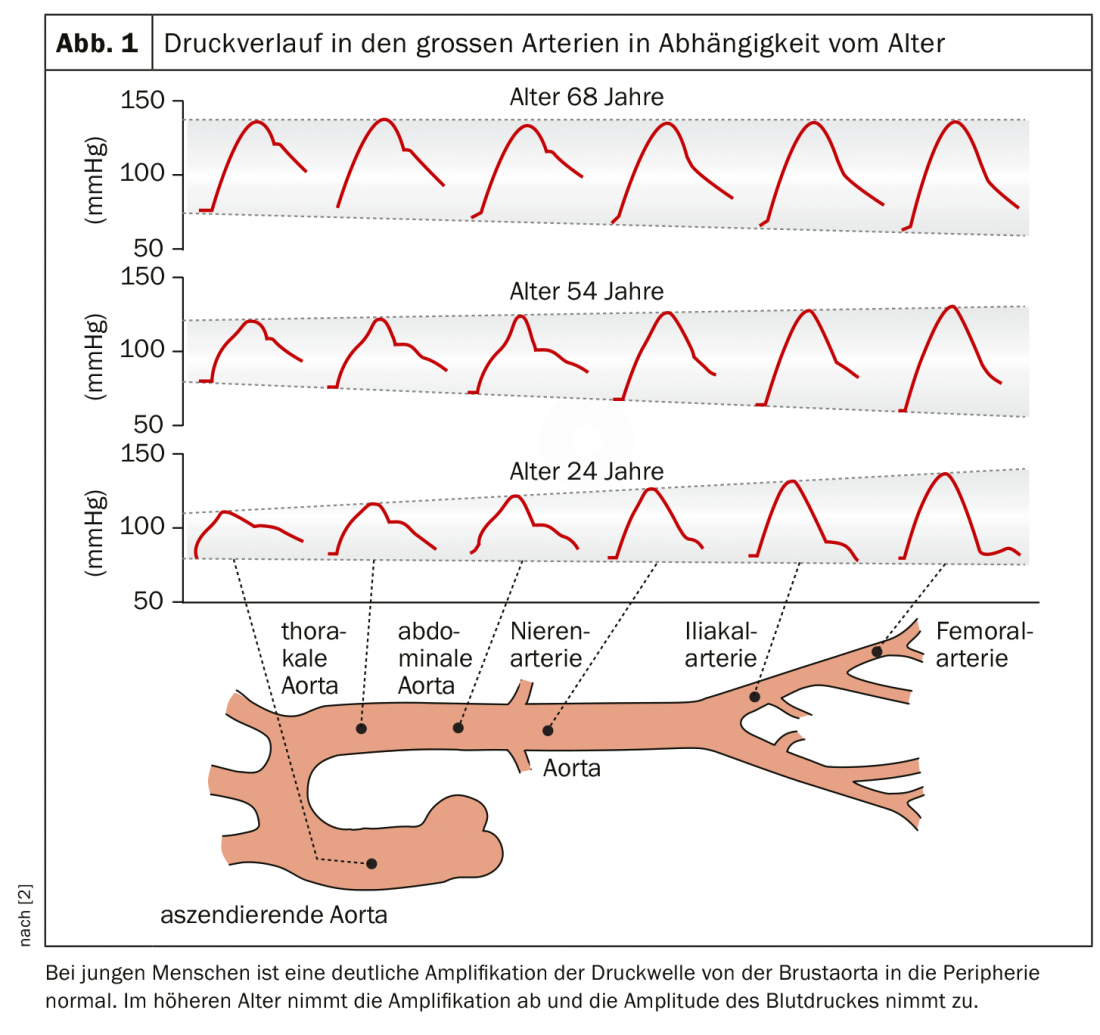
L’analisi delle onde del polso per la determinazione della pressione arteriosa aortica è adatta alla routine clinica, spiega il relatore [1]. L’amplificazione e l’aumento della pressione arteriosa sistolica possono essere differenziati in modo non invasivo solo con l’analisi delle onde del polso [2]. Si tratta di un metodo semplice per esaminare la funzione vascolare; l’onda del polso viene riflessa nella periferia, torna al cuore e l’onda di pressione riflessa si aggiunge all’onda che viaggia in senso anterogrado e aumenta la pressione sistolica [1].
Ipertensione sistolica giovanile e ipertensione aortica mascherata
Per ragioni fisiologiche, la pressione arteriosa brachiale è normalmente leggermente superiore alla pressione aortica centrale, anche se questa differenza può essere particolarmente grande in età giovane e con un’aorta molto elastica. Per diagnosticare l’ipertensione sistolica isolata giovanile benigna o per proteggere gli adolescenti e i giovani adulti colpiti da una terapia antipertensiva non necessaria, la determinazione aggiuntiva della pressione arteriosa aortica è indispensabile [1]. Di solito colpisce giovani uomini alti, snelli e atletici, i cui valori sistolici sono elevati nella misurazione brachiale convenzionale, ma la cui pressione arteriosa aortica risulta normale, a causa di una maggiore amplificazione della pressione sistolica dal centro alla periferia in vasi molto elastici e di un aumento del volume dell’ictus [7].
Con l’aumentare dell’età, l’amplificazione diminuisce e l’ampiezza (sistole meno diastole) aumenta, a causa dell’aumento della rigidità vascolare (Fig. 2) [2]. Che l’ipertensione sistolica isolata in età avanzata sorga sui generis come conseguenza dell’invecchiamento/rigidità vascolare fisiologica e non dall’ipertensione primaria in età più giovane è stato dimostrato in modo definitivo solo nel 2012 [1,8]. Vale a dire, l’aumento della pressione sistolica deriva dalla maggiore riflessione dell’onda di pressione nella rigidità arteriosa, con un aumento della pressione arteriosa sistolica.
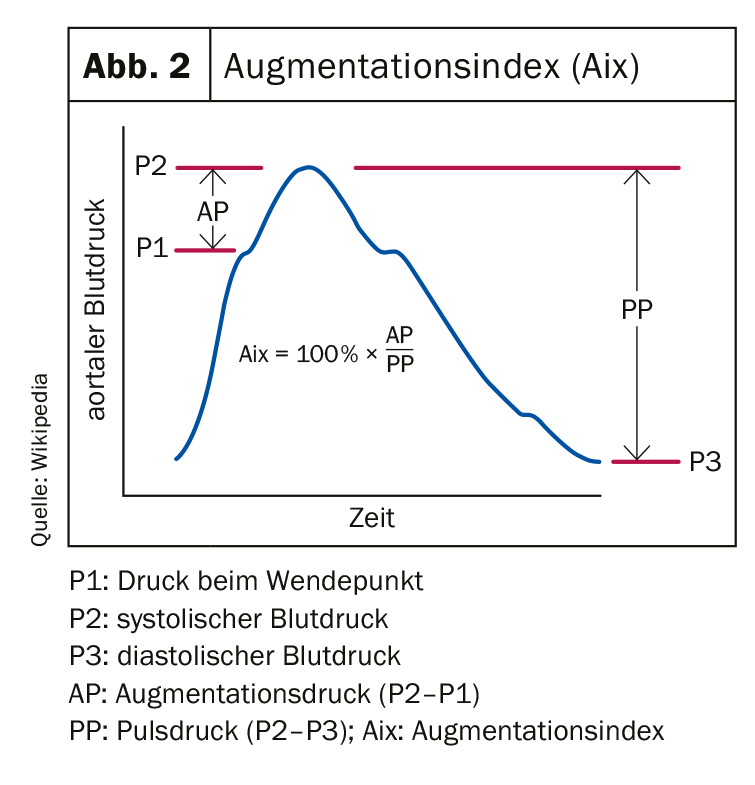
Inoltre, la cosiddetta ipertensione aortica mascherata non può essere esclusa in caso di valori di pressione arteriosa brachiale nell’intervallo normale. Nell’ipertensione aortica mascherata, la pressione sanguigna aortica è elevata, il che è associato a un aumento del rischio cardiovascolare o a un danno agli organi ipertesi già verificatosi [2].
Importanza per la terapia antipertensiva
Il fatto che gli eventi cardiovascolari e la mortalità siano significativamente correlati in modo positivo con la pressione sanguigna aortica è stato dimostrato, tra l’altro, in una meta-analisi [9,10]. Esistono anche prove empiriche che il trattamento antipertensivo ha effetti differenziali sulla pressione arteriosa brachiale rispetto alla pressione arteriosa aortica [11,12]. Per esempio, i dati dello studio “CAFE”, un sotto-studio di ASCOT [11,13], mostrano che i pazienti nella condizione atenelolo avevano una pressione arteriosa aortica di 4,3 mmHg superiore rispetto a quelli nella condizione amlodipina, nonostante valori identici di pressione arteriosa brachiale.
Nello studio ASCOT, i pazienti nella condizione di abbassamento della pressione sanguigna (BPLA) sono stati assegnati in modo casuale alla terapia antipertensiva con amlodipina o con atenololo. I pazienti con colesterolo totale di 6,5 mmol/L o inferiore e nessun trattamento precedente di riduzione dei lipidi sono stati assegnati in modo casuale ad atovarstatina o placebo (condizione di riduzione dei lipidi=LLA) [14].
Uno studio di follow-up dell’ASCOT pubblicato nel 2018 sugli effetti a lungo termine degli ipertesi sugli esiti cardiovascolari e sulla mortalità da Gupta et al. [14] ha mostrato che i pazienti che assumevano amlodipina (calcio antagonista) e atorvastatina (statina) avevano un minor numero di decessi cardiovascolari entro dieci anni dalla fine dello studio ASCOT rispetto alla condizione atenololo (amlodipina vs. condizione atenololo: HR aggiustato 0,71; 0,53-0,97; p=0,0305).

Il tasso di mortalità complessivo in relazione a tutti i partecipanti allo studio è stato del 38,3%. Tra i pazienti del gruppo BPLA, non c’era alcuna differenza nella mortalità per tutte le cause a seconda del trattamento (hazard ratio aggiustato [HR] 0,90; 95% CI 0,81-1,01; p=0,0776]). Nella condizione atenololo, il tasso di mortalità complessivo è stato dell’8,4% (1640 su 4275), e nella condizione amlodipina, il tasso di mortalità complessivo è stato del 38,1% (1642 su 4305). Di tutti i decessi, 1210 (36,9%) erano correlati al sistema cardiovascolare. Tra i 3975 pazienti del gruppo non-LLA, ci sono stati meno decessi correlati all’apparato cardiovascolare nei pazienti nella condizione amlodipina rispetto alla condizione atenololo (HR aggiustato 0,79; 0,67-0,93; p=0,0046). Nel gruppo LLA, c’è stato un numero significativamente inferiore di decessi correlati all’apparato cardiovascolare nei pazienti in condizione di statina rispetto al placebo (HR 0,85; 0,72-0,99; p=0,0395) [14]. Gli antagonisti della renina-angiotensina e/o i calcio antagonisti sono risultati avere un effetto più forte sulla pressione sanguigna aortica rispetto ai β-bloccanti e/o ai diuretici [15–17].
Letteratura:
- Middeke M: L’importanza della pressione arteriosa centrale per il trattamento dell’ipertensione. Prof. Dr. med. Martin Middeke, Facoltà di Medicina della Ludwig-Maximilians-Universität e Centro per l’Ipertensione di Monaco, presentazione alla Conferenza annuale della DGIM, 6. maggio 2019, Monaco.
- Middeke M: Pressione arteriosa aortica centrale: Middeke M: Pressione arteriosa aortica centrale: Dtsch Med Wochenschr 2017; 142: 1430-1436.
- Mancia G, et al: Linee guida ESH/ESC 2013 per la gestione dell’ipertensione arteriosa. J Hypertens 2013; 31: 1281-1357.
- Middeke M: [Davvero un’opzione nell’ipertensione? Sanguinare fino a quando la pressione sanguigna è normale]. [Article in German]. MMW Fortschr Med 2012; 154(14): 22-23.
- Baulmann J, et al.: Rigidità vascolare arteriosa e analisi delle onde di polso – documento di posizione su basi, metodologia, influenzabilità e interpretazione dei risultati. Dtsch Med Wochenschr 2010; 1: 4-14.
- Baulmann J, Herzberg C-P, Störk T: Il rinascimento della velocità dell’onda di polso, dell’aumento e della pressione aortica centrale come determinanti del rischio cardiovascolare. Med World 2013; 1: 30-33.
- O’Rourke MF, Adji A: Linee guida su linee guida: focus sull’ipertensione sistolica isolata nei giovani. J Hypertens 2013; 31: 649-654.
- Kaess BM, et al: Rigidità aortica, progressione della pressione sanguigna e ipertensione incidente. JAMA 2012; 308(9); 875-881.
- Vlachopoulos C, et al: Previsione di eventi cardiovascolari e mortalità per tutte le cause con l’emodinamica centrale: una revisione sistematica e una meta-analisi, Eur Heart J 2010; 31: 1865-1871.
- Roman MJ, et al: La pressione centrale è più fortemente correlata alla malattia vascolare e all’esito rispetto alla pressione brachiale: lo Strong Heart Study, Hypertension 2007; 50: 197-203.
- Williams B, et al: Impatto differenziale dei farmaci che abbassano la pressione sanguigna sulla pressione aortica centrale e sugli esiti clinici: risultati principali dello studio Conduit Artery Function Evaluation (CAFE). Circolazione 2006; 113: 1213-1225.
- Herbert A, et al. a nome della The Reference Values for Arterial Measurements Collaboration: Stabilire i valori di riferimento per la pressione arteriosa centrale e la sua amplificazione in una popolazione generale sana e in base ai fattori di rischio cardiovascolare. European Heart Journal 2014; 35(44): 3122-3133.
- Dahlof B, et al: Prevenzione degli eventi cardiovascolari con un regime anti-ipertensivo di antodipina con l’aggiunta di perindopril come richiesto rispetto all’atenololo con l’aggiunta di ben dioflumetiazide come richiesto, nell’Anglo-Scandinavian Cardiac Outcomes Trial Blood Pressure Lowering Arm (ASCOT – BPLA): uno studio multicentrico randomizzato controllato. Lancet 2005; 366: 895-906.
- Gupta A et al: Mortalità a lungo termine dopo il trattamento di abbassamento della pressione sanguigna e di abbassamento dei lipidi nei pazienti con ipertensione nello studio Anglo-Scandinavian Cardiac Outcomes Trial (ASCOT) Legacy: risultati di 16 anni di follow-up di uno studio fattoriale randomizzato. Lancet 2018; 392(10153):1127-1137. doi: 10.1016/S0140-6736(18)31776-8. Epub 2018 Aug 26.
- Wojciechowska W, et al: Valori di riferimento negli europei bianchi per l’onda del polso arterioso registrata mediante il dispositivo SphygmoCor. Hypertens Res 2006; 29: 475-483.
- McEniery CM, et al: Anglo-Cardiff Collaboration Trial ITl’impatto dei fattori di rischio cardiovascolare sulla rigidità aortica e sulla riflessione delle onde dipende dall’età: l’Anglo-Cardiff Collaborative Trial (ACCT III), Hypertension 2010; 56: 591-597.
- Janner JH, et al: Indice di aumento aortico: valori di riferimento in un’ampia popolazione non selezionata mediante il dispositivo SphygmoCor, Am J Hypertens 2010; 23: 180-185.
PRATICA GP 2019; 14(8): 35-36
CARDIOVASC 2019; 18(5): 21-22