I disturbi subclinici della tiroide sono comuni. Sebbene l’ipotiroidismo latente sia spesso trattato in modo eccessivo, il contrario può avere un impatto sulla mortalità.
I disturbi subclinici della tiroide sono comuni. Circa il 13% è affetto da ipertiroidismo subclinico [1], il 4-8% nella popolazione più giovane e il 15-18% nella popolazione più anziana da ipotiroidismo subclinico [2]. Quando e come si deve trattare?
I pazienti ipertiroidei più anziani spesso hanno pochi sintomi.
L’ipertiroidismo latente si ha quando il livello di TSH è inferiore al limite inferiore dell’intervallo di riferimento e il T4 e il T3 liberi sono normali. Dal punto di vista eziologico, si può fare una distinzione tra cause esogene (sovratrattamento ormonale) ed endogene; queste ultime includono, in particolare, la malattia di Graves, l’adenoma tossico e il gozzo nodulare tossico. Mentre la malattia di Graves si verifica prevalentemente nei pazienti più giovani (<65 anni) e nelle aree sature di iodio, l’adenoma tossico e il gozzo nodulare sono più comuni nelle aree povere di iodio e negli individui più anziani [3]. Secondo i dati dello studio SHIP, la distribuzione specifica per genere è approssimativamente comparabile (m=14%; f=20%) [1]. Osservando il tasso di invio dei pazienti ipertiroidei, si nota che un numero significativamente maggiore di pazienti giovani con “ipertiroidismo più grave” viene indirizzato a centri specializzati (fino al 70%), mentre i “casi più lievi” più anziani rimangono in carico ai medici di base (15-40% di invio). Tuttavia, il Prof. Dr. med. Matthias Schott, Direttore Medico di Endocrinologia presso l’Ospedale Universitario di Düsseldorf (D), avverte: “Soprattutto i pazienti più anziani hanno sintomi meno facili da cogliere: Perdita di appetito, stanchezza, debolezza e umore depresso”.
I pazienti con ipertiroidismo subclinico muoiono prima?
Sebbene i bassi livelli di TSH siano spesso transitori, l’ipertiroidismo latente non dovrebbe essere liquidato con leggerezza, in quanto può causare complicazioni cardiovascolari e scheletriche e avere un impatto sulla mortalità, tra le altre cose.
“Naturalmente, i pazienti con ipertiroidismo latente hanno un rischio maggiore di sviluppare la fibrillazione atriale”, afferma il Prof. Schott. Per esempio, due grandi studi prospettici hanno mostrato un rischio da due a tre volte maggiore nei pazienti anziani ipotiroidei di sviluppare la fibrillazione atriale. È stata riscontrata anche una maggiore incidenza di fibrillazione atriale nei pazienti anziani con TSH basso (0,1-0,5 mlU/l) [4]. Una meta-analisi con un follow-up di 8,8 anni ha anche mostrato un’incidenza significativamente più alta nei soggetti con ipertiroidismo subclinico e un rischio attribuibile del 41,5%. Non è stato possibile determinare le differenze rispetto al sesso, all’età o alle malattie cardiovascolari preesistenti [5].
Sebbene l’ictus sia considerato una potenziale complicanza della fibrillazione atriale nell’ipertiroidismo manifesto [6], questo non sembra essere il caso dell’ipertiroidismo subclinico.
Tuttavia, i dati raggruppati di una meta-analisi mostrano un’associazione tra ipertiroidismo subclinico e insufficienza cardiaca. Nel periodo di studio di 10,4 anni, l’HR per l’insufficienza cardiaca era significativamente maggiore nei pazienti con ipertiroidismo subclinico di tipo 2 (HR=1,94; 95% CI: 1,01-3,72) [7]. “I pazienti con ipertiroidismo latente hanno un rischio maggiore di insufficienza cardiaca, soprattutto con un livello di TSH di <0,1 mU/l”, conclude il Prof. Schott.
Esiste anche una correlazione con la malattia coronarica: i pazienti con ipertiroidismo latente hanno un rischio leggermente aumentato di eventi CHD (HR=1,21), aggiustato per l’età e il sesso, anche se non è stata riscontrata alcuna variazione significativa del rischio in base al grado di depressione del TSH [5].
Anche Blum e colleghi hanno confermato un aumento del rischio di osteoporosi nella loro meta-analisi con tredici studi prospettici [8].
Ultimo ma non meno importante: i pazienti con ipertiroidismo subclinico muoiono prima delle persone eutiroidee? Collet e colleghi hanno risposto a questa domanda in modo affermativo. La loro meta-analisi con un totale di dieci coorti di studio (n=52.674) ha mostrato solo un leggero, ma comunque significativo aumento della mortalità per tutte le cause [5]. Più anziani sono i pazienti con ipertiroidismo latente, maggiore è la probabilità di morire a causa di questo ipertiroidismo per eccesso di mortalità. Questo vale sia per gli uomini che per le donne [9]. Questa è stata anche la conclusione di un recente studio di coorte danese che ha coinvolto quasi 630.000 pazienti [10].
Quindi, l’indicazione per il trattamento dell’ipertiroidismo latente è data in linea di principio, riassume il Prof. Schott. La questione cruciale è come trattarli.
Quando il paziente ipertiroideo subclinico trae beneficio dal trattamento?
Fondamentalmente, le opzioni terapeutiche disponibili sono tre: farmaci, terapia con radioiodio e chirurgia.
Farmaci: mentre la terapia sintomatica viene applicata naturalmente in caso di ipertiroidismo da rilascio (eventualmente con l’uso di beta-bloccanti), il trattamento tireostatico viene applicato in caso di ipertiroidismo da formazione. Questo comporta principalmente la somministrazione di tiamazolo a basso dosaggio, carbimazolo o propiltiouracile. A causa della lunga emivita, una singola dose giornaliera è sufficiente per il tiamazolo e il carbimazolo. Le dosi più elevate devono essere somministrate due o tre volte al giorno (tab. 1). I controlli devono essere effettuati a intervalli di due settimane nella terapia iniziale e ogni sei-dieci settimane nella terapia continua.

Operazione: l ‘indicazione viene data se la ghiandola tiroidea è grande (>50 ml), sono presenti noduli multipli, soprattutto freddi, il paziente desidera una “cura” rapida o c’è evidenza di compressione dei tessuti molli in questo paziente.
Terapia con radioiodio: la terapia con radioiodio viene presa in considerazione nei casi di ghiandola tiroidea da normalmente grande a moderatamente ingrossata, nei casi di precedenti operazioni alla tiroide e di controindicazioni (relative) alla chirurgia. Non deve esserci alcun sospetto di carcinoma.
Il Prof. Schott riassume: “Se la soppressione del TSH è massima e il paziente ha >65 anni, si deve ricorrere alla terapia ablativa, di solito con l’aiuto della terapia con radioiodio, l’intervento chirurgico dipende dalle dimensioni della ghiandola tiroidea e dalla presenza di linfonodi. Nei pazienti più giovani, si deve considerare la terapia in base ai possibili sintomi e alle comorbidità”. Se è presente un lieve ipertiroidismo subclinico, il trattamento deve essere preso in considerazione nei pazienti >65 anni. I pazienti più giovani non traggono beneficio in questo caso (panoramica 1).

“Attenzione al calcolo dei numeri”.
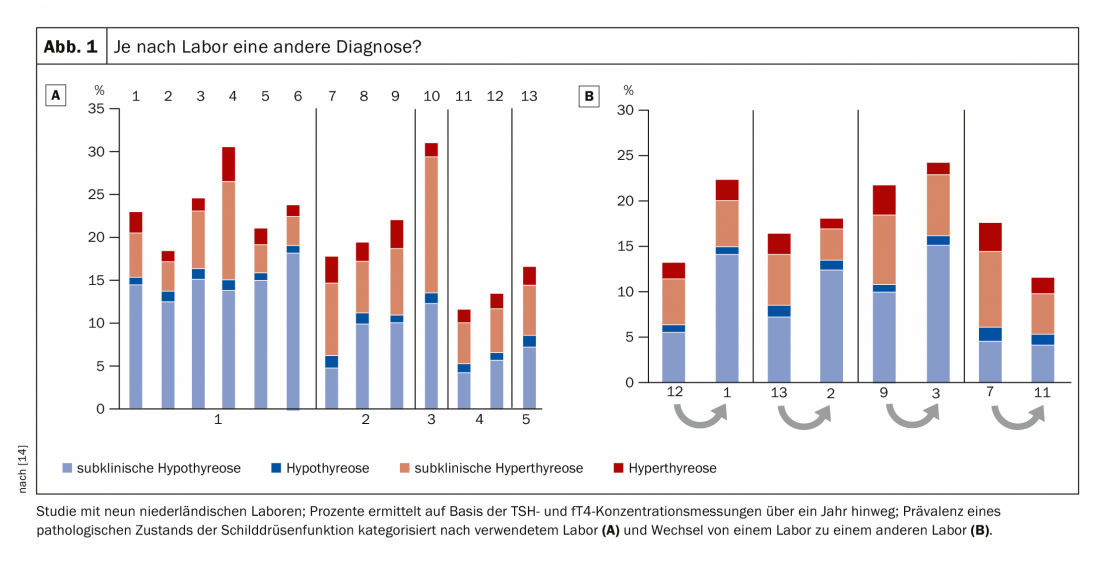
Mentre l’ipertiroidismo latente tende ad essere sottovalutato, c’è un eccesso di trattamento per quanto riguarda l’ipotiroidismo latente. Il problema inizia già con il valore standard del TSH. Per anni si è discusso sul limite standard superiore; il valore di cut-off di 2,5 mU/l si basa su un compromesso statistico [11]. E in effetti, il cut-off del TSH per il range di riferimento superiore della norma potrebbe essere tranquillamente spostato verso l’alto di 1-2 mU/l prima che diventi necessaria la misurazione dell’fT4 [12]. In uno studio sui centenari, è stato rilevato che hanno livelli di TSH molto più elevati, ma – almeno per quanto riguarda la funzione tiroidea – sono in perfetta salute [13]. Tuttavia, si tende a voler definire le concentrazioni assolute di TSH, che servono come strumento decisionale per decidere se un paziente debba essere osservato più da vicino o addirittura trattato. Il Prof. Dr. med. Jörg Bojunga, responsabile del reparto di Endocrinologia e Diabetologia e vicedirettore della Clinica dell’Ospedale Universitario di Francoforte a.M. (D), ha una visione critica al riguardo. Egli sottolinea non solo la costruzione del valore di cut-off 2,5 mU/l, ma anche le principali differenze nell’analisi di laboratorio. Per esempio, uno studio ha esaminato la questione della misura in cui la diagnosi di “ipotiroidismo subclinico” fosse una condizione “indotta dal laboratorio”, per così dire. Il risultato: a seconda del laboratorio, la valutazione dello stesso campione presentava una deviazione compresa tra il 6 e il 15%. Lo stesso è accaduto quando un campione è stato inviato dal laboratorio 1 al laboratorio 2 per un nuovo esame: Il solo cambiamento di laboratorio raddoppiava o dimezzava la possibilità che al paziente venisse diagnosticato un ipotiroidismo subclinico (Fig. 1) [14]. Questi risultati mettono in dubbio l’assoluta affidabilità delle misurazioni di TSH/fT4. “Si tratta di una questione puramente di laboratorio. Quindi, attenzione ai numeri!”, avverte il Prof. Bojunga. “Nel caso di risultati subclinici, è sempre necessario un controllo. In nessun caso si deve agire immediatamente!”, afferma l’esperta, con uno sguardo ai dati assicurativi, secondo i quali oltre il 90% riceve già una terapia dopo una singola misurazione del TSH.
99 casi su 100 trattati inutilmente
In molti casi, la funzione tiroidea si normalizza senza ulteriori interventi quando i livelli di TSH sono inizialmente elevati. Solo nell’1-5% dei pazienti l’ipotiroidismo subclinico si trasforma in ipotiroidismo manifesto [15]. “Questo significa che se si inizia la terapia dopo la prima misurazione, 99 casi su 100 saranno trattati inutilmente”, sottolinea il Prof. Bojunga; le persone anziane sono particolarmente a rischio di sovra-trattamento.
E il rischio di complicazioni? Mentre il rischio di malattie cardiovascolari aumenta chiaramente in presenza di ipertiroidismo subclinico, l’ipotiroidismo latente sembra avere un effetto generale positivo: La mortalità complessiva tende ad essere più bassa. Sebbene i dati sull’infarto miocardico siano borderline, il rischio di insufficienza cardiaca, ictus, CHD (e incidentalmente anche di cancro) non aumenta fino a un valore di TSH di 7 [16]. Questi due valori devono essere ricordati: “Tra il TSH 7 e il TSH 10, aumenta solo la CHD, l’insufficienza cardiaca non aumenta realmente, e solo a partire da un TSH di 10 succede qualcosa”. Conclusione divertita del relatore: “Ovviamente si vive più a lungo con l’ipotiroidismo subclinico”. Non è nemmeno possibile dimostrare un legame tra depressione e ipotiroidismo latente, né un’influenza sulla sessualità nelle donne.
Niente levotiroxina nei pazienti anziani con comorbidità!
La questione dell’utilità della levotiroxina per il trattamento dell’ipotiroidismo subclinico è stata analizzata in uno studio in doppio cieco, randomizzato, controllato con placebo e a gruppi paralleli, pubblicato nel 2017. Sono stati inclusi 737 pazienti (≥65 anni) con ipotiroidismo subclinico persistente. In un periodo di studio di un anno, non è stato riscontrato un beneficio significativo dal trattamento con levotiroxina [17]. Attenzione: nei pazienti con comorbidità, ad esempio la cardiopatia coronarica, la levotiroxina aumenta addirittura la mortalità [18]!
Tuttavia, la levotiroxina viene di solito prescritta a un TSH di 4,5-10. “In effetti, il rischio di assumere erroneamente ormoni tiroidei è aumentato nel corso degli anni. Due terzi di coloro che l’hanno ricevuta avevano più di sessant’anni – e sono quelli che non dovrebbero riceverla affatto”, spiega il Prof. Bojunga. Inoltre, questi pazienti avevano ricevuto una sola misurazione del TSH prima di iniziare la terapia.
Osservando il rapporto tra i sessi, sono soprattutto le donne in postmenopausa a ricevere ormoni tiroidei.
Quando trattare?
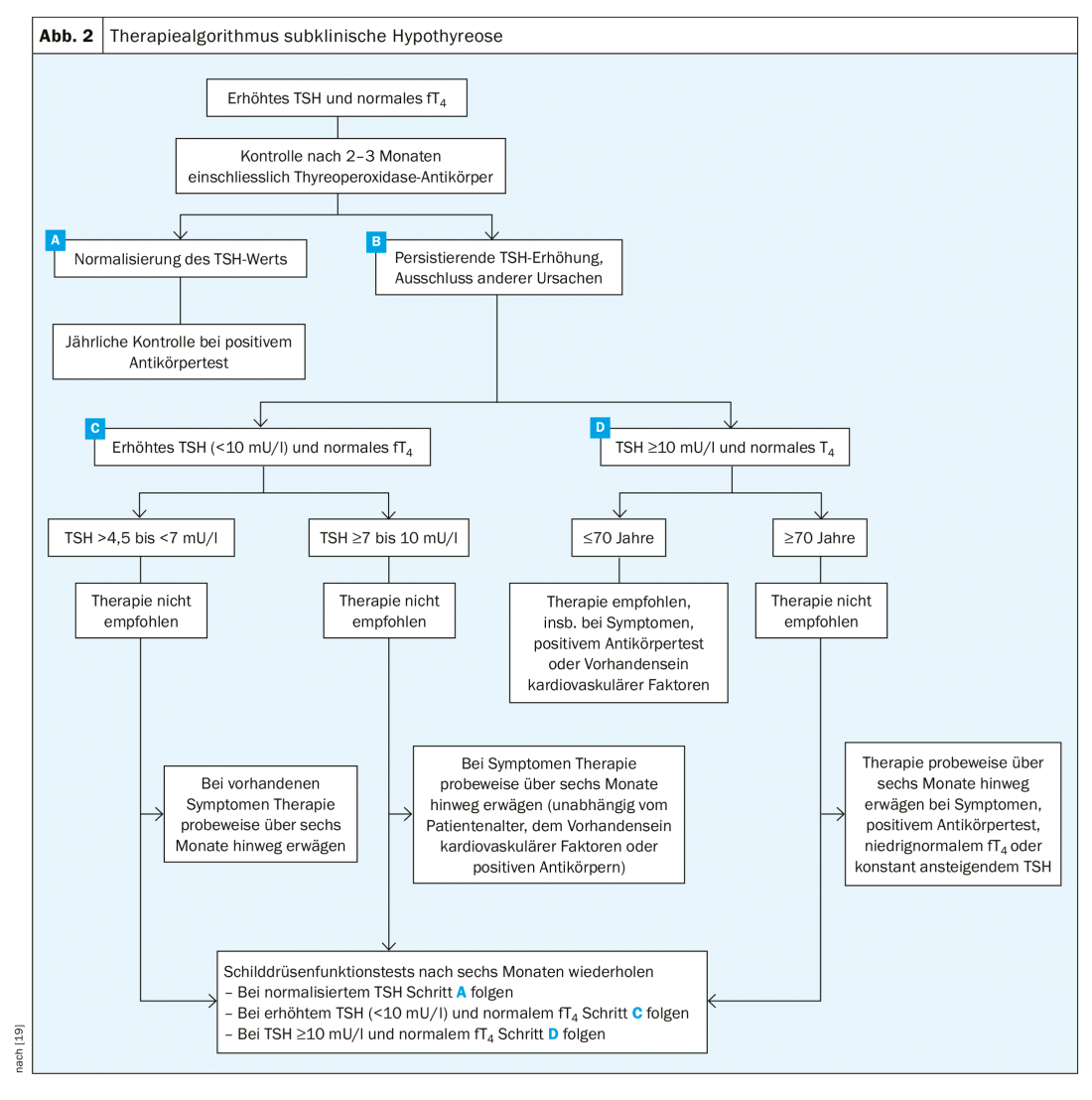
Se sono soddisfatti i criteri dell’ipotiroidismo subclinico (TSH elevato, fT4 normale), il paziente deve essere controllato dopo due o tre mesi. Nella maggior parte dei casi, il livello di TSH si normalizza. Se invece è ancora elevato durante il controllo, viene prima differenziato in <10 mU/l e ≥10 mU/l. Anche l’età del paziente è importante. Se il paziente ha meno di settant’anni e presenta un valore di TSH superiore a 10 mU/l, è indicata la somministrazione di levotiroxina. La terapia può essere presa in considerazione anche in caso di sintomi gravi, aumento dei livelli di TSH nel corso degli anni e presenza di anticorpi. Se si inizia una terapia, il decorso deve essere sempre monitorato. Se il valore del TSH va da >4,5 a <7 mU/l, di solito il trattamento non è indicato. Un tentativo di trattamento può essere fatto se il paziente presenta gravi sintomi di ipofunzione. Con valori di TSH ≥7 a <10 mU/l, si può prendere in considerazione la terapia prima (Fig. 2) . “Ma nel complesso”, conclude il Prof. Bojunga, “ci sono poche indicazioni. Le persone sono diventate più caute e, soprattutto in corrispondenza dei valori soglia, sono più propense a controllare”.
Letteratura:
- Völzke H, et al: La prevalenza di disturbi tiroidei non diagnosticati in un’area precedentemente carente di iodio. Tiroide 2003; 13(8) :803-810.
- Villar HC, et al: Sostituzione dell’ormone tiroideo per l’ipotiroidismo subclinico. Database Cochrane di revisioni sistematiche 2007: CD003419.
- Biondi B, et al: Le linee guida 2015 dell’Associazione Europea della Tiroide sulla diagnosi e il trattamento dell’ipertiroidismo endogeno subclinico. Eur Thyroid J 2015; 4: 149-163.
- Cappola AR, et al: Stato della tiroide, rischio cardiovascolare e mortalità negli anziani. JAMA 2006; 295(9): 1033-1041.
- Collet TH, et al: Ipertiroidismo subclinico e rischio di malattia coronarica e mortalità. Arch Intern Med 2012; 172(10): 799-809.
- Biondi B: Meccanismi in endocrinologia: insufficienza cardiaca e disfunzione tiroidea. Eur J Endocrinol 2012; 167(5): 609-618.
- Gencer B, et al.: Disfunzione tiroidea subclinica e rischio di eventi di insufficienza cardiaca: un’analisi dei dati dei singoli partecipanti di 6 coorti prospettiche. Circolazione. 2012; 126(9): 1040-1049.
- Blum MR, et al: Disfunzione tiroidea subclinica e rischio di frattura: una meta-analisi. JAMA 2015; 313(20): 2055-2065.
- Haentjens P, et al.: Disfunzione tiroidea subclinica e mortalità: una stima dell’eccesso relativo e assoluto di mortalità per tutte le cause basata su dati time-to-event di studi di coorte. Eur J Endocrinol 2008; 159(3): 329-341.
- Selmer C, et al: Disfunzione tiroidea subclinica e manifesta e rischio di mortalità per tutte le cause ed eventi cardiovascolari: un ampio studio di popolazione. J Clin Endocrinol Metab 2014; 99(7): 2372-2382.
- Surks MI, Goswami G, Daniels GH: L’intervallo di riferimento della tireotropina dovrebbe rimanere invariato. J Clin Endocrinol Metab 2005; 90: 5489-5496.
- Henze M, et al: Razionalizzare i test di funzionalità tiroidea: quali sono i cutoff del TSH ottimali per il test della T4 libera? J Clin Endocrinol Metab 2017; 102: 4235-4241.
- Atzmon G, et al.: L’estrema longevità è associata ad un aumento della tireotropina nel siero. J Clin Endocrinol Metab 2009; 94(4): 1251-1254.
- Coene KLM, et al: Ipotiroidismo subclinico: una condizione “indotta in laboratorio”? Europ J Endocrinol 2015; 173: 499-505.
- Cooper DS, Biondi B: Malattia tiroidea subclinica. Lancet. 2012; 379(9821): 1142-1154.
- Floriani C, et al: Disfunzione tiroidea subclinica e malattie cardiovascolari: aggiornamento 2016. Europ Heart J 2017; 39: 503-507.
- Stott DJ, et al: Terapia con ormoni tiroidei per gli adulti anziani con ipotiroidismo subclinico. N Engl J Med 2017; 376: 2534-2544.
- Nygaard Einfeldt M, et al.: Esito a lungo termine nei pazienti con insufficienza cardiaca trattati con levotiroxina: Uno studio osservazionale di coorte a livello nazionale. J Clin Endocrinol Metab 2019; 104: 1725-1734.
- Peeters RP: Ipotiroidismo subclinico. N Engl J Med 2017; 376: 2556-2565.
PRATICA GP 2019; 14(8): 22-25