Il carcinoma dell’endometrio è il sesto tumore più comune nelle donne in tutto il mondo e ha una prognosi sfavorevole, soprattutto in termini di risultati a lungo termine. Il tempo di sopravvivenza globale mediano è inferiore a tre anni. Una gestione efficace della terapia è particolarmente indicata per le pazienti con carcinoma endometriale primario avanzato o ricorrente. Ora i risultati dello studio alimentano la speranza di un nuovo trattamento combinato.
Il carcinoma endometriale (EC) è un tumore maligno dell’utero che origina dallo strato mucoso interno dell’utero. La malattia colpisce prevalentemente le donne in post-menopausa, con un picco di età compreso tra 65 e 85 anni. Il menarca precoce, la menopausa tardiva, la bassa parità o la sindrome dell’ovaio policistico sono descritti come fattori di rischio endogeni. I fattori di rischio esogeni includono la sola terapia estrogenica sostitutiva non ciclica, la terapia con tamoxifene e la radioterapia precedente. L’EC di solito coinvolge gli adenocarcinomi del rivestimento uterino. Gli adenocarcinomi sierosi e a cellule chiare o i carcinomi a cellule squamose si verificano solo raramente. Viene fatta una distinzione tra il carcinoma di tipo I estrogeno-dipendente e il carcinoma di tipo II estrogeno-indipendente. Tuttavia, anche i marcatori immunoistochimici e molecolari stanno giocando un ruolo sempre più importante.
La tipizzazione molecolare consente una terapia più precisa
La sottotipizzazione molecolare consente una stratificazione del rischio personalizzata e una scelta più precisa della terapia. Nell’ambito del progetto The Cancer Genome Atlas (TCGA), sono stati identificati quattro sottotipi molecolari di EC utilizzando il sequenziamento di nuova generazione (NGS):
- POLE: gene mutato della polimerasi epsilon (POLE), funzione di correzione compromessa durante la replicazione del DNA, fenotipo ultramutato.
- MSI-H/dMMR: riparazione di mismatch carente (dMMR) a causa di mutazioni, elevata instabilità microsatellitare (MSI-H), fenotipo ipermutato
- Numero di copie elevato/TP53abn: numero elevato di alterazioni somatiche del numero di copie, soprattutto mutazioni TP53 (TP53 anormale).
- Numero di copie basso/NSMP: varie mutazioni, nessun profilo molecolare specifico (NSMP)
Partendo da questa base, negli ultimi anni sono state sviluppate sostanze mirate (ad esempio Dostarlimab, Lenvatinib). I tumori MSI-H rappresentano il 25-30% dei carcinomi endometriali. La maggiore espressione del recettore della morte cellulare programmata 1 (PD-1) e dei suoi ligandi (PD-L1 e PD-L2) e l’elevato carico di mutazioni tumorali associato ai tumori dMMR-MSI-H li rendono potenzialmente suscettibili alle terapie anti-PD-1 e anti-PD-L1.
EC primario avanzato o ricorrente
Carboplatino più paclitaxel è la chemioterapia standard per il trattamento di prima linea dell’EC primario avanzato o ricorrente. Tuttavia, i risultati a lungo termine non sono ancora soddisfacenti. Prima dell’approvazione degli agenti mirati, non esistevano strategie di trattamento efficaci per i pazienti che avevano fallito la chemioterapia a base di platino. Dostarlimab è un inibitore del checkpoint immunitario attivo che ha come target il recettore PD-1. Sulla base dei risultati dello studio GARNET, il farmaco è stato approvato per il carcinoma endometriale avanzato o ricorrente dMMR-MSI-H. I ricercatori sono ora andati oltre: la chemioterapia citotossica può avere effetti immunomodulatori, come l’interruzione dei percorsi di segnalazione immunosoppressivi e un aumento della risposta citotossica delle cellule T. Era quindi ragionevole supporre che la combinazione di chemioterapia e immunoterapia potesse avere un effetto sinergico nel microambiente tumorale. Lo studio ENGOT-EN-6-NSGO/GOG-3031/RUBY ha quindi analizzato l’efficacia e la sicurezza di dostarlimab in combinazione con carboplatino e paclitaxel rispetto al placebo più carboplatino e paclitaxel nei pazienti con EC primario avanzato o ricorrente.
Nello studio di Fase III, multicentrico e in doppio cieco, 494 pazienti (118 dei quali con dMMR-MSI-H-EC) sono stati randomizzati in uno schema 1:1 e hanno ricevuto 500 mg di dostarlimab o placebo per via endovenosa in combinazione con carboplatino e paclitaxel ogni tre settimane per i primi sei cicli, seguiti da 1000 mg di dostarlimab o placebo per via endovenosa ogni sei settimane per un massimo di tre anni o fino alla progressione della malattia, all’interruzione del trattamento a causa di effetti tossici, al ritiro del paziente, alla decisione dello sperimentatore di ritirare il paziente o alla morte. Gli endpoint primari erano la sopravvivenza libera da progressione nei pazienti con dMMR-MSI-H-EC primario avanzato o ricorrente e nella popolazione complessiva, nonché la sopravvivenza globale nella popolazione complessiva. Gli endpoint secondari comprendevano la sopravvivenza libera da progressione determinata da una revisione centrale indipendente e in cieco, la risposta obiettiva, il controllo della malattia, la durata della risposta, il tempo alla seconda progressione della malattia, gli esiti riferiti dal paziente e le analisi di farmacocinetica e immunogenicità.
Sopravvivenza libera da progressione prolungata
Il tasso di sopravvivenza globale dopo 24 mesi è stato del 71,3% con dostarlimab e del 56,0% con il placebo. Nella popolazione dMMR-MSI-H, la sopravvivenza libera da progressione stimata era del 61,4% nel gruppo siero e del 15,7% nel gruppo placebo. Nella popolazione totale, era del 36,1% contro il 18,1%. Gli eventi avversi più comuni sono stati nausea (53,9% contro 45,9%), alopecia (53,5% e 50,0%) e affaticamento (51,9% e 54,5%). È stato quindi dimostrato che i pazienti con EC primario avanzato o ricorrente traggono un beneficio significativo dalla combinazione di dostarlimab, carboplatino e paclitaxel in termini di minor rischio di progressione della malattia.
Ulteriori letture:
- Mirza MR, Chase DM, Slomovitz BM, et al.: Dostarlimab for Primary Advanced or Recurrent Endometrial Cancer. N Engl J Med 2023; 388: 2145–2158.
- www.leitlinienprogramm-onkologie.de/fileadmin/user_upload/LL_Endometriumkarzinom_Langversion_3.01_.pdf (ultimo accesso 05.01.2024)
- www.gelbe-liste.de/krankheiten/endometriumkarzinom (ultimo accesso 05.01.2024)
- www.krebsgesellschaft.de/onko-internetportal/basis-informationen-krebs/krebsarten/andere-krebsarten/gebaermutterkoerperkrebs.html (ultimo accesso 05/01/2024).
HAUSARZT PRAXIS 2024; 19(1): 41
InFo ONKOLOGIE & HÄMATOLOGIE 2024; 12(1): 26
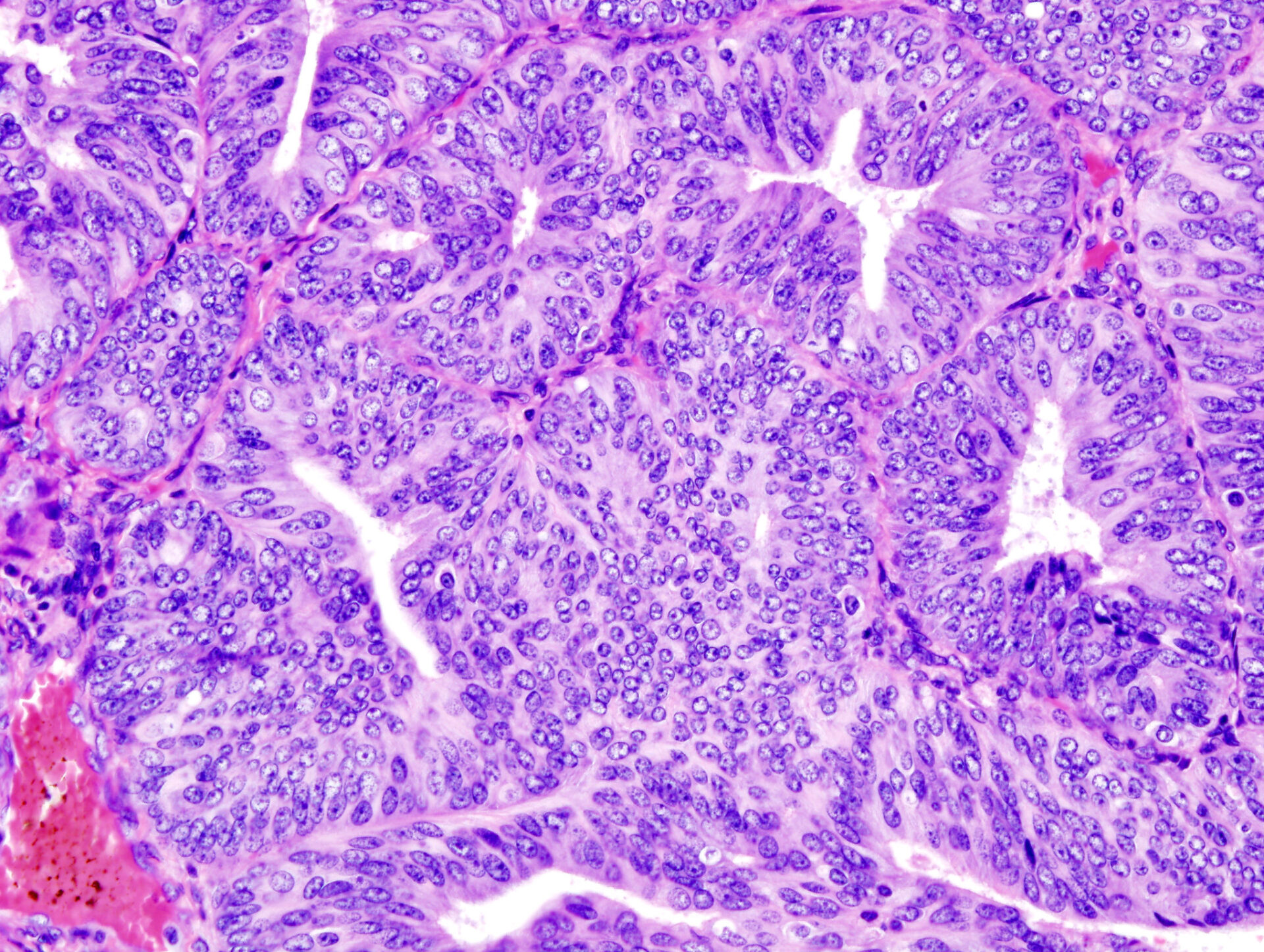
Immagine di copertina: Rappresentazione istopatologica dell’adenocarcinoma endometrioide dimostrato nella biopsia endometriale. Macchia di ematossilina-eosina.
© KGH, wikimedia