Negli ultimi anni, lo spettro di trattamento dei pazienti con malattia infiammatoria intestinale (IBD) si è ampliato in modo significativo. Sulla base della consapevolezza che l’infiammazione cronica e non trattata ha un’influenza sfavorevole sul decorso della malattia, oggi si diffonde l’intervento farmacologico precoce e il monitoraggio intensivo per prevenire le complicazioni.
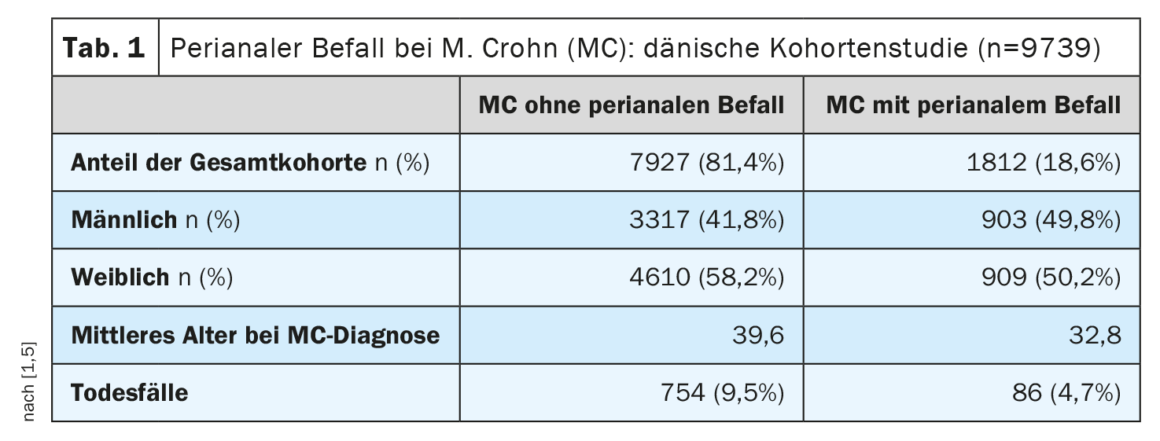
La malattia di Crohn (MC) è caratterizzata da un quadro eterogeneo di fenotipi diversi [1]. La valutazione dell’attività e della gravità della MC si basa principalmente su parametri di laboratorio e su informazioni cliniche e anamnestiche (ad esempio, frequenza delle feci, condizione, dolore). Questi parametri sono stati riassunti in vari punteggi clinici, con l’indice di attività della malattia di Crohn (CDAI) che è il più comune [2]. Il valore di cut-off per la MC da moderata a grave secondo la FDA/EMA è CDAI ≥220 [3]. Il professor David T. Rubin, MD, Università di Chicago, ha sottolineato che i pazienti con MC lieve ma con malattia perianale dovrebbero essere classificati come moderati o gravi in termini di trattamento. [4,5]L’infestazione perianale si verifica in circa il 20% dei pazienti con MC durante il decorso della malattia. Questo è dimostrato, tra l’altro, da uno studio di coorte danese su larga scala (Tab. 1).
Monitoraggio del decorso della malattia e del trattamento
La terapia mira inizialmente a indurre la remissione. A lungo termine, l’obiettivo è mantenere la remissione. Il controllo della malattia è inteso come un costrutto multidimensionale nel MC (riquadro) . La gamma di opzioni di trattamento farmacologico si è notevolmente ampliata. L’introduzione degli anticorpi contro il fattore di necrosi tumorale (TNF)-α è stata seguita dall’anticorpo α4β7 vedolizumab e dall’anticorpo (IL)-12/ IL-23 ustekinumab. È importante valutare il decorso della malattia e del trattamento sullo sfondo della dimensione temporale, dice il Prof. Rubin. [1,6,7]Diverse analisi post-hoc hanno dimostrato che la risposta dei pazienti affetti da MC con una durata di malattia più breve al trattamento con anticorpi anti TNF-α, ustekinumab e vedolizumab è migliore rispetto a quelli con una durata di malattia più lunga.
| Decisione terapeutica basata sull’evidenza La scelta della terapia si basa su una valutazione del rapporto rischio/beneficio, in cui devono essere presi in considerazione diversi fattori e anche situazioni di trattamento particolari. Un’interpretazione appropriata dei dati è un prerequisito per prendere decisioni terapeutiche basate sull’evidenza. Gli studi controllati randomizzati sono classificati come prove empiriche forti, seguiti in ordine decrescente da studi testa a testa, dati post-marketing, metanalisi di rete, dati reali, rapporti di casi e infine opinioni di esperti. |
Ad esempio, una meta-analisi pubblicata nel 2020, che ha incluso 18.471 pazienti, ha mostrato che l’uso precoce di biologici (cioè entro due anni dalla diagnosi) era associato a una probabilità da due a tre volte maggiore di remissione clinica a 6-12 mesi. entro due anni dalla diagnosi) è stato associato a una probabilità da due a tre volte maggiore di remissione clinica a 6-12 mesi (OR 2,10 [95% CI: 1,69-2,60], n=2763, p<0,00001) e a tassi di guarigione mucosa più elevati (OR 2,37 [95% CI: 1,78-3,16], n=994, p<0,00001) [8].
Vedolizumab e ustekinumab: dati dello studio attuale
Nello studio SEAVUE, ustekinumab e adalimumab sono stati confrontati testa a testa [9]. Si è trattato di uno studio randomizzato, in doppio cieco e con controllo attivo, con un disegno a gruppi paralleli. In totale, erano disponibili i risultati valutabili di 386 pazienti biologici-naïve trattati con ustekinumab (n=191) o adalimumab (n=195). Non ci sono state differenze significative tra i due biologici nell’endpoint clinico alla settimana 52: i tassi di risposta per adalimumab e ustekinumab sono stati rispettivamente del 61,0% e del 64,9% (p=0,417), con la remissione clinica operata come CDAI <150 alla settimana 52. In termini di tollerabilità, tuttavia, ustekinumab ha ottenuto risultati leggermente migliori.
In un’analisi secondaria pubblicata nel 2022, ustekinumab si è dimostrato superiore a vedolizumab nel contesto di seconda linea (dopo la terapia anti-TNF). L’analisi si è basata su 5 studi (4 retrospettivi e 1 prospettico) in pazienti MC con trattamento anti-TNF fallito. [10]Nella fase di mantenimento, ustekinumab ha funzionato meglio di vedolizumab e nella fase di induzione, i due anticorpi monoclonali hanno mostrato effetti terapeutici simili.
Opzioni di trattamento dei gas di scarico
Altre terapie biologiche sono attualmente oggetto di studi registrativi, tra cui il risankizumab, per esempio. Questo anticorpo si lega alla subunità p19 dell’interleuchina-23 umana (IL-23), inibendo l’interazione con il suo recettore. [11]Negli studi clinici, il risankizumab si è dimostrato efficace sia nei pazienti di prima linea che in quelli esperti di biologici. Una buona risposta a risankizumab è stata osservata anche nei pazienti precedentemente trattati con ustekinumab. Secondo il relatore, risankizumab è adatto in una fase iniziale del trattamento, grazie alla sua buona sicurezza e tollerabilità. Secondo i dati attuali, ha senso utilizzarlo anche nelle sequenze di trattamento successive.
Ilcontrollo della malattia come costrutto multidimensionaleFattori importanti legati al paziente per la valutazione del controllo della malattia sono, ad esempio, BMI, sesso, nutrizione, farmacogenomica, aderenza, fumo. Oltre alla gravità e all’attività della malattia, i fattori correlati alla malattia includono anche la latenza diagnostica, il fenotipo, i fattori extraintestinali e i precedenti tentativi di trattamento. I fattori legati alla terapia si riferiscono alle proprietà farmacocinetiche e farmacodinamiche del principio attivo, nonché alla via di somministrazione e al profilo complessivo beneficio-rischio. I predittori di un decorso complesso della MC in termini di fattori di rischio indipendenti alla diagnosi (Tabella 2) includevano l’età più giovane, le manifestazioni perianali e la necessità di una terapia steroidea precoce. |
| secondo [3] |
Per quanto riguarda la sequenza della terapia biologica e dell’intervento chirurgico, le attuali raccomandazioni delle linee guida consigliano di non interrompere la terapia biologica a lungo termine, ma piuttosto di programmare l’intervento chirurgico al termine del normale intervallo di somministrazione dei biologici, a condizione che l’attività della malattia lo consenta [1].
Nelle piccole molecole, l’inibitore della Janus chinasi (JAK) tofacitinib è stato finora approvato solo per la colite ulcerosa. [12]L’upadacitinib, anch’esso un inibitore JAK, è attualmente oggetto di studi clinici di fase III per il trattamento della malattia di Crohn.
Congresso: Organizzazione Europea Crohn e Colite
Letteratura:
- “Diagnostica e terapia della malattia di Crohn”, Società tedesca di gastroenterologia, malattie dell’apparato digerente e metabolico (DGVS), linea guida S3 aggiornata, agosto 2021 – numero di registro AWMF: 021-004.
- Best WR, et al: Sviluppo di un indice di attività della malattia di Crohn. Studio cooperativo nazionale sulla malattia di Crohn. Gastroenterologia 1976; 70: 439-444.
- “Sequenza di trattamento nella CD da moderata a grave: chi è il primo e chi l’ultimo?”, Prof. David T. Rubin, MD, ECCO, Copenhagen, 1-4 marzo 2023.
- Eglinton TW, et al: Fattori di rischio clinici e genetici per la malattia di Crohn perianale in una coorte basata sulla popolazione. Am J Gastroenterol 2012; 107: 589-596.
- Wewer MD, et al: The Incidence and Disease Course of Perianal Crohn’s Disease: A Danish Nationwide Cohort Study, 1997-2015. J Crohns Colitis 2020; 15: 5-13.
- Alric H, et al: L’efficacia di ustekinumab o vedolizumab in 239 pazienti con malattia di Crohn refrattaria agli anti-fattore di necrosi tumorale. Aliment Pharmacol Ther 2020; 51: 948-957.
- Hamdeh S, et al: Uso precoce e tardivo della terapia anti-TNFa nei pazienti adulti con malattia di Crohn: revisione sistematica e meta-analisi. Inflamm Bowel Dis 2020; 26: 1808-1818.
- ngaro RC, et al: Revisione sistematica e meta-analisi: efficacia e sicurezza del trattamento biologico precoce nei pazienti adulti e pediatrici con malattia di Crohn. Aliment Pharmacol Ther 2020; 51(9): 831-842.
- Sands BE, et al: Gruppo di studio SEAVUE. Ustekinumab rispetto ad adalimumab per la terapia di induzione e di mantenimento in pazienti biologici-naive con malattia di Crohn da moderatamente a gravemente attiva: uno studio multicentrico, randomizzato, in doppio cieco, a gruppi paralleli, di fase 3b. Lancet 2022; 399(10342): 2200-2211.
- Parrot L, et al: Revisione sistematica con meta-analisi: l’efficacia di ustekinumab o vedolizumab nei pazienti con malattia di Crohn refrattaria agli anti-fattore di necrosi tumorale. Aliment Pharmacol Ther 2022; 55(4): 380-388.
- Farrante M, et al: Presentato alla UEGW. Ottobre 2022. OP128.
- Chugh R, et al: Esperienza multicentrica del mondo reale di Upadacitinib nel trattamento della malattia di Crohn. J Crohns Colitis 2023; 17(4): 504-512.
- (ACG) Lichtenstein GR, et al: Linee guida cliniche ACG: Gestione della malattia di Crohn negli adulti. Am J Gastroenterol 2018; 113: 481-517.
HAUSARZT PRAXIS 2023; 18(5): 37-38 (pubblicato il 25.5.23, prima della stampa).