I nuovi dati di fase III degli studi DISCOVER-1 e DISCOVER-2 mostrano un miglioramento dei sintomi articolari e cutanei dell’artrite psoriasica alla settimana 52. Un’espansione delle indicazioni di guselkumab è attualmente in fase di revisione. Si tratterebbe di un ulteriore progresso nelle opzioni di trattamento di questa penosa malattia autoimmune.
I dati dei due studi del programma DISCOVER hanno costituito la base della domanda di autorizzazione all’immissione in commercio presentata per Tremfya® per il trattamento di pazienti adulti con PsA attiva. Circa il 75% dei pazienti trattati con Tremfya® ha ottenuto una risposta ACR-20 negli studi DISCOVER-1 e DISCOVER-2 [1,2]. Questi sono i primi risultati di fase III della durata di un anno che studiano l’inibizione specifica dell’IL23p19 nell’artrite psoriasica attiva. I dati sono stati presentati all’European League Against Rheumatism (EULAR) E-Congress 2020 e pubblicati su The Lancet [3–5]. Nei due studi clinici di fase III, guselkumab (Tremfya®) nei pazienti adulti con artrite psoriasica attiva (PsA) ha mostrato miglioramenti in diversi endpoint clinici, tra cui i sintomi articolari e cutanei, l’infiammazione dei tessuti molli, la funzionalità fisica e la riduzione della progressione radiografica alla settimana 52 [1,2]. Tremfya® non è attualmente approvato per il trattamento della PsA ed è in fase di revisione da parte di Swissmedic per questo uso.
| Abbreviazioni ACR = criterio di risposta ACR MDA = Attività minima della malattia DAS-28 = Punteggio di attività della malattia 28 VLDA = Attività di malattia molto bassa HAQ-DI = Indice di disabilità del Questionario di Valutazione della Salute SF-36 = Questionario di indagine sulla salute in forma breve 36 PCS = Riassunto del componente fisico MCS = Riassunto della componente mentale |
DISCOVER-1 e DISCOVER-2 dimostrano efficacia e sicurezza
I pazienti inclusi in DISCOVER-1 erano naïve ai biologici o avevano ricevuto in precedenza dei biologici anti-TNF-α. DISCOVER-2 comprendeva solo pazienti naïve ai biologici. DISCOVER-2 ha anche analizzato la progressione radiologica del danno articolare. In entrambi gli studi, i pazienti sono stati randomizzati per un periodo di un anno in due gruppi verum, Tremfya® 100 mg ogni 4 settimane (q4w) o ogni 8 settimane (q8w), e gruppi placebo con crossover alla settimana 24 a Tremfya® q4w. I risultati sono stati presentati come poster al congresso elettronico dell’EULAR di quest’anno [1,2]. Gli studi DISCOVER hanno anche mostrato miglioramenti in diversi endpoint secondari alla settimana 52 rispetto alla settimana 24, tra cui la risposta ACR70, la risoluzione dell’infiammazione dei tessuti molli (entesite e dattilite) [7], il punteggio dell’attività di malattia (DAS-28), la proteina C-reattiva (CRP) [4], l’attività di malattia minima (MDA) [8], l’attività di malattia molto bassa (VLDA) [9], il miglioramento del funzionamento fisico (HAQ-DI) [7], il miglioramento complessivo della salute (SF-36*, PCS**, MCS†).
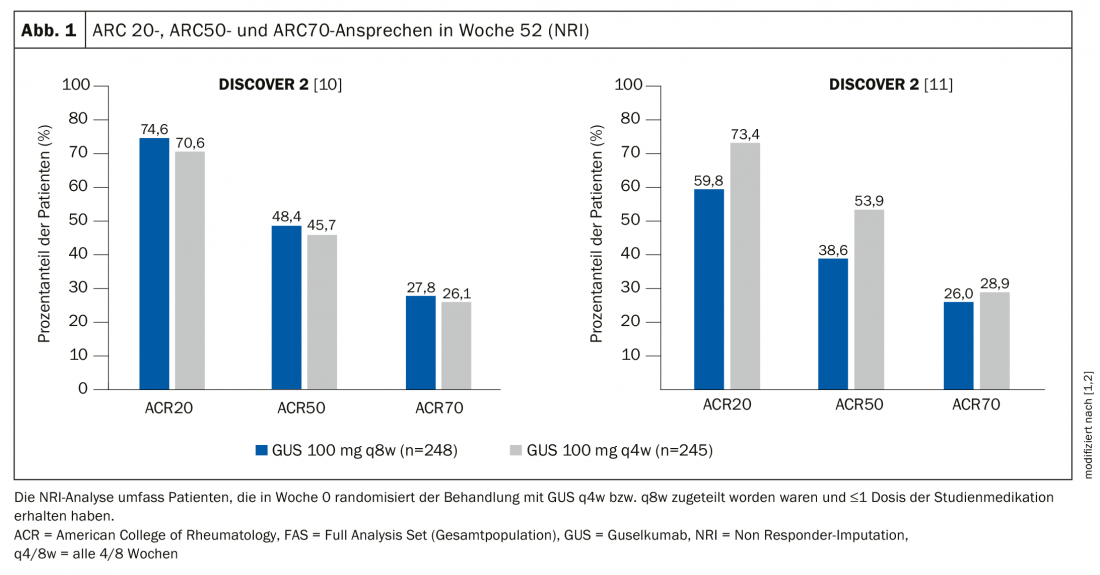
In entrambi gli studi, Tremfya® è stato ben tollerato fino alla fine dello studio e gli eventi avversi osservati erano generalmente coerenti con gli studi precedenti su Tremfya® e con le attuali informazioni di prescrizione [6]. Gli effetti avversi gravi e le infezioni gravi si sono verificati nel 4% e nell’1% dei pazienti trattati con Tremfya®, sia in DISCOVER-1 che in DISCOVER-2. Non sono stati segnalati decessi nei pazienti trattati con Tremfya® e nessun paziente trattato con Tremfya ha avuto malattie infiammatorie intestinali, infezioni opportunistiche, tubercolosi attiva o reazioni anafilattiche o simili alla malattia da siero [1,2].
Fonte: Janssen
*/** L’SF-36 è un questionario per i pazienti che misura la salute funzionale e il benessere in base ai resoconti dei pazienti. Come parte dell’SF-36, la sottoscala PCS è composta da quattro scale che valutano la funzione fisica, le limitazioni causate da problemi fisici, i sintomi del dolore somatico e la salute generale.
† L’MCS è composto da quattro scale che valutano la vitalità, l’impatto emotivo, il funzionamento sociale e la salute mentale.
Letteratura:
- Ritchlin C, et al: Guselkumab, un inibitore dell’IL-23 che si lega specificamente alla subunità IL23p19, per l’artrite psoriasica attiva: risultati a un anno di uno studio di fase 3, randomizzato, in doppio cieco, controllato con placebo, condotto su pazienti biologicamente naïve o con esperienza di inibitori del TNFα. SAT0397. Presentato al 2020 EULAR E-Congress dal 3 al 6 giugno.
- McInnes I, et al: Efficacia e sicurezza di Guselkumab, un anticorpo monoclonale specifico per la subunità p19 dell’interleuchina-23, fino alla settimana 52 di uno studio di fase 3, randomizzato, in doppio cieco, controllato con placebo, condotto in pazienti naïve ai biologici con artrite psoriasica attiva. SAT0402. Presentato al 2020 EULAR E-Congress dal 3 al 6 giugno.
- Business Wire. Janssen cerca di espandere l’uso di TREMFYA, www.businesswire.com/news/home/20191022006172/en/Janssen-Seeks-Expand-TREMFYAC2AEE296%BC-guselkumab-Treatment-Adults® (guselkumab) nel trattamento degli adulti con artrite psoriasica attiva. ultima chiamata 28.07.2020.
- Deodhar A, et al: Guselkumab in pazienti con artrite psoriasica attiva che erano biologici-naive o avevano ricevuto in precedenza un trattamento con inibitore del TNFα (DISCOVER-1): uno studio di fase 3 in doppio cieco, randomizzato, controllato con placebo. The Lancet 2020; 395: 1115-1125.
- Mease PJ, et al: Guselkumab in Biologic-naive Patients with Active Psoriatic Arthritis (DISCOVER-2): Uno studio di fase 3 in doppio cieco, randomizzato e controllato con placebo. The Lancet 2020; 395: 1126-1136.
- Informazioni tecniche su TREMFYA®, a partire dal 09/2019, disponibili su www.swissmedicinfo.ch.
- Clinicaltrials.gov: Studio che valuta l’efficacia e la sicurezza di Guselkumab somministrato per via sottocutanea nei partecipanti con artrite psoriasica attiva, compresi quelli precedentemente trattati con agenti biologici anti-fattore di necrosi tumorale (TNF) alfa (DISCOVER-1). Identificatore: NCT03162796. https://clinicaltrials.gov/ct2/show/NCT03162796, ultimo accesso 28.07.2020.
- Gossec L, et al: L’attività minima della malattia come obiettivo del trattamento nell’artrite psoriasica: una revisione della letteratura. J Rheumatol 2018; 45: 6-13.
- Coates L, et al: Abstract 2548. Presentato alla Riunione annuale ACR/ARHP 2017. Disponibile presso: https://acrabstracts.org/abstract, ultimo accesso 28.07.2020.
- McInnes, et al.: Presentato all’EULAR E-Congress, giugno 2020. Poster 0402.
- Ritchlin, et al: Presentato all’EULAR E-Congress, giugno 2020, Poster 0397.
PRATICA GP 2020, 15(8): 36-37
PRATICA DERMATOLOGICA 2020; 30(4): 28-29