Secondo le nuove linee guida ESPEN, le misure di nutrizione enterale dovrebbero essere generalmente preferite alla nutrizione parenterale. Esistono tuttavia alcune eccezioni, che comprendono controindicazioni come l’ostruzione intestinale, lo shock grave, l’ischemia intestinale, le fistole ad alto rendimento o l’emorragia intestinale.
In questi casi, può essere necessaria la nutrizione parenterale per un periodo di giorni o settimane, fino al ripristino della funzione gastrointestinale, secondo le nuove linee guida della Società Europea di Nutrizione Clinica e Metabolismo (ESPEN), pubblicate sulla rivista Clinical Nutrition nel marzo di quest’anno. [1,2] (Panoramica 1). In presenza di insufficienza intestinale acuta/fistole enterocutanee, la nutrizione parenterale è spesso necessaria a causa della compromissione del tratto gastrointestinale, eventualmente in aggiunta alla nutrizione enterale [3]. Una combinazione di nutrizione enterale e parenterale dovrebbe essere presa in considerazione nei pazienti in cui più del 60% dell’apporto energetico richiesto non è fornito dalle misure enterali (raccomandazione 25A) [2]. L’infusione parenterale di fluidi ed elettroliti può essere necessaria se persistono stomi ad alto rendimento (raccomandazione 9B). Nella fase perioperatoria dei pazienti con IBD, la nutrizione parenterale è solitamente indicata come supplemento alla nutrizione enterale (raccomandazione 25B) [1]. Nei pazienti affetti da malattia di Crohn con insufficienza gastrointestinale persistente (come la sindrome dell’intestino corto dopo la resezione), l’infusione di nutrienti è una misura necessaria e salvavita, almeno nelle fasi iniziali dell’insufficienza intestinale (raccomandazione 26B) [1]. Subito dopo una proctocolectomia o una colectomia, è necessario fornire acqua ed elettroliti per garantire la stabilità emodinamica (raccomandazione 27B) [1].

I pazienti con stomia beneficiano della nutrizione parenterale
Una diarrea persistente e grave o uno stoma ad alto rendimento possono portare a un’insufficienza intestinale caratterizzata da malassorbimento, perdita di peso involontaria, malnutrizione e/o disidratazione. Il malassorbimento è un fattore importante per la malnutrizione nelle IBD [4,5]. Uno studio retrospettivo [6] su 687 pazienti portatori di stomia ha mostrato che l’elevata produzione precoce di un’ileostomia entro tre settimane è comune e, sebbene il 49% guarisca spontaneamente, il 51% richiede un ulteriore trattamento medico, soprattutto a causa di una precedente sindrome dell’intestino corto. Il 71% dei pazienti è stato trattato con restrizione di liquidi ipotonici per via orale, soluzione di glucosio e sale e farmaci antidiarroici per interrompere le infusioni parenterali. Nell’8% dei casi, è stato necessario continuare l’infusione parenterale o sottocutanea di soluzione salina a casa. È stato dimostrato diversi anni fa che il trattamento con l’assunzione di liquidi per via orale e il monitoraggio del sodio nelle urine è fattibile in ambito domestico [7].
In uno studio su 13 adulti con stomie ad alto rendimento, le soluzioni reidratanti orali contenenti integratori di maltodestrina di riso hanno migliorato l’equilibrio di sodio e potassio. Un’associazione tra l’aumento del peso corporeo e la diminuzione delle concentrazioni di renina sierica suggerisce che l’equilibrio idrico potrebbe essere raggiunto anche [11]. In un altro studio, sono state testate tre diverse soluzioni saline e/o di glucosio in sei pazienti con digiunostomia. In base ai risultati di questo campione relativamente piccolo, una soluzione orale di glucosio-elettrolita sembra essere un sostituto adeguato del sodio nei pazienti con stomie ad alto rendimento [8].
Nei casi di studio, il trattamento con restrizione di liquidi ipotonici, dieta arricchita di sodio, alimentazione solo enterale e/o infusioni parenterali contenenti sodio ha mostrato effetti positivi nei pazienti con malattia di Crohn con stoma ad alta uscita.
Dopo l’intervento chirurgico, è stato dimostrato che l’alimentazione precoce post-operatoria è associata a una riduzione significativa delle complicanze rispetto ai metodi tradizionali di alimentazione post-operatoria. Non è stato possibile stabilire un’influenza negativa sulla mortalità, sulla deiscenza dell’anastomosi, sulla ripresa della funzione intestinale o sulla durata dell’ospedalizzazione [9]. In una revisione sistematica Cochrane [10] l’alimentazione orale o enterale precoce, compresi i liquidi chiari il primo o il secondo giorno dopo l’intervento, non ha peggiorato la guarigione delle anastomosi coloniche o rettali ed è stata correlata a tempi di ospedalizzazione significativamente più brevi.
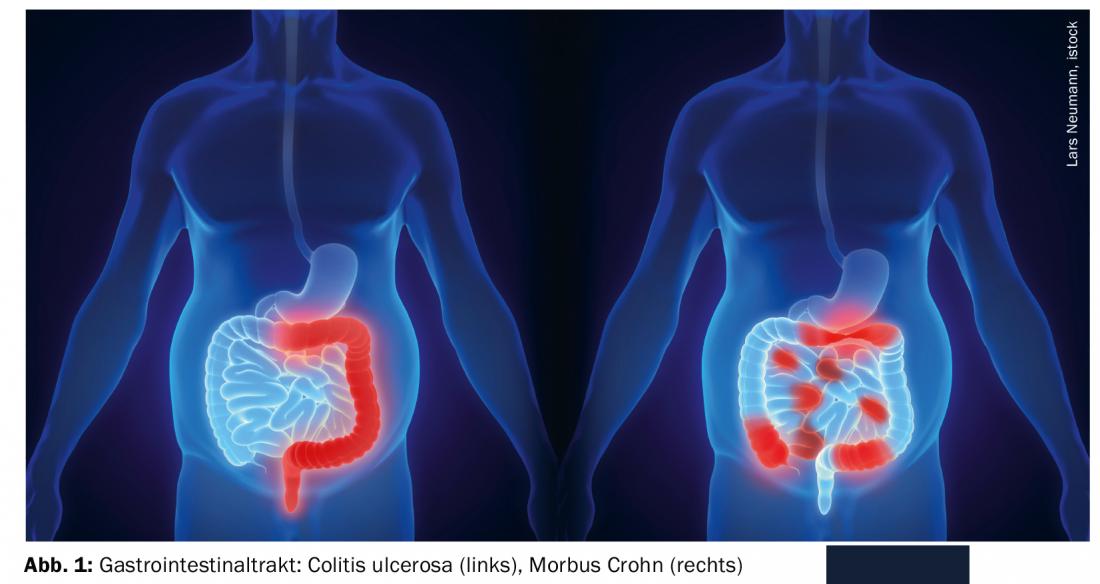
Misure generali legate alla nutrizione nell’IBD
Le linee guida ESPEN raccomandano che i pazienti con malattia infiammatoria intestinale che sono ad alto rischio di malnutrizione siano sottoposti a screening per la malnutrizione al momento della diagnosi e durante il follow-up. Se viene rilevata la malnutrizione, è necessario fornire un trattamento adeguato, poiché la qualità della vita, le complicazioni, la prognosi e la mortalità possono essere influenzate. Nelle IBD attive, l’apporto proteico deve essere aumentato (fino a 1,2-1,5 g/kg/d). Nella fase di remissione, il fabbisogno proteico normalmente non aumenta; in questo caso, è sufficiente un apporto di 1 g/kg/d, analogo a quello degli adulti sani. Tutti i pazienti con IBD dovrebbero essere sottoposti a screening regolari per le carenze di micronutrienti, e dovrebbero essere affrontate le carenze specifiche di vitamine o oligoelementi.
Anche i test per l’anemia sono importanti. Se viene rilevata un’anemia da carenza di ferro, si raccomanda un trattamento con integrazione di ferro per reintegrare i livelli di emoglobina (Hb) e le riserve di ferro. Nell’anemia lieve e nell’IBD clinicamente inattiva, il ferro orale è raccomandato come trattamento di prima linea, se non ci sono controindicazioni/intolleranze. La terapia sostitutiva di ferro per via endovenosa è consigliata nei pazienti con IBD clinicamente attiva o intolleranza al ferro orale, nonché nei livelli di Hb inferiori a 100 g/L e nei pazienti che richiedono agenti stimolanti l’eritropoietina.

Non esiste una dieta specifica per l’IBD che abbia dimostrato di favorire la remissione. Nei pazienti adulti e pediatrici con IBD attiva e in quelli in trattamento con steroidi, i livelli di calcio e di vitamina 25(OH) devono essere monitorati e integrati, se necessario, per prevenire una bassa densità ossea. Se è presente osteopenia o osteoporosi, si raccomanda di trattarla secondo le linee guida pertinenti. Le diete di esclusione non sono raccomandate, non ci sono prove che questo favorisca la remissione dell’IBD attiva, anche quando il paziente soffre di intolleranze individuali. Quando si dovrebbero usare i probiotici? Nei pazienti con colite ulcerosa da lieve a moderata, si può prendere in considerazione il Lactobacillus reuteri o “VSL#3” per indurre la remissione, ma non altri probiotici. I probiotici non devono essere utilizzati nella colite ulcerosa attiva.
Letteratura:
- Bischoff SC, et al: Linea guida pratica ESPEN: Nutrizione clinica nella malattia infiammatoria intestinale. ESPEN. Clin Nutr 2020; 39(3): 632-653.
- Weimann A, et al: Linea guida ESPEN: nutrizione clinica in chirurgia. Clin Nutr 2017; 36: 623-650
- Slonim AE, et al: Effetto della dieta di esclusione con terapia nutraceutica nella malattia di Crohn giovanile. J Am Coll Nutr. 2009; 28: 277-285.
- Pironi L, et al: Nutrizione artificiale domiciliare e insufficienza intestinale cronica; gruppi di interesse sull’insufficienza intestinale acuta dell’ESPEN. Raccomandazioni approvate dall’ESPEN. Definizione e classificazione dell’insufficienza intestinale negli adulti. Clin Nutr 2015; 34: 171-180.
- Hart JW, et al: Spesa energetica misurata rispetto a quella prevista nei bambini con malattia di Crohn inattiva. Clin Nutr 2005; 24: 1047-1055.
- Baker ML, et al: Cause e gestione di uno stoma ad alta uscita. Dis. colorettale. 2011; 13: 191-197
- Grischkan D, et al: Mantenimento dell’iperalimentazione domiciliare nei pazienti con digiunostomia ad alto rendimento. Arch Surg 1979; 114: 838-841.
- Nightingale JM, et al: Supplementi salini orali per compensare le perdite della digiunostomia: confronto tra capsule di cloruro di sodio, soluzione elettrolitica di glucosio e soluzione elettrolitica di polimeri di glucosio. Gut 1992; 33: 759-761.
- Osland E, et al: Alimentazione precoce rispetto all’alimentazione post-operatoria tradizionale nei pazienti sottoposti a chirurgia gastrointestinale resezionale: una meta-analisi. J Parenter Enter Nutr 2011; 35: 473-448.
- Shukla HS, et al: Iperalimentazione enterale nei pazienti chirurgici malnutriti. Indian J Med Res 1984; 80: 339-346.
- Pironi L, et al.: Soluzione reidratante orale contenente maltodestrine di riso in pazienti con colectomia totale e alta produzione intestinale. Int J Clin Pharmacol Res 2000; 20: 55-60.
PRATICA GP 2020; 15(11): 40-41