Com o antisense oligonucleotide nusinersen, o primeiro medicamento para o tratamento causal de pacientes com atrofia muscular espinal associada a 5q (5q-SMA) foi aprovado em 2017 [1]. O medicamento visa a causa da doença, a falta da proteína SMN [1]. Extensos estudos clínicos e do mundo real demonstraram que a nusinersen pode levar à estabilização e mesmo à melhoria da função motora – em todos os grupos etários e tipos de AME I-III [2-7].
5q-SMA é uma doença neomuscular progressiva autossomal recessiva [8]. Se não forem tratados, os pacientes correm o risco de degeneração progressiva dos neurónios motores, resultando em fraqueza e atrofia crescente dos músculos [8]. Até à introdução de uma terapia medicamentosa causalmente eficaz, a forma infantil de 5q-SMA, em que os sintomas já são visíveis nos primeiros 6 meses de vida, era considerada uma das causas genéticas mais comuns de morte em bebés e crianças pequenas [8]. Com nusinersen (SPINRAZA®), está disponível uma opção terapêutica que torna possível manter ou mesmo aumentar a força muscular [1-7].
Nusinersen leva à formação de quantidades mais elevadas de proteína SMN [9].
A causa da denervação progressiva dos músculos esqueléticos é uma deficiência da proteína “survival motor neuron” (SMN), que é vital para os neurónios motores. Devido a mutações ou supressões no gene SMN1, muito pouca proteína SMN é produzida em doentes com 5q-SMA [8].
Nusinersen contribui para a produção de proteína SMN mais funcional e assim assegura que os neurónios motores possam sobreviver [9]. Isto pode abrandar ou mesmo parar o curso da doença. Os pacientes beneficiam da preservação ou melhoria da função muscular. A eficácia do nusinersen foi demonstrada para todas as idades e estados da doença: bebés com AME 5q pré-sintomática, crianças e adolescentes sintomáticos, e adultos [2-7].
Crianças com 5q-SMA beneficiam de terapia pré-sintomática
Em ensaios clínicos, muitas crianças com 5q SMA tratadas com nusinersen conseguiram atingir importantes marcos motores não observados em doentes não tratados com 5q SMA [2-4]. Isto mostrou que a terapia SPINRAZA precoce pode permitir um desenvolvimento adequado à idade em crianças com 5q-SMA. A maioria dos pacientes com 5q-SMA geneticamente diagnosticados que foram pré-sintomaticamente tratados com nusinersen no ensaio clínico NURTURE tinham atingido os marcos motores adequados à sua idade na avaliação intercalar do estudo (Tab. 1) [10].
Quadro 1: Avaliação intercalar do estudo NURTURE em Fevereiro de 2020; idade média dos participantes no estudo 3,8 anos (n = 25) [10]
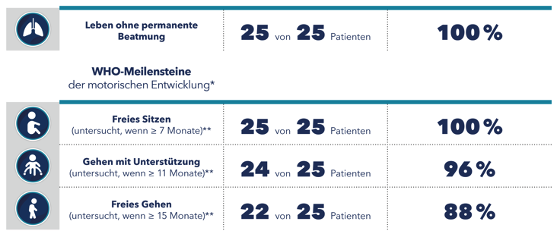





* Idade em que as crianças saudáveis atingem normalmente estes marcos.
** A hora do exame foi dentro do período de tempo especificado pela OMS [11]
Foram também observadas melhorias significativas nas funções de bulbar, que são necessárias para mastigar e engolir [12]. Enquanto muitos pacientes não tratados com pneus 5q-SMA quando mastigam, se engasgam com alimentos ou requerem uma sonda de alimentação [13-16], o tratamento pré-sintomático com nusinersen no estudo NURTURE resultou em 92% das crianças continuarem a engolir e 84% conseguirem sem uma sonda de alimentação [12]. Assim, os pais de crianças com 5q-SMA tratados com nusinersen não estavam geralmente preocupados com a deglutição, alimentação e peso dos seus filhos [12].
Eficácia de nusinersen também comprovada em adultos
Dados exaustivos de estudos observacionais em doentes adultos com 5q-SMA mostram que o tratamento com nusinersen pode conduzir a melhorias significativas em todas as escalas de função motora utilizadas (HFMSE, RULM, 6 minutos de distância a pé) [5-7].
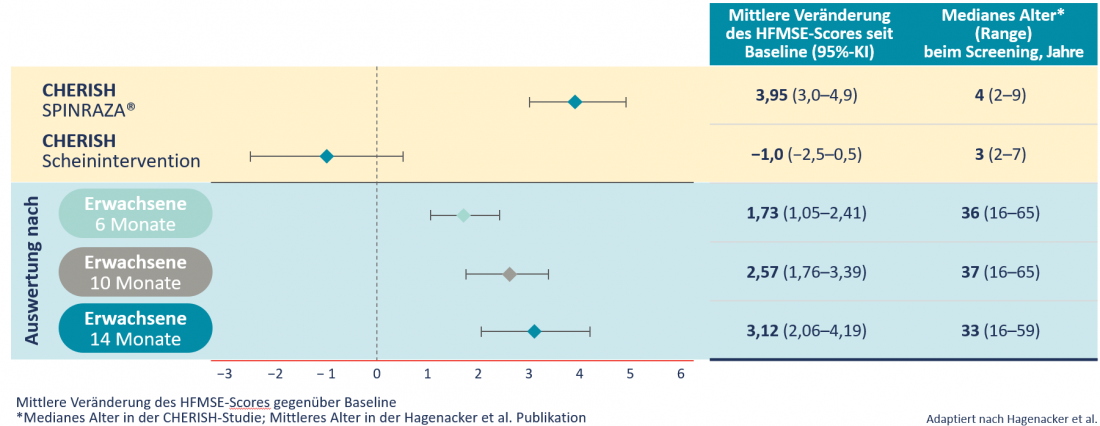
Num estudo prospectivo, multicêntrico envolvendo 139 pacientes de 10 centros clínicos na Alemanha, uma elevada proporção de pacientes com 5q-SMA tipo II ou III mostrou melhorias clinicamente relevantes na função motora. Em todos os pontos do tempo de estudo, os pacientes alcançaram melhorias estatisticamente significativas na pontuação HFMSE em média. Isto tinha aumentado em 3,12 pontos após 14 meses. No entanto, no curso natural da doença, a pontuação do HFMSE diminui em média 0,5-1,0 pontos por ano [6]. Uma melhoria comparável na pontuação HFMSE foi observada em adultos como em crianças (Tab. 2) [6].
Tabela 2: Alterações médias na pontuação HFMSE desde a linha de base: Comparação de 126 crianças com doença 5q-SMA de início tardio do estudo CHERISH e 173 pacientes adultos do estudo Hagenacker et al. Publicação [3,6].

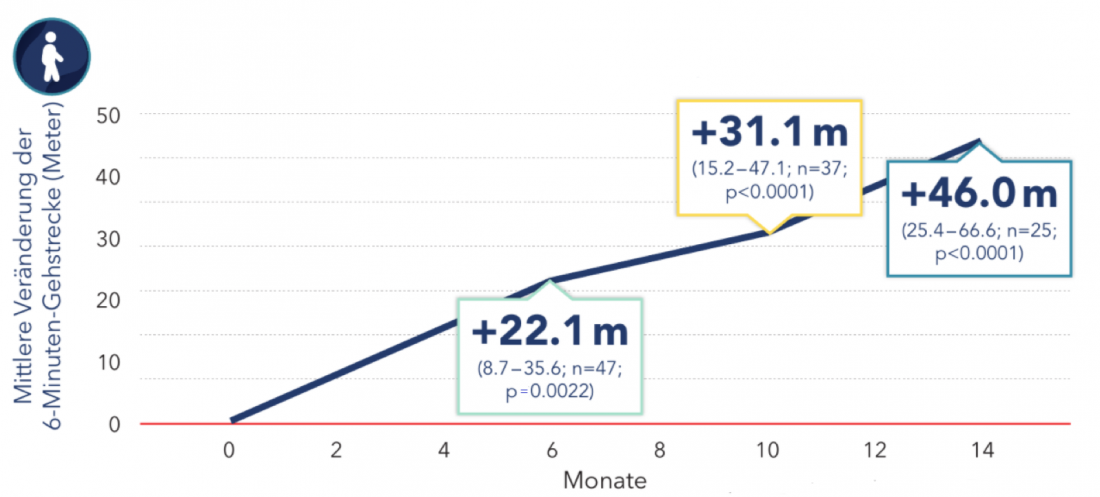
A pontuação RULM, que mede a função dos membros superiores, mostrou uma melhoria significativa de 1,09 pontos em média após 14 meses no estudo. Além disso, os pacientes conseguiram cobrir uma média de 403 metros em 6 minutos. Em média, foram capazes de caminhar 46 metros mais do que antes do início da terapia (Fig. 2) [6].
A idade dos pacientes não teve qualquer influência nos resultados. No entanto, a extensão das melhorias dependia da função motora residual do paciente no início do estudo. Quanto maior for o nível de função motora residual antes do início da terapia, maior será o efeito esperado da terapia nusinersen [6].
Figura 2: Mudança em 6 minutos a pé em adultos com terapia de nusinersen. As caixas mostram média e IC 95% [6]. Modificado de acordo com Hagenacker T et al. [6].
Os pacientes querem participar na vida normal
Muitos pacientes adultos desejam manter as suas forças para que possam sentar-se, levantar-se e caminhar independentemente [17]. As funções das mãos e dos braços são indispensáveis para tarefas quotidianas, tais como poder lavar-se ou vestir-se de forma independente. As capacidades motoras finas também desempenham um papel importante no ambiente social dos pacientes, que se manifesta na utilização de um smartphone ou de um computador portátil.
No entanto, no curso natural do 5q-SMA, há uma fraqueza muscular progressiva e perda da função motora [8]. O tratamento com nusinersen pode dar aos adultos com 5q-SMA esperança para o futuro. Os pacientes podem assim não só conseguir uma estabilização a longo prazo do status quo funcional, como muitos deles experimentam melhorias relevantes nas funções motoras, têm mais força nas mãos e nos dedos e podem levantar-se melhor, ficar de pé mais tempo e andar mais longe [5-7].
Efeito direccionado – Central para o SNC
Ao fazê-lo, Nusinersen visa a causa do 5q-SMA. Liga-se reversivelmente ao pré-mRNA do gene parálogo SMN2, que é utilizado para a formação da proteína SMN em doentes com 5q-SMA. Isto desloca os factores de emenda e exon 7 permanece no SMN2 mRNA maduro para que se possa formar mais proteína SMN funcional (Fig. 3) [1, 9].
Figura 3: Mecanismo de acção orientada de nusinersen [9].

Nusinersen é administrado por via intratecal através de uma punção lombar e, assim, chega directamente ao local onde é suposto funcionar – o sistema nervoso central [1]. A aplicação Intrathecal assegura que o nusinersen chega directamente ao local central de acção, onde pode exercer o seu efeito direccionado e específico sobre o pré-mRNA do gene SMN2 [1]. O efeito de nusinersen instala-se rapidamente, logo 1 a 3 dias após a injecção [18]. A elevada especificidade do nusinersen e a sua aplicação direccionada ao sistema nervoso central demonstraram ser seguros na utilização a longo prazo e também resultaram num efeito sustentado na função motora numa vasta gama de pacientes com 5q SMA [5-7,10,19-23].
Ao mesmo tempo, a aplicação intratecal tem vantagens em termos de aderência. Os dados até à data mostram que a maioria dos doentes está a receber as suas doses de nusinersen conforme planeado [24]. Para outras doenças, o cumprimento tem demonstrado ser mais elevado para as terapias administradas numa clínica do que para as terapias orais e diárias [25,26]. É portanto razoável supor que, devido à administração intratecal, os médicos podem ter a certeza de que os pacientes recebem a dose certa de nusinersen na altura certa e que a sua saúde e resposta ao tratamento podem ser controladas de rotina.
Não se esperam efeitos secundários sistémicos
Uma vantagem importante da utilização intratecal de nusinersen é a exposição específica ao compartimento, o que torna improváveis os efeitos secundários sistémicos. Isto foi confirmado tanto em estudos clínicos como no mundo real. Dor de cabeça, dores de costas e vómitos são os eventos adversos mais frequentemente observados associados à administração intratecal [1]. Podem ocorrer pouco depois da administração de nusinersen e devem-se em grande parte à síndrome pós-perfuração que pode ocorrer após punções lombares mesmo sem a aplicação de substâncias medicamentosas [6]. O perfil de segurança do nusinersen está bem documentado ao longo de 7 anos [19].
Também pode ser utilizado para escoliose
Mesmo em casos de escoliose pronunciada ou outras deformidades espinais graves, que são comuns em doentes com AME 5q, a injecção intratecal de nusinersen pode geralmente ser bem sucedida, segura e rápida [27]. Se necessário, a injecção no espaço do QCA deve ser efectuada sob controlo de imagem através de tomografia computorizada (CT) [27].
Conclusão
A aplicação central de nusinersen proporciona um efeito direccionado directamente onde ele é necessário. A eficácia do nusinersen foi demonstrada em extensos ensaios clínicos e em estudos do mundo real para todas as idades e severidades de 5q SMA [2-7]. Os doentes adultos com 5q-SMA também podem beneficiar da terapia e alcançar uma estabilização clinicamente significativa ou melhorias na função motora [5-7].
O benefício do nusinersen reflecte-se também na satisfação dos doentes: num estudo prospectivo de observação de doentes adultos realizado na Alemanha, 95,7% referiu satisfação com o nusinersen – independentemente da idade e da gravidade da doença [28].
Entretanto, existe uma vasta experiência da prática clínica diária. Mais de 11.000 pacientes em todo o mundo foram tratados com nusinersen até à data [29].
Literatura
- SPINRAZA® Informação Técnica, a partir de Agosto de 2019 (www.swissmedicinfo.ch)
- Finkel RS, Mercuri E, Darras BT, et al. Nusinersenversus Sham Control in Infantile-Onset Spinal Muscular Atrophy. N Eangl J Med. 2017;377:1723-32.
- Mercuri E, Darras BT, Chiriboga CA, et al. Nusinersen versus Sham Control in Later-Onset Spinal Muscular Atrophy. N Engl J Med. 2018;378:625-35.
- De Vivo DC, Bertini E, Swoboda KJ, et al. Nusinersen iniciado em bebés durante a fase pré-sintomática da atrofia muscular espinal: Resultados provisórios da eficácia e segurança do estudo NURTURE fase 2. Desordem Neuromuscul. 2019;29:842-56.
- Walter MC, Wenniger S, Thiele S, et al. Safety and Treatment Effects of Nusinersen in Longstanding Adult 5q-SMA Type 3 – A Prospective Observational Study. J Neuromuscul Dis. 2019;6:453-65.
- Hagenacker T, Wurster CD, Günther R, et al. Nusinersen em adultos com atrofia muscular espinal 5q: um estudo de coorte não intervencionista, multicêntrico e observacional. Lancet Neurol. 2020;19:317-25.
- Maggi L, Bello L, Bonanno S, et al. Nusinersensafety and effects on motor function in adult spinal muscular atrophy type 2 and 3. J Neurol Neurosurg Psychiatry. 2020;91(11):1166-74.
- Lunn MR, Wang CH. Atrofia muscular espinhal. Lanceta. 2008;371:2120-33.
- Goodkey K, Ashley T, Maruyama R, et al. Nusinersen in the Treatment of Spinal Muscular Atrophy. Métodos Mol Biol. 2018; 1828: 69-76.
- Swoboda KJ, Kirschner J, Finkel RS, et al; Grupo de Estudo NURTURE. Efeito Nusinersen em bebés que iniciam o tratamento numa fase pré-sintomática de SMA: resultados NURTURE. Cura SMA 2020 Conferência Virtual SMA; 8-12 de Junho de 2020; https://curesma2020.biogenscicomm.com/curesma2020/sma/swoboda/#home. Recuperado em Setembro de 2021.
- Grupo de Estudo de Referência de Crescimento Multicêntrico da OMS. Estudo de Desenvolvimento Motor da OMS: janelas de realização para seis marcos de desenvolvimento motor bruto. Acta Paediatr Suppl. 2006; 450: 86 – 95.
- Swoboda KJ, Sansone VA, De Vivo DC, et al. Preservação da função de deglutição em bebés que iniciaram o tratamento nusinersen na fase pré-sintomática da SMA: resultados do estudo NURTURE. Apresentado na Conferência Clínica e Científica MDA 2021, 15-18 de Março de 2021.
- Van der Heul AMB, Wijngaarde CA, Wadman RI, et al. Problemas de Bulbar Auto-Relatados por Crianças e Adultos com Atrofia Muscular Espinhal. J Neuromuscul Dis. 2019;6:361-8.
- Finkel RS, McDermott MP, Kaufmann P, et al. Estudo observacional da atrofia muscular espinhal tipo I e implicações para os ensaios clínicos. Neurologia. 2014;83:810-7.
- Van der Heul AMB, Cuppen I, Wadman RI, et al. Problemas de alimentação e deglutição em bebés com Atrofia Muscular Espinhal Tipo 1: um estudo observacional. J Neuromuscul Dis. 2020;7:323-30.
- Choi YA, Suh DI, Chae JH, et al. Trajectória de alteração do estado de deglutição na atrofia muscular espinhal tipo I. Int J Pediatr Otorhinolaryngol. 2020;130:109818.
- Burbridge C, Kelly K, Garcia L, et al. PND74 Mapeamento de uma exploração qualitativa de uma mudança significativa na atrofia muscular espinal posterior (tipo II ou III) ao Hammersmith Functional Motor Scale Expanded (HFMSE). Valor na Saúde. 2019; 22, Suppl 2, p284.
- Mazur C, Powers B, Zasadny K, et al. Farmacologia cerebral dos oligonucleótidos intratecais antisensoriais revelados através de imagens multimodais. JCI Insight. 2019;4:e129240.
- Claborn MK, Stevens DL, Walker CK, et al. Nusinersen: Um tratamento para a atrofia muscular espinhal. Ann Pharmacother. 2019; 53(1): 61-69.
- Castro D, Finkel RS, Farrar MA, et al. Nusinersen na atrofia muscular espinal infantil: resultados do tratamento a longo prazo do estudo de extensão de SHINE com rótulo aberto. Neurologia. 2020; 94(15):1640.
- Chiriboga CA, et al. Tratamento a longo prazo com nusinersen: resulta em atrofia muscular espinal posterior do estudo do brilho. Apresentado em AAN 2020; 25. Abril-1. Maio 2020; https://www.neurologylive.com/view/nusinersen-shows-efficacy-in-infantile-and-lateonset-spinal-muscular-atrophy; Recuperado em Setembro de 2021.
- Acsadi G, Crawford TO, Müller-Felber W, et al. Segurança e eficácia do nusinersen na atrofia muscular espinhal: O estudo EMBRACE. Nervo Muscular. 2021;63:668-77.
- Duong T, Wolford C, McDermott, MP, et al. Nusinersen Treatment in Adults With Spinal Muscular Atrophy. Prática Neurol Clin. 2021; 11(3): e317-27.
- Paradis A, et al. A experiência de Nusinersen em atrofia muscular espinhal de início posterior. Apresentado no WMS 2020.
- Seal BS, Anderson S, Shermock KM, et al. Factores associados a taxas de aderência para a terapia anti-câncer oral e intravenosa em doentes com cancro do cólon metástático. J Manag Care Spec Pharm. 2016;22:227-35.
- Moran K, Null K, Huang Z, et al. Retrospective Claims Analysis Indirectly Comparing Medication Adherence and Persistence Between Intravenous Biologics and Oral Small-Molecule Therapies in Inflammatory Bowel Diseases. Advertência Ther. 2019;36:2260-72.
- Cordts I, Lingor B, Friedrich P, et al. Administração de nusinersen Intrathecal em pacientes adultos com atrofia muscular espinhal com anatomia espinhal complexa. Ther Adv Neurol Disord 2020; 13: 1756286419887616
- Meyer T, Maier, A, Uzelac Z, et al. Expectativas de tratamento e percepção da terapia em pacientes adultos com atrofia muscular espinhal a receber nusinersen. Eur J Neurol. 2021; 28(8): 2582-95.
- Novos Dados em Cure SMA 2021; Biogen, https://investors.biogen.com/news-releases/news-release-details/new-data-cure-sma-2021-highlight-long-term-efficacy-spinrazar; Último Acesso: Setembro 2021
Resumo resumido da informação do produto SPINRAZA® Z: Um frasco contém 12 mg nusinersen em 5 ml de líquido cerebrospinal artificial. I: Tratamento da atrofia muscular espinhal associada a 5q (SMA) D: Aplicação Intrathecal por punção lombar (LP). 4 Doses de saturação de 12 mg (5ml) por aplicação nos dias 0, 14, 28, 63; terapia de manutenção a cada 4 meses 12 mg (5ml). A Spinraza só deve ser administrada em centros neuromusculares especializados, com base hospitalar. É obrigatório que o pessoal médico assistente tenha experiência no diagnóstico e tratamento de doentes com atrofia muscular espinal e na realização de LP. KI: Hipersensibilidade à substância activa ou excipientes. VM: Sem dados de segurança a longo prazo. Risco de efeitos secundários associados à LP. Dificuldades de LP em pacientes muito jovens/doentes com escoliose. Exame de plaquetas e coagulação antes e regularmente durante a terapia. Monitorização das proteínas da urina antes e regularmente durante a terapia. ECG antes de começar e regularmente durante a terapia. Possível neurotoxicidade em doses elevadas e/ou utilização a longo prazo. Em pacientes com perda de consciência, considerar a investigação para hidrocefalia. S: Não recomendado durante S. UW: Forma infantil: Infecções respiratórias, nasofaringite, infecções do tracto urinário, infecções dos ouvidos, gripe, obstipação, flatulência, perda de peso, erupções cutâneas. Posterior aparecimento de doenças: febre, dores de cabeça, vómitos, epistaxe, congestão das vias respiratórias, alergia sazonal, dores nas costas, queda. Possível redução do crescimento. Baixa incidência de anticorpos antidroga (ADA), sem impacto aparente do desenvolvimento de ADA na resposta clínica, eventos adversos ou perfil farmacocinético de nusinersen notado. Pós-marketing: infecções graves tais como meningite, hidrocefalia comunicante, meningite asséptica, hipersensibilidade (por exemplo, angioedema, urticária, erupção cutânea). IA: Nenhuma interacção com o CYP450, interacção devido à ligação competitiva de proteínas plasmáticas, efeito competitivo ou baixa inibição dos transportadores. Lista A. A informação profissional completa é publicada em www.swissmedicinfo.ch. Biogen Switzerland AG, 6340 Baar. Estado da informação: Agosto de 2019. Biogen-29360_09.2020
Biogen Switzerland AG
Neuhofstrasse 30
6340 Baar
www.biogen.ch
Biogen-128051_09.2021