Tanto para tumores de células germinativas como epiteliais dos ovários, a primeira linha de terapia é a cirurgia e a quimioterapia. Contudo, muita coisa mudou nos últimos anos, especialmente no cancro dos ovários. Assim, existe uma base de dados crescente sobre terapia de manutenção utilizando bevacizumab e/ou inibidores PARP.
Embora as abordagens oncológicas orientadas ainda não tenham sido capazes de se estabelecerem em tumores de células germinativas do ovário, estão agora estabelecidas na prática diária com inibidores PARP na terapia de manutenção de tumores epiteliais dos ovários, tendo sido aprovadas pelas autoridades. No entanto, algumas questões permanecem sem resposta, tais como a combinação e sequência ideal de ingredientes activos. Há também uma falta de comparações directas entre as diferentes substâncias. E não são apenas os agentes recentemente introduzidos que não são claros, mas também as terapias padrão de primeira linha para tumores ovarianos. Deve a operação ser adiada para uma data posterior a fim de aumentar a possibilidade de uma ressecção R0? E como poderia ser possível melhorar o tratamento de pacientes com tumores de células germinativas, tendo em conta o baixo número de casos?
Tumores de células germinativas: aprender com os homens?
Embora os tumores das células germinativas do ovário tenham um bom prognóstico após uma cirurgia bem sucedida, os estudos sobre a terapia óptima precisam de ser melhorados. Por exemplo, há poucos dados sobre o valor da radioterapia, e não é certo se a quimioterapia é realmente necessária em todos os casos, na medida em que é realizada hoje. O cenário do estudo é também escassamente povoado no cenário recorrente – apesar de um prognóstico extremamente pobre e, portanto, de uma elevadanecessidade médica . Embora sejam repetidamente publicadas descobertas interessantes sobre o tratamento de seminoma e não-seminoma em homens, estas são raras em tumores de células germinativas femininas. Uma estratégia segue portanto a abordagem de transferir os resultados do estudo de coortes masculinas ou mistas para pacientes femininas. Isto porque os tumores de células germinativas ocorrem significativamente mais frequentemente nos homens, com uma incidência de 6/100.000 por ano, do que nas mulheres, com uma incidência de 0,2/100.000/ano. Por um lado, esta abordagem é uma oportunidade, mas também comporta perigos, advertiu o Prof. Viola Heinzelmann, Chefe do Centro de Tumores Ginecológicos e Médico Chefe de Ginecologia/Oncologia Ginecológica do Hospital Universitário de Basileia, no Congresso deste ano das Sociedades Alemã, Austríaca e Suíça de Hematologia e Oncologia Médica em Berlim. Em muitos aspectos – tais como os biomarcadores disponíveis, a idade de início e as estratégias de tratamento – os tumores de células germinativas masculinas e femininas são de facto semelhantes. No entanto, existem diferenças relevantes tais como a incidência crescente no sexo masculino e a encenação.
Actualmente, a terapia de primeira linha – amplamente extrapolada a partir de dados de estudo de tumores de células germinativas masculinas – consiste em particular em cirurgia (laparotomia ou minimamente invasiva) e quimioterapia. A ruptura deve ser evitada a fim de evitar que o tumor se propague. A cirurgia de preservação da fertilidade pode ser realizada na maioria dos casos, mas recomenda-se a histerectomia e a adnexectomia após a conclusão do planeamento familiar [1]. Os doentes com disgerminoma ou teratoma IA em fase imatura apenas requerem observação pós-operatória, enquanto todos os outros doentes devem receber quimioterapia no prazo de dez dias após a cirurgia [1]. Isto tem efeitos duradouros na fertilidade e pode ser desnecessário na fase IA para todos os tumores de células germinativas – mas faltam aqui dados fiáveis.
As recidivas devem também ser removidas cirurgicamente sempre que possível. Para o tratamento de segunda linha, utiliza-se vinblastina/ifosfamida/cisplatina (VeIP) ou paclitaxel/ifosfamida/cisplatina em particular. Contudo, as abordagens curativas baseadas em carboplatina também existem com bons resultados [2]. Outras opções experimentais incluem quimioterapia de alta dose com transplante de células estaminais autólogas, BEP acelerado ou padrão (bleomicina/etoposida/platina), carboplatina/paclitaxel, e vigilância activa [3]. Há um estudo de fase II publicado em 2021 sobre a utilização de imunoterapia com inibidores de pontos de controlo, no qual não foi observado qualquer benefício com a administração de pembrolizumab [4]. Devido à elevada instabilidade genómica, as terapias orientadas para tumores de células germinativas não são uma opção, de acordo com o Prof. Heinzelmann. Mais promissor é um ensaio multicêntrico randomizado em curso comparando paclitaxel/carboplatina com bleomicina/etoposido/cisplatina no cenário recaído. Os resultados deste estudo são esperados em 2024.
No congresso deste ano da Sociedade Europeia de Oncologia Médica (ESMO), foram apresentadas duas inovações interessantes – pelo menos para os tumores de células germinativas masculinas. Assim, na fase IIA/B seminoma, parece justificar-se uma redução da intensidade da terapia para um único curso de carboplatina e radioterapia [5]. Cabazitaxel poderia também proporcionar um benefício de sobrevivência em tumores avançados de células germinativas após duas a três linhas de tratamento anteriores [6]. Se estes resultados do estudo são também aplicáveis a pacientes do sexo feminino ainda precisam de ser investigados. A radiação não faz parte da terapia padrão para as mulheres, por um lado por razões de preservação da fertilidade e, por outro lado, devido a condições anatómicas. Os ensaios aleatórios ainda não investigaram esta opção nas fêmeas. Para resolver a insuficiência da base de dados para o tratamento de tumores de células germinativas femininas, as duas redes ENGOT (Rede Europeia de Grupos de Ensaios Oncológicos Ginecológicos) e GCIS (Intergrupo Internacional do Cancro Ginecológico Cancro do Ovário) que devem coordenar e iniciar estudos importantes a fim de finalmente proporcionar clareza no caso de disgerminoma, teratoma e afins nas mulheres.
Foco na terapia de primeira linha do cancro dos ovários
Para além dos tumores das células germinativas, a reunião anual da DGHO, OeGHO, SSMO e SGH/SSH também tratou do carcinoma ovariano muito mais comum. Em particular, o foco era se a quimioterapia neoadjuvante deveria ser dada antes da cirurgia. E a terapia de manutenção com bevacizumab e/ou inibidor PARP também foi discutida. Além da cirurgia e da quimioterapia adjuvante, isto já faz parte do padrão de cuidados na primeira linha, a partir da fase III [7]. Embora os benefícios correspondentes em termos de sobrevivência sem progressão (PFS) já tenham sido demonstrados nos vários ensaios cruciais, ainda não existem dados publicados sobre a sobrevivência global no âmbito da nova terapia de manutenção recomendada.
Em princípio, a ressecção macroscopicamente completa é considerada extremamente importante em termos de prognóstico [8]. Isto é conseguido em cerca de 60% dos casos, com uma taxa mais elevada de ressecções R0 após quimioterapia neoadjuvante. Por conseguinte, é uma consideração óbvia a realização de cirurgia apenas após a quimioterapia primária ter sido concluída. No entanto, esta abordagem não parece melhorar o resultado [9,10]. De acordo com os dados actuais, a liberdade de tumores após a cirurgia primária é, portanto, superior à da cirurgia intervalada. Isto também se reflecte nas directrizes, que não prevêem a quimioterapia neoadjuvante [7]. No entanto, a sequência do tratamento só tem sido investigada até agora em tumores avançados, muitas vezes inoperantes principalmente. A questão da quimioterapia neoadjuvante permanece, portanto, actualmente sem resposta para os pacientes que são principalmente avaliados como operáveis. Por esta razão, foi lançado o estudoTRUST (Trial on Radical Upfront Surgical Therapy), que inclui doentes das fases IIIB, IIIC e IV que são avaliados como livres de tumores. A avaliação dos dados está em pleno andamento e deve finalmente esclarecer se a cirurgia intervalada poderia ser superior ao padrão de cuidados em certos casos afinal de contas. Um factor que não deve ser negligenciado aqui é a morbidez e mortalidade associadas à surteza. Os doentes com elevado risco de cirurgia deveriam ser melhor reconhecidos, segundo a Prof. Barbara Schmalfeldt, chefe do Centro Ginecológico do Cancro no Centro Médico Universitário Hamburg-Eppendorf. Estes pacientes, cerca de 10%, beneficiariam mais da quimioterapia primária, seguida de uma reavaliação da cirurgia [11–13]. No entanto, a identificação de doentes tão frágeis é um desafio. O chamado método “4 A” foi apresentado no congresso como uma abordagem, em que a idade, a albumina, a fase da doença (doença avançada) e o estado geral são tidos em conta na decisão de tratamento.
Apesar dos dados convincentes para a terapia de manutenção na primeira linha, a cirurgia e, se possível, a ressecção completa continuam a ser de grande importância – isto também foi sublinhado pelo Prof. Schmalfeldt. Assim, o PFS está fortemente dependente do remanescente tumoral, mesmo em terapia de manutenção [14].
O papel dos inibidores de PARP no cancro seroso dos ovários de alta qualidade
As inovações mais revolucionárias no tratamento do cancro dos ovários nos últimos anos dizem respeito à terapia de manutenção de primeira linha. Após a introdução do inibidor VEGF bevacizumab nesta indicação, os inibidores PARP niraparib e olaparib foram também adicionados na presença de uma mutação BRCA ou outra deficiência de recombinação homóloga (HRD). O pré-requisito para a terapia de manutenção com bevacizumab e/ou inibidor PARP é uma resposta à quimioterapia de primeira linha [15]. O benefício da inibição VEGF – em que bevacizumab é iniciado simultaneamente com a quimioterapia e continuado após o fim da quimioterapia – foi confirmado na Reunião Anual da ASCO deste ano. O prolongamento do tratamento de 15 para 30 meses, por outro lado, não trouxe qualquer benefício adicional [16]. A utilização dos inibidores PARP olaparib e niraparib em terapia de manutenção de primeira linha leva também a um benefício PFS comprovado em tumores HRD-positivos em comparação com placebo, bem como monoterapia usando bevacizumab [17]. Isto já levou a aprovações Swissmedic e correspondentes alterações às directrizes [7,15].
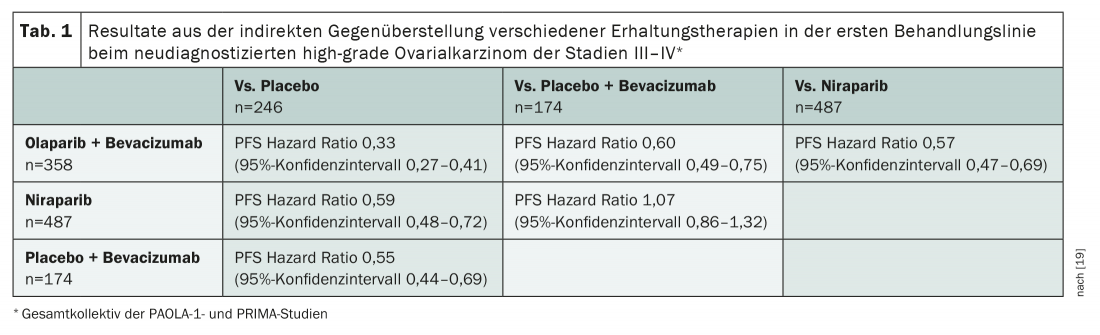
Embora o benefício dos inibidores PARP no cancro dos ovários de alta qualidade positivo para os DRH seja agora pouco controverso, há ainda algumas questões a serem respondidas sobre a sua utilização. Até agora, não há comparações directas entre as substâncias activas individuais. Além disso, a terapia de combinação com bevacizumab é sempre discutida de forma controversa. Para tal, existem duas comparações indirectas ajustadas à população, com base nos estudos de registo [18,19]. Estes são metodologicamente questionáveis – e extremamente interessantes. Por um lado, fornecem provas de que a administração simultânea de um inibidor PARP com bevacizumab tem vantagens sobre a monoterapia com inibidor PARP em termos de PFS. Esta opção também parece ter melhor desempenho em comparação com a administração de bevacizumab apenas (tab. 1) . Se não houver contra-indicação para bevacizumab, a substância deve, portanto, ser utilizada – em casos positivos para HRD complementada por um inibidor PARP. Se houver contra-indicações para bevacizumab, a terapia de manutenção só com inibição PARP pode ser iniciada após quimioterapia em pacientes com DRH positivo. Os inibidores PARP – neste caso olaparibe, niraparibe e rucaparibe – são também aprovados para o cancro de ovário recorrente sensível à platina, independentemente do estado de mutação.
Com o aumento da utilização de agentes específicos, a questão da estratégia de teste ideal está a tornar-se cada vez mais importante. Uma coisa é clara: os testes genéticos devem ser oferecidos em qualquer caso [7]. Enquanto alguns centros realizam primeiro o diagnóstico do tumor e depois o diagnóstico da linha germinal, outros preferem a abordagem oposta. Falta um padrão estabelecido.
Fonte: Simpósio Científico “Update Ovarian Tumours” presidido por Sigrun Greil-Ressler e Hans Tesch, 04.10.2021, Reunião Anual das Sociedades Alemã, Austríaca e Suíça de Hematologia e Oncologia Médica, Berlim (D).
Literatura:
- Brown J, et al: Revisão de consenso do Intergroupe Gynecologic Cancer (GCIG) para tumores de células germinativas dos ovários. Int J Gynecol Cancer. 2014; 24(9 Suppl 3): S48-54.
- De Giorgi U, et al.: Quimioterapia de salvamento em doses elevadas em pacientes do sexo feminino com tumores de células germinais recaídas/refractárias: uma análise retrospectiva do Grupo Europeu de Transplante de Sangue e Medula Óssea (EBMT). Ann Oncol. 2017; 28(8): 1910-1916.
- Uccello M, et al.: Tratamento sistémico anti-cancerígeno em tumores malignos de células germinativas dos ovários (MOGCTs): gestão actual e abordagens promissoras. Ann Transl Med. 2020; 8(24): 1713.
- Tsimberidou AM, et al: Pembrolizumab em Pacientes com Tumores Metástáticos Avançados de Células de Germes. Oncologista. 2021; 26(7): 558-e1098.
- Papachristofilou A, et al: dose única de carboplatina seguida de radioterapia de nó envolvido como tratamento curativo para seminoma fase IIA/B: Eficácia resulta do ensaio internacional fase II multicêntrico SAKK 01/10. ESMO Congress 2021, Proffered Paper Session – Genitourinary tumours, non-prostate 2, Abstract #LBA30.
- Baciarello G, et al.: Um ensaio prospectivo de fase II de cabazitaxel em pacientes do sexo masculino com tumores metastáticos de células germinativas pré-tratados com quimioterapia: o estudo CABA-GCT. ESMO Congress 2021, Mini sessão oral – Genitourinary tumours, non-prostate, Abstract #655MO.
- AWMF S3-Leitlinie: Diagnostik, Therapie und Nachsorge maligner Ovarialtumoren, Versão 5.0, Setembro de 2021.
- du Bois A, et al: Role of surgical outcome as prognostic factor in advanced epithelial ovarian cancer: a combined exploratory analysis of 3 prospectively randomized phase 3 multicenter trials: by the Arbeitsgemeinschaft Gynaekologische Onkologie Studiengruppe Ovarialkarzinom (AGO-OVAR) and the Groupe d’Investigateurs Nationaux Pour les Etudes des Cancers de l’Ovaire (GINECO). Cancro. 2009; 115(6): 1234-1244.
- Vergote I, et al: Quimioterapia neoadjuvante ou cirurgia primária na fase IIIC ou IV do cancro do ovário. N Engl J Med. 2010; 363(10): 943-953.
- Kehoe S, et al: Quimioterapia primária versus cirurgia primária para o recém-diagnosticado cancro avançado dos ovários (CORO): um ensaio aberto, randomizado, controlado e não-inferioritário. Lanceta. 2015; 386(9990): 249-257.
- Vergote I, et al.: Quimioterapia neoadjuvante no cancro ovariano avançado: Em que concordamos e discordamos? Gynecol Oncol. 2013; 128(1): 6-11.
- Aletti GD, et al: Abordagem multidisciplinar na gestão de doentes avançados com cancro nos ovários: Uma abordagem personalizada. Resultados de uma unidade especializada em cancro nos ovários. Gynecol Oncol. 2017; 144(3): 468-473.
- Ataseven B, et al.: A albumina sérica pré-operatória está associada à taxa de complicações pós-operatórias e sobrevivência global em doentes com cancro epitelial dos ovários submetidos a cirurgia citoreducativa. Gynecol Oncol. 2015; 138(3): 560-565.
- Harter P, et al: Eficácia da manutenção olaparib mais bevacizumab pelo estado de biomarcador em doentes de alto e baixo risco clínico com cancro dos ovários recentemente diagnosticado e avançado no ensaio PAOLA-1. International Journal of Gynecologic Cancer. 2020; 30: A13-A4.
- Informação sobre drogas Swissmedic: www.swissmedicinfo.ch (último acesso em 28.10.2021).
- Pfisterer J, et al.: Duração óptima do tratamento de bevacizumab (BEV) combinada com carboplatina e paclitaxel em doentes (pts) com ovário epitelial primário (EOC), trompa de falópio (FTC) ou cancro peritoneal (PPC): Um ensaio multicêntrico de 2 fases de 2 braços aleatórios ENGOT/GCIG do Grupo de Estudo AGO, GINECO, e NSGO (AGO-OVAR 17/BOOST, GINECO OV118, ENGOT Ov-15, NCT01462890). Reunião Anual ASCO 2021, Oral Abstract Session Gynecologic Cancer, Abstract #5501.
- Ray-Coquard I, et al: Olaparib mais bevacizumab como manutenção de primeira linha no cancro dos ovários. N Engl J Med. 2019; 381(25): 2416-2428.
- Vergote I, et al: Comparação indirecta ajustada da população dos estudos SOLO1 e PAOLA-1/ENGOT-ov25 de olaparib com ou sem bevacizumab, bev sozinho e placebo no tratamento de manutenção de mulheres com cancro do ovário de fase III/IV recentemente diagnosticado com mutação BRCA. Reunião Anual da SGO 2020, Resumo #35.
- Hettle R, et al: Comparação de tratamento indirecto ajustado à população (PAITC) do inibidor PARP de manutenção (PARPi) com ou sem bevacizumab versus bevacizumab em mulheres com cancro dos ovários recentemente diagnosticado (OC). Reunião Anual da ASCO 2020, Sessão de Poster sobre o Cancro Ginecológico, Resumo #6052.
InFo ONCOLOGY & HEMATOLOGY 2021; 9(6): 19-22 (publicado 7.12.21, antes da impressão).