As convulsões na terapia de primeira linha do cancro do pulmão mutado por EGFR de células não pequenas estão iminentes. Com o ensaio FLAURA, osimertinib apresenta-se, pela primeira vez com confiança, como uma opção de tratamento para pacientes inexperientes.
Dificilmente se passa uma conferência oncológica sem resultados de peso do campo do cancro do pulmão de células não pequenas (NSCLC). Não é, portanto, surpreendente que os estudos sobre o NSCLC também tenham constituído uma parte central das apresentações no congresso da OMPE deste ano. Desta vez, dizia respeito ao tratamento de primeira linha de pacientes avançados com mutações EGFR.
Breve revisão
Em 2016, InFo ONKOLOGIE & HÄMATOLOGIE relatou, como habitualmente, a Conferência Europeia sobre Cancro do Pulmão em Genebra. Nessa altura, dois resumos tardios tinham demonstrado a eficácia do osimertinibe, um potente inibidor selectivo de tirosina quinase de terceira geração (anti-EGFR), na população acima referida. Tratava-se de resultados de estudos parcialmente agrupados das fases I e II. As investigações em questão foram designadas AURA P1, extensão AURA e AURA 2. concluíram unanimemente que o osimertinib na dose de 80 mg/d em pacientes com NSCLC avançado e a mutação EGFR T790M que tinham progredido na terapia EGFR TKI prévia proporcionaram uma alta taxa de resposta durante uma duração relativamente longa, com uma sobrevivência sem progressão encorajadora e um perfil de efeito secundário controlável. Porque é que isso é importante? Agora, quando é detectada uma mutação de EGFR do condutor, que se aplica a cerca de 15% de todos os casos NSCLC no mundo ocidental e a um bom terço no mundo asiático, os inibidores específicos de tirosina quinase (TKIs) têm estado disponíveis há muito tempo com bons resultados. Contudo, estes TKIs levam ao desenvolvimento de resistência e à progressão da doença – a mutação T790M é a causa da maioria de toda a resistência. O Osimertinib como inibidor do EGFR com mutações sensibilizantes (EGFRm) e a mutação de resistência TKI T790M preenche esta lacuna e foi por isso incluído com gratidão no regime terapêutico. Assim, o osimertinib foi também aprovado na Suíça na segunda linha desde meados do ano passado.
A primeira linha como alvo
Mesmo assim, contudo, tornou-se evidente que o osimertinib também faria incursões no mercado de primeira linha. Outra apresentação no ELCC 2016 com dados positivos de 60 pacientes ingénuos da terapia sugeriu isto. Osimertinib atrasa a resistência. O tumor tem obviamente de procurar novos mecanismos de resistência para além da mutação EGFR T790M. Então o que acontece se bloquear esta “via de fuga” central para o tumor logo desde o início?
A clareza final deveria ser proporcionada por um ensaio de fase III com mais de 500 pacientes que comparavam o osimertinibe com o erlotinib e o gefitinib (“padrão de cuidados”). Os resultados eram esperados em cerca de um ano e meio – na OMPE 2017 tinha chegado o momento. Isto com muita antecedência: a apresentação foi convincente. É provável que o osimertinib em breve esteja disponível na primeira linha.
FLAURA – a história de sucesso continua
O ensaio da fase III em questão tem o nome retumbante FLAURA. O estudo envolveu 556 adultos da Ásia, Europa e América do Norte com NSCLC avançado com activação de mutações de EGFR-TK, incluindo a eliminação em exon 19 e a mutação pontual L858R no exon 21. Foram aleatorizados na primeira linha para receber o “padrão de cuidados”, que é o gefitinib 250 mg/d ou erlotinib 150 mg/d foi definido, ou osimertinib 80 mg/d. O crossover ao osimertinib foi possível em progressão e resistência T790M. As características básicas dos pacientes, tais como o estatuto de mutação, género, metástases do SNC e etnia (asiática, não asiática) foram distribuídas uniformemente pelas armas.
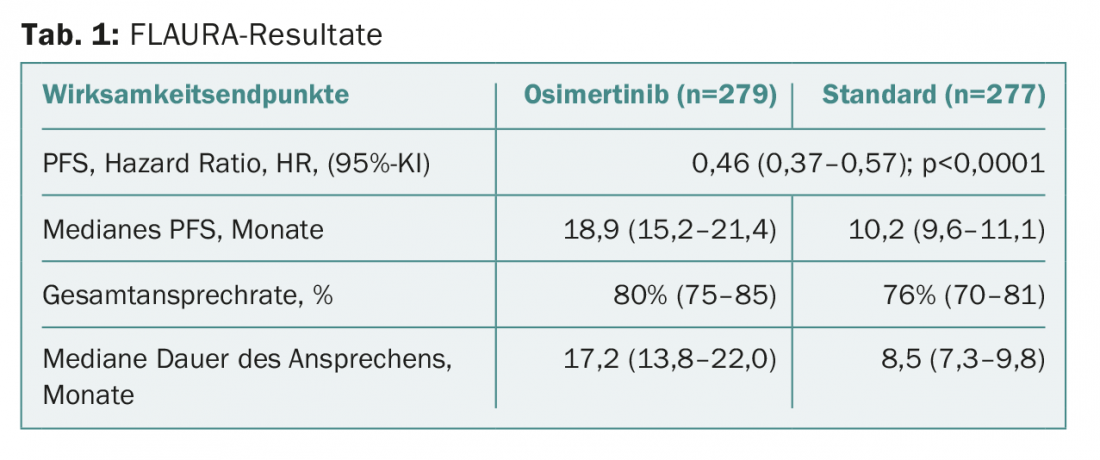
O ponto final primário, sobrevivência sem progressão, foi prolongado para 18,9 meses com a substância em estudo em comparação com 10,2 meses com a terapia padrão. Isto corresponde a uma redução do risco clínica e estatisticamente significativa em mais de metade. Os valores são apresentados no quadro 1 . O benefício foi observado em todos os subgrupos predefinidos (incluindo pacientes com/sem metástases cerebrais na linha de base). Uma análise final correspondente sobre a sobrevivência global ainda está actualmente pendente. A análise intercalar ainda não tinha revelado quaisquer valores estatisticamente significativos. Nesta fase inicial, os dados ainda são “imaturos”. Por conseguinte, ainda não é possível fazer uma declaração conclusiva a este respeito. A duração da resposta foi duplicada com osimertinib.
Os acontecimentos adversos mais frequentes com o osimertinibe foram – como já era conhecido de estudos anteriores – diarreia (58%, em 2% pelo menos grau 3) ou pele seca (32%). Em geral, os acontecimentos adversos de qualquer causa eram igualmente frequentes nos dois braços. Os casos graves ocorreram mais frequentemente sob terapia padrão (que incidentalmente também se aplicou à taxa de descontinuação da terapia correspondente: 13% vs. 18%). Globalmente, o osimertinib tem, portanto, um melhor desempenho em termos de segurança.
Estão todos de acordo?
Os autores inferem dos dados um perfil de risco-benefício superior para o osimertinib na definição da primeira linha. O perfil de segurança foi claramente melhor apesar da duração global mais longa do tratamento com a substância em estudo (16,2 meses). O facto de o benefício em PFS com/sem metástases cerebrais ser quase o mesmo (HR 0,47 e 0,46) sugere que o osimertinib está activo tanto no cérebro como sistemicamente. Isto é particularmente importante para tumores alterados por EGFR, uma vez que estes ocorrem frequentemente com metástases cerebrais. Os resultados da actividade cerebral são apoiados pela descoberta de que 6% no grupo osimertinib mas 15% no grupo padrão desenvolveram a progressão do SNC. Também foi digno de nota que as curvas PFS divergiram significativamente desde muito cedo e continuaram a divergir claramente durante o curso. O desenvolvimento na sobrevivência global também parece promissor. Por isso, parece uma mudança de paradigma.

A resposta dos peritos e dos visitantes à conferência foi igualmente positiva? Na sua maioria, sim. A relevância para a primeira linha foi claramente concedida à FLAURA. Foram feitas comparações com a situação em tumores com mutação ALK e o estudo correspondente sobre o alectinibe – recentemente publicado no NEJM [1]. Também aí a questão era se a utilização na primeira linha era superior à sequenciação das substâncias activas. Especificamente, isto significa que um PFS mais longo é conseguido com o segundo agente original na primeira linha do que seria possível com sequenciação. Contudo, embora a situação para a ALK seja muito clara, a situação para a FLAURA é um pouco mais complexa. Isto porque apenas cerca de metade da população do estudo da FLAURA teria precisado e beneficiado do osimertinib na segunda linha após a terapia de primeira linha com os agentes estabelecidos (uma vez que teriam desenvolvido resistência via T790M). Dado que o estudo também inclui um grande número de pacientes que nunca teriam desenvolvido tal resistência, mas sim um tipo diferente de resistência, não se esperaria uma PFS mediana de 19 meses. Períodos tão longos só são normalmente atingidos com pacientes que são adequados para a sequenciação de osimertinibe (isto não é estatisticamente verdade para cerca de 50% da população da FLAURA). Para todos os outros, podem ser assumidos períodos mais curtos, pois muitas vezes só podem mudar para a quimioterapia após a terapia de primeira linha. Tendo isto em conta, 19 meses de sobrevivência sem progressão é impressionante e, na verdade, defende a utilização da primeira linha nesta população. Em particular, porque nunca é certo se é sequer possível mudar para o osimertinib ou outra terapia específica de segunda linha – uma vez que permanece pouco claro no início da terapia inicial se os pacientes desenvolverão resistência como o T790M e assim beneficiarão dos agentes específicos – os 19 meses com o osimertinib que podem ser alcançados com antecedência podem facilitar a decisão de o utilizar na primeira linha. Livremente de acordo com o princípio: “o vencedor leva tudo”.
No entanto, pode não ser assim tão simples afinal. Neste contexto, o desenvolvimento futuro do OS na FLAURA é também importante. A última palavra ainda não foi dita para tumores mutantes de EGFR.
Fonte: Congresso da Sociedade Europeia de Oncologia Médica (ESMO) 2017, 8-12 Setembro 2017, Madrid
Literatura:
- Peters S, et al: Alectinib versus crizotinib em Câncer de Pulmão Não-Positivo de Pequenas-Células ALK não tratado. N Engl J Med 2017; 377: 829-838.
- Eggermont AM, et al: Sobrevivência prolongada no melanoma de fase III com terapia adjuvante de ipilimumab. NEJM 2016; 375: 1845-1855.
- Weber J, et al: Adjuvant Nivolumab versus Ipilimumab em Resected Stage III ou IV Melanoma. NEJM 2017 10 de Setembro. DOI: 10.1056/NEJMoa1709030 [Epub ahead of Print].
- Long GV, et al: Adjuvant dabrafenib mais trametinib na fase III melanoma modificado por BRAF. NEJM 2017 10 de Setembro. DOI: 10.1056/NEJMoa1708539 [Epub ahead of print].
InFo ONCOLOGY 2017; 5(5): 35-37











