A prevalência crescente de insuficiência cardíaca é um problema médico e económico importante. O número de doentes a serem tratados no hospital por insuficiência cardíaca tem vindo a aumentar há anos. O quadro clínico da insuficiência cardíaca é complexo. Os sintomas típicos incluem dispneia, redução do desempenho, fadiga e retenção de líquidos.
A prevalência crescente da insuficiência cardíaca é um problema médico e económico importante [1]. O número de doentes a serem tratados no hospital por insuficiência cardíaca tem vindo a aumentar há anos. Os custos associados para o sistema de saúde são elevados [1,2].
A insuficiência cardíaca é definida como a incapacidade do coração de fornecer ao organismo sangue e oxigénio suficientes para assegurar um metabolismo estável em condições de repouso e de esforço. O quadro clínico da insuficiência cardíaca é complexo. Os sintomas típicos incluem dispneia, redução do desempenho, fadiga e retenção de líquidos [1,2].
As recomendações actuais do ESC diferenciam entre insuficiência cardíaca com fracção de ejecção ventricular esquerda reduzida (HFrEF; EF 50%) [1]. Cada uma destas três categorias de insuficiência cardíaca está associada a um mau prognóstico com aumento da morbidade e mortalidade [1,2].
Insuficiência cardíaca com fração de ejeção ventricular esquerda reduzida (HFrEF)
Apesar do enorme progresso com uma vasta gama de opções terapêuticas em farmacologia e terapia de dispositivos (CID, CRT) para procedimentos intervencionais ou cirúrgicos (Mitra clip, VAD), o prognóstico dos pacientes com HFrEF continua pobre [1]. Durante um seguimento mediano de 47 meses, a mortalidade foi de 32% em doentes com HFrEF com LV-EF de 35-50%. Com um LV-EF <35%, a mortalidade aumentou para 41% [1–3].
A capacidade de exercício cardiopulmonar, medida pela absorção máxima de oxigénio na espiroergometria (pico VO2 ml/min-1/kg-1) é significativamente reduzida em doentes com HFrEF. É inferior nas mulheres do que nos homens e diminui ainda mais significativamente na velhice e após a descompensação [3].
O pico de VO2 é considerado um preditor significativo de mortalidade por todas as causas [3] e um pico de VO2 inferior a 1 ml/min-1/kg-1 está associado a uma mortalidade por todas as causas 16% mais elevada [3]. As causas da reduzida capacidade de exercício em HFrEF incluem redução da função da bomba ventricular esquerda, redução da capacidade pulmonar causada por disfunção cardíaca, e acentuada descondicionamento do músculo esquelético periférico com massa muscular reduzida [1,3]. A sarcopenia (desperdício muscular) está presente em 30-50% dos doentes com HFrEF [3]. Além disso, a falta de adaptação do ritmo cardíaco (incompetência cronotrópica) e o insuficiente fluxo sanguíneo à musculatura periférica devido à vasoconstrição periférica em neuroendócrina e sobreestimulação simpaticotónica podem, adicionalmente, limitar o desempenho físico.
Insuficiência cardíaca com fração de ejeção ventricular esquerda preservada (HFpEF)
A fisiopatologia da insuficiência cardíaca com FEV-EF preservada (HFpEF) é complexa, heterogénea e ainda não totalmente compreendida [2]. HFpEf está frequentemente associado a comorbidades tais como diabetes mellitus e hipertensão. O foco inicial é uma perturbação de enchimento do ventrículo esquerdo (disfunção diastólica), geralmente com hipertrofia ventricular esquerda e função da bomba inicialmente preservada. Os distúrbios microvasculares podem levar a lesões do miocárdio e a uma redução da função sistólica do ventrículo esquerdo [2]. Para além dos sintomas clínicos (dispneia, redução do desempenho, retenção de líquidos), HFpEF é definida pelo LV-EF [1,4]%, péptidos natriuréticos elevados (BNP >35 pg/ml, NT-proBNP >125 pg/ml) e evidência ecocardiográfica de doença cardíaca estrutural (hipertrofia ventricular esquerda, aumento do átrio esquerdo) ou disfunção diastólica . A proporção de pacientes com HFpEF na população total de insuficiência cardíaca é suposta ser de cerca de 50%. O prognóstico destes pacientes é comparativamente pobre ao dos pacientes com HFrEF [1,4]. Ao contrário do HFrEF, a terapia farmacológica dos pacientes com HFpEF não está assegurada. A morbilidade e mortalidade de pacientes com HFpEF não pôde ser reduzida pela farmacoterapia baseada na terapia de HFrEF até agora [1,4]. Isto torna a prevenção e tratamento dos factores de risco cardiovascular e comorbidades em HFpEF proporcionalmente ainda mais importante.
Os pacientes com HFpEF tendem a ser mais velhos, mais frequentemente do sexo feminino, mais propensos a ter diabetes tipo 2 e/ou hipertensão, e têm mais comorbilidades. Estes pacientes são frequentemente altamente sintomáticos, a sua resiliência física na vida quotidiana é severamente limitada e a sua qualidade de vida é significativamente reduzida como resultado [1,3,4], apesar do LV-EF normal! Estudos recentes mostram que a insuficiência cardíaca em doentes com FEFH está associada a mecanismos de adaptação periféricos comparáveis aos dos doentes com FEFH, ou seja, a uma acentuada descondicionamento dos músculos esqueléticos e a uma redução da massa muscular periférica [6].
Nos doentes com HFpEF, a redução da capacidade de exercício está associada a um aumento significativo da morbilidade e mortalidade [3]. No entanto, estudos iniciais mostram que a melhoria do desempenho físico estava também associada a uma diminuição da mortalidade por todas as causas [5]. Tendo em conta este contexto e a farmacoterapia não comprovada, a formação física é de extrema importância na terapia de pacientes com HFpEF [1,4].
Actividade física e exercício em insuficiência cardíaca (HFrEF e HFpEF)
Como consequência da insuficiência cardíaca com dispneia por esforço, fadiga e exaustão, a prevalência de inactividade física prolongada é muito elevada nesta população [3]. Intervenções de treino adaptadas individualmente podem contrariar eficazmente o descondicionamento dos músculos esqueléticos com os seus efeitos negativos nas actividades da vida diária. Desta forma, a actividade física regular pode ser altamente eficaz na estabilização do desempenho físico e na melhoria da qualidade de vida dos doentes com HFrEF e HFpEF [3].
Durante décadas, o treino físico na terapia de pacientes com HFrEF tem sido investigado em muitos estudos e avaliado em revisões sistemáticas e meta-análises. Estas confirmam consistentemente a segurança e a elevada eficácia das intervenções de formação em doentes com HFrEF [3]. Só nos últimos anos é que a formação física em pacientes com HFpEF se tornou o foco da atenção científica. Os estudos confirmam igualmente a segurança e eficácia da formação adaptada neste grupo de doentes [3].
Os resultados destes estudos e meta-análises demonstram uma melhoria significativa da qualidade de vida, bem como do desempenho cardiopulmonar e da mobilidade na vida quotidiana (por exemplo, no teste de caminhada de 6 minutos) [3]. A participação em programas de reabilitação baseados no exercício também reduziu significativamente a taxa de hospitalização devido ao agravamento da insuficiência cardíaca. No entanto, não foi possível demonstrar uma redução da mortalidade através da intervenção de formação em nenhuma das actuais meta-análises [3]. Por conseguinte, as actuais directrizes das sociedades profissionais recomendam a utilização de formação física adaptada individualmente para todos os doentes com insuficiência cardíaca clinicamente estável com HFrEF e HFpEF, e isto para todos os grupos etários [1,3].
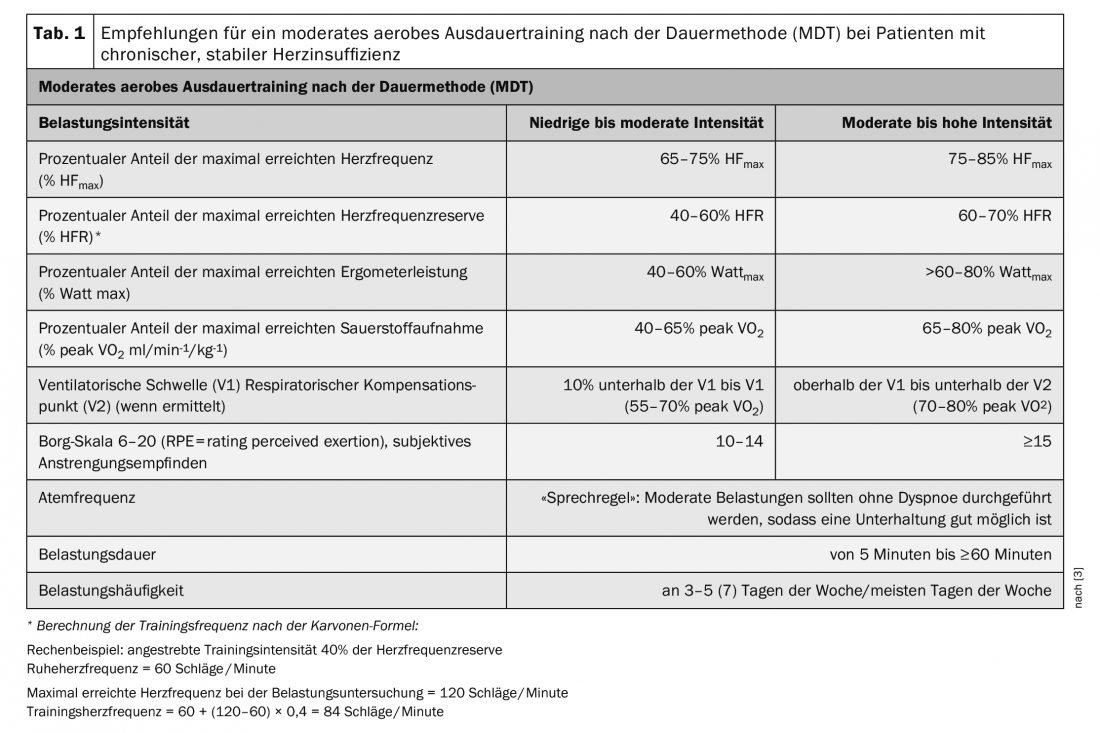
Os doentes com insuficiência cardíaca crónica estável devem ser basicamente classificados como doentes de risco acrescido. Os pré-requisitos para iniciar uma intervenção de exercício são, portanto, a estabilidade clínica, bem como a optimização de medicamentos, dispositivos ou terapia intervencionista. A isquemia e a arritmia miocárdica induzidas pelo exercício, bem como a exsiccose ou a hipervolémia devem ser excluídas antes de se iniciar o exercício [3]. As recomendações de formação devem ser sempre feitas com base numa estratificação completa do risco, incluindo um teste de stress. O teste de exercício preferido é a espiroergometria com exercício submaximal, se necessário em cooperação com uma prática devidamente equipada [3]. Os resultados permitem uma avaliação da tolerância ao exercício individual e uma prescrição de formas e intensidades de treino adaptadas. As recomendações de formação estabelecidas nas directrizes (Tab. 1-3) fornecem “corredores” para os limites inferior e superior entre os quais a formação é segura e eficaz. As recomendações individuais de formação devem situar-se dentro destes limites.
A formação deve ser iniciada no âmbito de programas estruturados orientados pelo terapeuta especializado e supervisionados por um médico. Todas as medidas de formação devem ser continuadas a longo prazo, por exemplo, em grupos de insuficiência cardíaca em regime ambulatório. Os pacientes clinicamente estáveis e treinados podem também fazer a formação em casa. No âmbito dos programas de formação orientada, o doente deve ser informado sobre a importância da actividade física regular no curso da doença e receber aconselhamento para uma rotina diária e de lazer mais activa. A monitorização e supervisão inicial da formação por profissionais é importante para que os pacientes possam avaliar correctamente os seus sintomas que possam ocorrer durante a formação e reconhecer a sua relevância para a continuação da formação. Desta forma, os pacientes aprendem a avaliar realisticamente a sua resiliência e os seus limites de stress também na vida quotidiana [3].
Formação aeróbica moderada de resistência de acordo com o método de resistência (MDT)
Os efeitos mais estudados são os do treino de resistência aeróbica moderada utilizando o método de duração (MDT). Esta forma de treino influencia a progressão e sintomatologia do HFrEF de muitas maneiras. Os efeitos bem documentados incluem uma influência positiva na função autonómica do coração com uma redução na activação simpática, melhoria da função endotelial, redução da pós-carga cardíaca, melhoria da FEV-EF, redução do tamanho do ventrículo esquerdo e melhoria da capacidade oxidativa dos músculos esqueléticos [3]. Os resultados das meta-análises confirmam a melhoria significativa da capacidade de exercício cardiopulmonar (+2,82 a +3,10 ml/min-1/kg-1) através do treino de endurance aeróbico. As maiores intensidades de formação estão associadas a maiores melhorias [3]. Os resultados de um estudo recentemente publicado fornecem provas da eficácia do treino em doentes com FHF, independentemente do desempenho cardiopulmonar no início do treino [3]. Isto significa que mesmo os pacientes mais fracos beneficiam! Um aumento significativo do pico de VO2 do treino físico foi associado a uma redução de risco de 81% para o parâmetro primário de admissão hospitalar e/ou mortalidade em pacientes com um pico de VO2 elevado e uma redução de risco de 59% em pacientes com um VO2 baixo [3]. Estes resultados apoiam a relevância do aumento do pico de VO2 através de formação adaptada em pacientes com HFrEF.
Em doentes com HFpEF, os resultados de uma meta-análise recentemente publicada de estudos sobre a eficácia de uma MDT mostram um aumento significativo no desempenho cardiopulmonar (+1,67 ml/min-1/kg-1), mobilidade (6MWD: +33,9 m) e qualidade de vida. A MDT, por outro lado, não demonstrou ter um efeito positivo sobre a função diastólica ou LV-EF [7].
O treino aeróbico moderado de resistência de acordo com o método de resistência (MDT) é portanto recomendado como treino básico para todos os grupos de pacientes. Após o teste de stress no ergómetro da bicicleta, a potência máxima (Wattmax) e a frequência cardíaca (HFmax) atingida pode ser utilizada para determinar a carga individual de treino. Uma percentagem da HRmax ou da reserva de frequência cardíaca (HFR) é dada como recomendação de formação. O controlo do exercício como percentagem do HFR é recomendado para a incompetência cronotrópica e, quando apropriado, para a terapia com bloqueador beta-receptor. A indicação em percentagem de Wattmax é útil para doentes para os quais a FC não pode ser utilizada para controlo de treino, por exemplo, fibrilação atrial. Como apoio ou alternativa, o sentimento subjectivo de esforço através da escala de Borg, bem como a frequência respiratória, podem ser utilizados para controlo de carga [3] (Tab. 1).
Após os testes espiroergométricos, a recomendação de formação pode ser dada como uma percentagem do pico de VO2. A determinação dos limiares ventilatórios (VT) e do ponto de compensação respiratória (VT2) permite uma avaliação objectiva do desempenho aeróbico e um controlo de treino mais direccionado [3].
O treino aeróbico de resistência deve ser inicialmente incorporado sob a forma de curtos períodos de exercício (5-10 minutos ≥2 vezes/semana) com intensidade baixa a moderada (40-50% de pico VO2, 40% HFR, escala 10 de Borg). Com boa tolerância ao exercício, recomenda-se primeiro aumentar a frequência do treino (≥5 vezes/semana, de preferência diariamente) e prolongar a duração do exercício (20-30 minutos). Esta abordagem cautelosa é muito importante especialmente para pacientes descondicionados e pouco resilientes no início da formação. Os pacientes com boa tolerância ao exercício devem ser gradualmente introduzidos a exercícios de resistência mais intensivos de uma forma adaptada individualmente [3] (Quadro 1).
Formação de resistência de acordo com o método de intervalo
A formação segundo o método de intervalo é caracterizada por uma alternância constante de curtos períodos de esforço e de recuperação. Esta forma de treino permite manter repetidamente uma intensidade mais elevada a muito elevada durante as fases de carga. A eficácia a curto prazo e a segurança do treino intervalado em doentes com insuficiência cardíaca está agora bem estudada. A discussão científica centra-se no treino intensivo a intervalo de alta intensidade. Isto é definido como repetições curtas (≤45 s) a longas (2-4 min), de exercícios de intensidade alta a muito alta, mas não máxima (≥90% pico de VO2) alternando com os exercícios de recuperação de intensidade moderada a baixa.
Formação em intervalo com fases curtas de carga intensiva (IT)
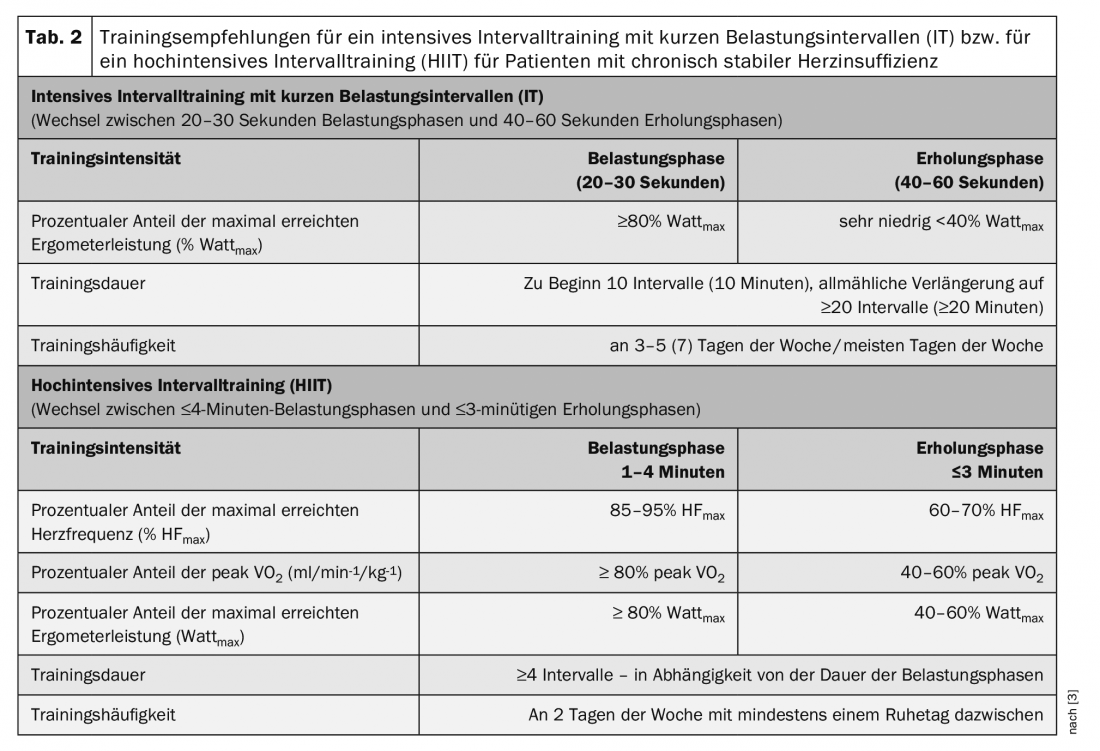
O treino intervalado com períodos curtos de exercício intenso (20-30 segundos) alternando com períodos de recuperação (40-60 segundos) (IT) duas vezes mais longos (Tabela 2 ) leva a melhorias comparáveis no desempenho e mobilidade cardiopulmonar como a MDT em pacientes com HFrEF [3].
Este treino intervalado é geralmente muito bem tolerado por doentes com insuficiência cardíaca crónica estável e é considerado adequado e seguro para todos os grupos de doentes. É rotineiramente utilizado em muitos programas de reabilitação cardíaca. Pode ser feito como uma alternativa ou complementar à MDT. A utilização de TI é particularmente recomendada para doentes idosos e/ou particularmente descondicionados com fraca força muscular, bem como para doentes que sofrem de comorbilidades, tais como doenças circulatórias periféricas das pernas e/ou doenças pulmonares obstrutivas crónicas [3]. Uma TI deve ser sempre utilizada quando os pacientes não podem tolerar vários minutos de exercício contínuo (dispneia ou muscular).
Formação em intervalo com longos períodos de exercício de alta intensidade (HIIT)
Um protocolo com longas fases de carregamento que é frequentemente utilizado é o chamado protocolo 4×4. Após uma curta fase de aquecimento com intensidade moderada (60% HRmax), quatro intervalos de carga de 4 minutos (85-95% HRmax) alternam com fases de recuperação de 3 minutos (60-70% HRmax). Os resultados sobre a eficácia e adequação deste treino de intervalo de alta intensidade (HIIT) para pacientes com HFrEF ainda são controversos. Os resultados das meta-análises mostram uma maior eficácia do HIIT na melhoria do pico de VO2 em comparação com o MDT (+0,73 a +2,13 ml/min-1/kg-1). No entanto, esta superioridade do HIIT não pôde ser confirmada num grande RCT multicêntrico prospectivo [8]. Os resultados deste estudo demonstram uma eficácia comparável de HIIT e MDT com aumentos significativos no pico de VO2 (HIIT +1,4 vs. MDT +1,8 ml/min-1/kg-1), sem diferenças significativas entre os dois grupos de treino. HIIT não teve uma influência positiva no tamanho LV-EF ou LV [8]. Durante a intervenção de formação, os acontecimentos adversos foram igualmente distribuídos em ambos os grupos. No entanto, durante o período de acompanhamento de 52 semanas, houve uma tendência não significativa para mais acontecimentos adversos não fatais e fatais no grupo HIIT [8]. Além disso, vários autores relatam que muitos pacientes têm problemas em atingir a intensidade de exercício muito elevada desejada durante a HIIT ou em mantê-la durante a fase de exercício.
Os resultados deste estudo levaram a que a formação em intervalos de alta intensidade (HIIT) não seja actualmente totalmente recomendada para doentes com HFrEF. Esta forma de treino deve antes ser considerada no curso de longo prazo da terapia de treino em pacientes estáveis com boa tolerância ao exercício, se necessário em adição à MDT, ou HIIT deve ser realizada alternadamente com fases de exercício mais curtas e possivelmente menos intensivas [3] (Tab. 2).
Para pacientes com HFpEF, uma meta-análise recentemente publicada demonstrou a segurança, boa tolerância e eficácia do HIIT para aumentar o pico de VO2. Se este método de treino é mais eficaz na melhoria do pico de VO2 em comparação com o MDT ainda não está claro. Quando os protocolos de treino isocalórico são comparados num estudo, a eficácia de ambos os métodos é comparável [9].
Em resumo, o método de treino intervalado oferece muitas possibilidades de desenho. Pode ser adaptado às necessidades individuais através da duração e intensidade do exercício e dos intervalos de recuperação, bem como da relação entre o exercício e a recuperação [3]. Para todos os protocolos de treino de resistência, o treino num ergómetro de bicicleta (de preferência com monitorização de ECG) oferece a vantagem do alívio do peso corporal, a dosabilidade exacta e a reprodutibilidade da carga. Como alternativa ou complemento ao treino no ergómetro de bicicleta, o treino de resistência aeróbica pode ser realizado sob a forma de caminhada e/ou caminhada (caminhada rápida com aumento do uso dos braços) ou caminhada com o uso de postes (caminhada nórdica) numa pista de nível firme, em cross-trainer ou numa passadeira [3].
Treino dinâmico da força
Os benefícios e a segurança do treino de força dinâmica moderada em pacientes com insuficiência cardíaca são bem estudados. O treino de força não tem qualquer efeito negativo na função sistólica do coração. A resposta hemodinâmica central à carga de força dinâmica moderada é comparável à do treino de resistência aeróbica [3].
Como uma forma autónoma de treino, o treino de força em pacientes com HFrEF leva a uma melhoria da força muscular e contraria a perda de massa muscular causada pela doença. Tem também uma influência positiva na mobilidade, desempenho cardiopulmonar e qualidade de vida [3]. Além disso, o treino dinâmico de força é adequado como prevenção de quedas.
Em pacientes com HFrEF, a combinação do treino de força e resistência leva a um maior aumento do desempenho cardiopulmonar (+2,48 ml/min-1/kg-1) e da mobilidade (+50,05 m) em comparação com o treino de resistência apenas [3].
Em pacientes com HFpEF, três meses de treino combinado de resistência aeróbica (MDT: 50-70% pico VO2) em combinação com treino de força dinâmica moderada (50-60% “1-repetição máxima” [1RM]) produziram um aumento significativo no pico VO2 (+3,3 ml/min-1/kg-1) e uma melhoria na função diastólica determinada ecocardiograficamente em comparação com um grupo de controlo não activo [10].
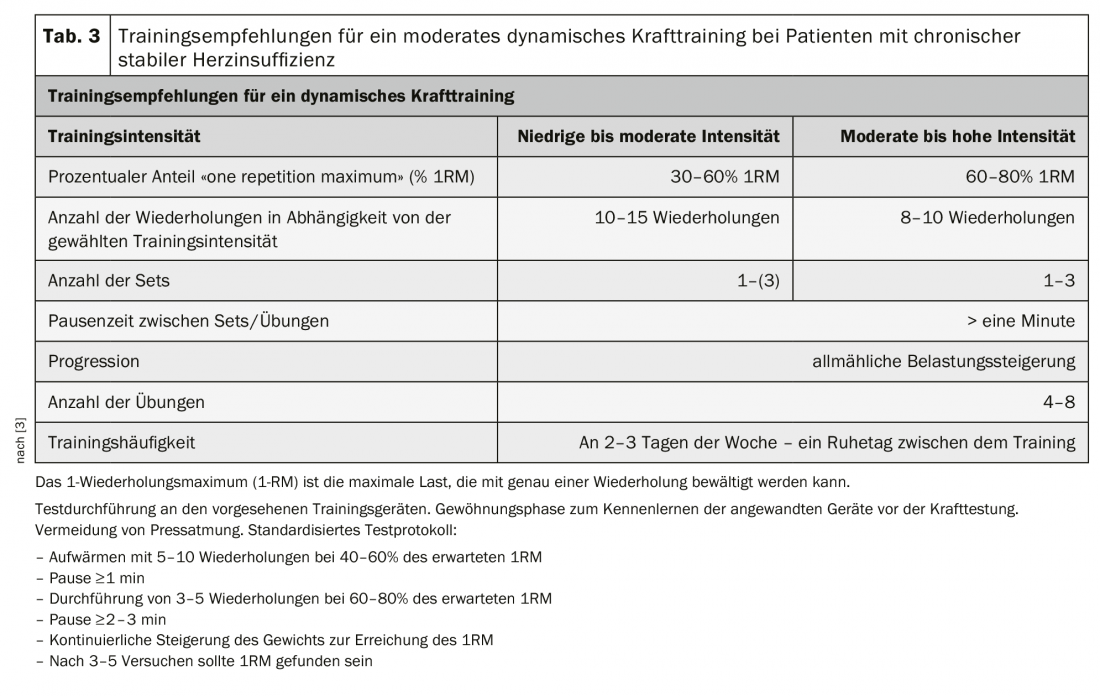
O treino de força dinâmica com intensidade baixa a moderada e uma componente isométrica baixa é portanto recomendado como complemento ao treino de resistência aeróbica tanto em pacientes com HFrEF como com HFpEF [3]. Uma introdução suave ao treino de força com intensidade muito baixa, baixo número de repetições e velocidade de movimento lenta serve para aprender e praticar a execução correcta do exercício e a respiração. Deve ser evitada a todo o custo a respiração pressionada com os lábios fechados. Os pacientes devem inspirar e expirar lentamente com a boca aberta ao ritmo do movimento. O treino de força deve ser iniciado com uma carga baixa a moderada <30-50 1RM. Com uma boa tolerância ao exercício, a intensidade pode ser gradualmente aumentada individualmente no decurso do programa de treino [3] (Tab. 3).
Literatura:
- Ponikowski P, Voors AA, Anker SD, et al.: 2016 ESC Guidelines for the diagnosis and treatment of acute and chronic heart failure: The Task Force for the diagnosis and treatment of acute and chronic heart failure of the European Society of Cardiology (ESC). Desenvolvido com a contribuição especial da Associação da Insuficiência Cardíaca (HFA) do CES. Eur J Heart Fail 2016; 18: 891-975.
- Associação Médica Alemã (BÄK), Associação Nacional de Médicos de Seguros de Saúde (KBV), Associação das Sociedades Médicas Científicas (AWMF). Orientação nacional sobre insuficiência cardíaca crónica – versão longa, 3ª edição. Versão 2. 2019 [citada: 17-06-2020]; doi: 10.6101/AZQ/000467. www.herzinsuffizienz.versorgungsleitlinien.de.
- S3 – Guideline on cardiac rehabilitation (LL-KardReha) in German-speaking Europe, Germany, Austria, Switzerland (D-A-CH), Long version – Part 1, 2019; AWMF Register number: 133/001, www.awmf.org.
- Tschöpe C, Birner C, Böhm M, et al.: Insuficiência cardíaca com fracção de ejecção preservada: gestão actual e estratégias futuras: Parecer de peritos em nome do Núcleo do “Grupo de Trabalho de Insuficiência Cardíaca” da Sociedade Alemã de Cardiologia (DKG). Clin Res Cardiol 2018; 107: 1-19.
- Orimoloye OA, Kambhampati S, Hicks AJ, et al: A aptidão cardiorrespiratória superior prevê a sobrevivência a longo prazo em pacientes com insuficiência cardíaca e fração de ejeção preservada: o Projeto Henry Ford Exercise Testing (FIT). Arch Med Sci 2019; 15: 350-358.
- Tucker WJ, Haykowsky MJ, Seo Y, et al: Impaired Exercise Tolerance in Heart Failure: Role of Skeletal Muscle Morphology and Function. Curr Heart Fail Rep 2018; 15: 323-331.
- Fukuta H, Goto T, Wakami K, et al: Efeitos do treino físico na função cardíaca, capacidade de exercício, e qualidade de vida na insuficiência cardíaca com fração de ejeção preservada: uma meta-análise de ensaios controlados aleatorizados. Heart Fail Rev 2019; 24: 535-547.
- Ellingsen Ø, Hall M, Conraads V, et al: Treino de alta intensidade de intervalo em pacientes com insuficiência cardíaca com fracção de ejecção reduzida. Circulação 2017; 135: 839-849.
- Gomes Neto M, Durães AR, Conceição LSR, et al: Treino intervalado de alta intensidade versus treino contínuo de intensidade moderada sobre capacidade de exercício e qualidade de vida em doentes com insuficiência cardíaca com fracção de ejecção reduzida: Uma revisão sistemática e meta-análise. Int J Cardiol 2018; 261: 134-141.
- Edelmann F, Gelbrich G, Düngen HD, et al: O treino de exercício melhora a capacidade de exercício e a função diastólica em pacientes com insuficiência cardíaca com fracção de ejecção preservada: resultados do estudo piloto do Ex-DHF (Exercise training in Diastolic Heart Failure). J Am Coll Cardiol 2011; 58: 1780-1791.
CARDIOVASC 2021; 20(2): 11-16