A excisão cirúrgica é ainda considerada a primeira escolha, mas novas descobertas atestam também um papel importante para o imiquimod na terapia desta perigosa mudança cancerígena da pele.
79-83% de todos os tumores de melanoma in situ são lentigo maligno (LM) [1]. Nos últimos anos, o número de novos casos deste subtipo de melanoma pré-invasivo tem aumentado acentuadamente. A taxa de incidência normalizada de tumores melanocíticos em geral aumentou mais de cinco vezes na Europa Central ao longo dos últimos cinquenta anos [1–3].
Alternativa ou complementar à excisão
A probabilidade de um lentigo maligno (LMM) se transformar num melanoma lentigo maligno (LMM) se não for tratado é relativamente alta. Um estudo publicado em 2019 examinou lesões de 682 pacientes e concluiu que o risco estimado de progressão da LMM para a LMM era de 3,5% por ano [4]. A remoção cirúrgica é ainda a primeira opção terapêutica, mas agora existem também opções de tratamento alternativas. De acordo com as directrizes NCCN, estas incluem a radioterapia ou terapia tópica com imiquimod [5]. Os dados actuais a longo prazo sobre a utilização de imiquimod em LM fora da rotulagem confirmam uma autorização de 72% para o período de seguimento de 4,1 anos (n=33) [6]. A duração do tratamento foi de 6 semanas, a frequência da terapia foi de 5 dias por semana.
Isto replicou os resultados de um estudo publicado em 2015, no qual foi alcançada uma taxa de aprovação de 86,2% [7]. Imiquimod tem também um registo terapêutico positivo como neoadjuvante antes da excisão cirúrgica: Num grande estudo que incluiu 345 biópsias excisadas, a taxa de recorrência foi de 3,9% num período de seguimento de 5,5 anos, e o tempo médio de recorrência foi de 4,3 anos [8]. O tratamento com creme Imiquimod 5% foi dado durante um período de 2-3 meses em 5 dias por semana. Em combinação com o tazaroteno, não houve recidiva após um período de seguimento de 3,5 anos [8].
Diagnosticar um “desafio
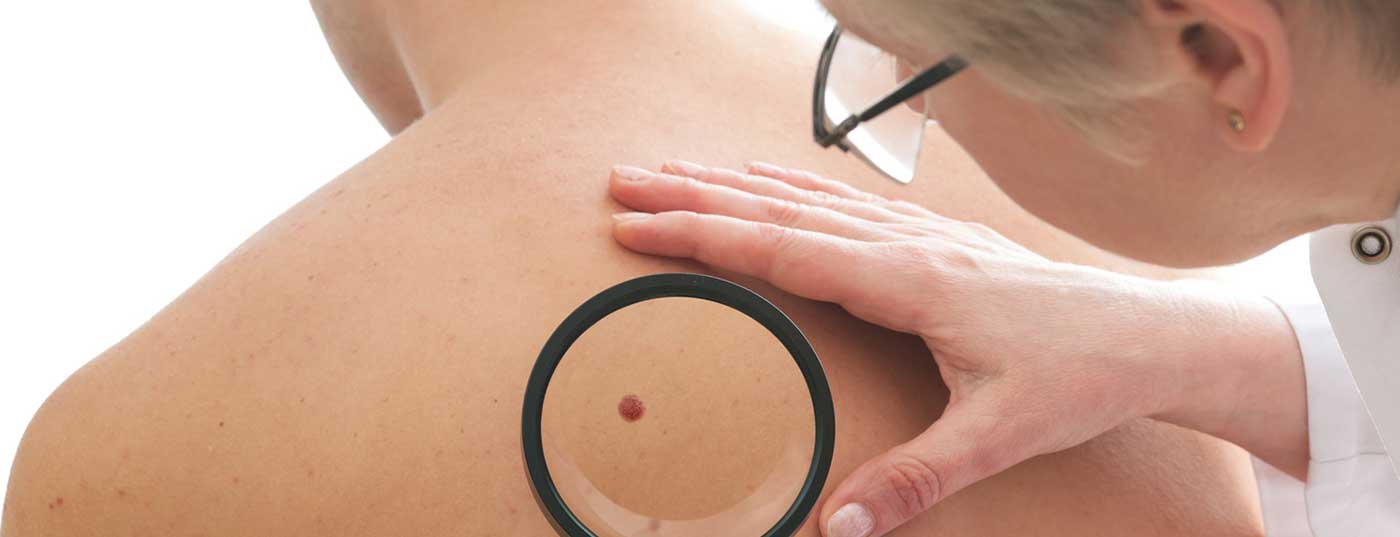
Lentigo maligna é predominantemente encontrado em pele actinicamente danificada em áreas expostas à luz, tais como o rosto, pescoço, antebraços, mãos e pernas inferiores. Como parte exposta ao sol do corpo, a face é um local comum de localização, com cerca de metade dos LM localizados na zona superior do corpo, de acordo com um estudo publicado em 2018 [1,2,9]. A regra ABCDE da dermoscopia não deve ser utilizada na face [1,2]. Como é que a mudança de pele se manifesta clinicamente? As características são inomogéneas, castanhas a negras, focos planos borrados de diferentes tamanhos. Se pelo menos uma das seguintes características de lesões não melanocíticas não for preenchida, deve ser realizada uma biopsia [10]: 1) escalas, 2) folículos brancos, 3) eritema, 4) linhas reticulares ou curvas, 5) cor castanha sem estrutura, 6) demarcação nítida, 7) quistos semelhantes a milia.
Uma biópsia incisional deve ser feita no site clinicamente mais espesso [1]. Aproximadamente 9% das LMM detectadas por biopsia são re-categorizadas como LMM ou melanoma após a excisão completa [11]. A microscopia de reflexão confocal (RCM) é particularmente útil para delinear as margens laterais da LM, bem como para monitorizar lesões não tratadas cirurgicamente e evitar a excisão desnecessária de tumores benignos [1]. A RCM e a histopatologia conduzem a resultados idênticos em 88% dos casos [1]. A RCM também é útil se for o subtipo raro de lentigo maligno não melanocítico, uma vez que revela as células dendríticas características deste subtipo raro [1]. Histopatologicamente, LM é caracterizada por melanócitos atípicos no basal do estrato sobre um fundo de elastose solar. Os melanócitos solitários e aninhados atípicos proliferam ao longo da zona juncional dermo-epidérmica. O envolvimento folicular é uma característica histopatológica presente em 95,8% do LM, como mostra um estudo de 2019 publicado em JAAD [12].
Resumo
|
Literatura:
- Cosgarea R: Lentigo maligna. Prof. Dr Rodica Cosgarea, Congresso EADV, Madrid, 11.10.2019.
- DeWane ME : JAAD 2019; 81 (3): 823-833.
- Guitera P, et al: Australas J Dermatol 2019; 60(2): 118-125.
- Menzies SW, et al: Melanoma Res 2020; 30(2): 193-197.
- National Comprehensive Cancer Network (NCCN), Guidelines 2. 2018, www.nccn.org
- Papanikolaou M, Lawrence CM: Clin Exp Dermatol 2019; 44(6): 631-636.
- Swetter SM, et al: J Am Dermatol 2015; 72(6): 1047-1053.
- Donigan JM, et al: JAMA Dermatol 2018; 154(8): 885-889.
- Duarte AF et al: Dermatologia 2018; 234: 37-42.
- Tschandl P, et al: Acta Derm Venereol 2017 15;97(10):1219-1224.
- Zoutendijk J, et al: Br J Dermatol 2019; 181(2): 383-384.
- Connolly KL, et al: J Am Acad Dermatol 2019 ; 80(2): 532-537.
- Yélamos O, et al: JAMA Dermatol 2017; 153(12): 1278-1284.
PRÁTICA DA DERMATOLOGIA 2020; 30(3): 32