A descongestionamento físico complexo – drenagem linfática manual combinada com compressão consistente – é o padrão de ouro no tratamento do linfedema. Visão geral da classificação do linfedema e das suas fases, bem como da abordagem diagnóstica e terapêutica conservadora.
O linfedema é uma doença crónica do interstício resultante de danos primários ou secundários no sistema de drenagem linfática. Em condições fisiológicas, existe um equilíbrio entre o fluido filtrado através da parede do vaso sanguíneo para o interstício e não reabsorvido e a sua remoção do interstício através do sistema linfático [1]. Aqui, a pressão coloidosmótica intravascular é responsável pela reabsorção do fluido intersticial no leito capilar, ou seja, a capacidade das proteínas para ligar a água. Como algumas proteínas também atravessam para o interstício, estas neutralizam o KOD intravascular e nem toda a água filtrada pode ser reabsorvida. Estas proteínas e o fluido a elas ligado, bem como outras substâncias intersticiais que requerem linfa (bactérias, vírus, detritos celulares, leucócitos, macrófagos, imunoglobulinas, etc.) devem ser obrigatoriamente drenados e removidos através do sistema linfático. Estudos recentes sugerem que o volume de fluido que requer drenagem linfática parece ser maior do que se pensava anteriormente [2].
Consequentemente, o edema ocorre sempre que a filtração é maior do que o KOD e a drenagem linfática. O linfedema forma-se assim que a drenagem linfática deixa de estar estrutural ou funcionalmente garantida. As proteínas e o fluido no interstício que requerem a acumulação linfática e a alteração dos tecidos ocorrem durante o curso da doença, embora os mecanismos exactos não sejam conhecidos. O linfedema evolui assim para uma doença crónica e progressiva. O risco de erisipela é aumentado, o que por sua vez afecta os vasos linfáticos [1].
Linfedema primário
Apenas cerca de 1% de todo o linfedema é de origem primária, com o linfedema primário (Fig. 1) a ocorrer sobretudo esporádica e menos frequentemente hereditária ou associada a sintomas [3]. A causa é um arranjo hipo ou hiperplástico/displásico do sistema vascular linfático, fibrose dos gânglios linfáticos ou acinesia. Na maioria dos casos, existem formas mistas [4]. O linfedema primário é mais frequentemente localizado para as extremidades inferiores e é geralmente unilateral. Os primeiros sinais clínicos aparecem na periferia (dedos dos pés, dedos das mãos) e espalham-se proximamente ao longo do tempo. Epidemiologicamente, o linfedema primário é mal estudado. A incidência de linfedema primário ao nascimento é estimada em aproximadamente 1:6000 [5], e a prevalência nos menores de 20 anos é de aproximadamente 1:87.000 [6]. A primeira manifestação nos rapazes ocorre frequentemente nos primeiros doze meses de vida, nas raparigas em torno da puberdade. No entanto, uma manifestação inicial pode ocorrer em qualquer idade. As mulheres são cerca de cinco vezes mais susceptíveis de serem afectadas [7–9].
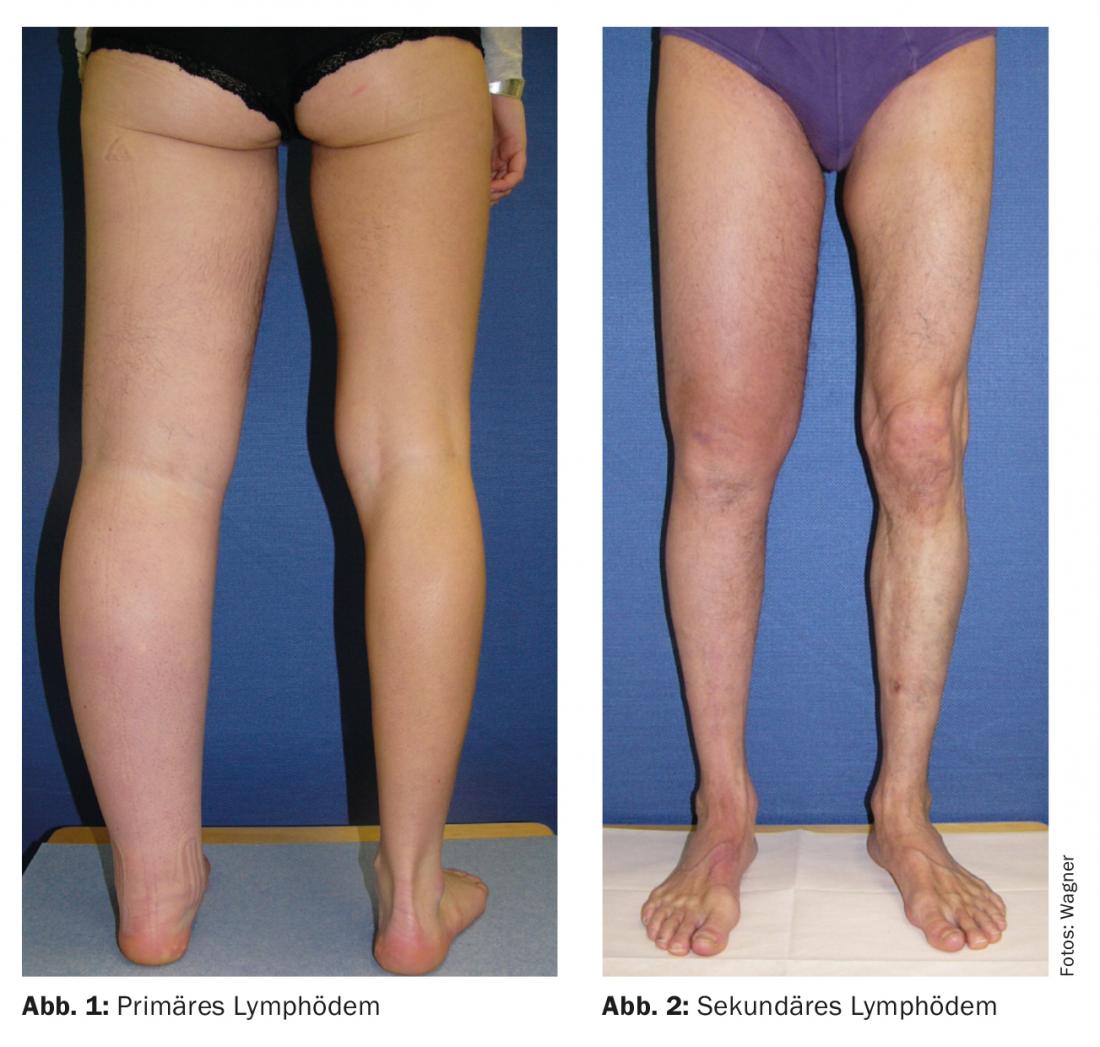
Linfedema secundário
A causa do linfedema secundário (Fig. 2) é uma interrupção adquirida da drenagem linfática. Isto pode ser o resultado de uma lesão linfática “benigna” (trauma, operações, infecções crónicas) ou associada a um tumor (“maligno”). Clinicamente, o linfedema secundário manifesta-se a partir do ponto de interrupção em direcção à periferia.
Em todo o mundo, a causa secundária mais comum é a filariose, um nemátodo que se aloja no sistema vascular, levando assim à obliteração dos capilares linfáticos através da inflamação crónica. Nos países industrializados, a terapia tumoral é a principal causa de linfedema secundário. Com a excisão dos gânglios linfáticos axilares, a incidência é de cerca de 20% [7] Após a excisão dos gânglios linfáticos sentinela, uma incidência de até 5% ainda está listada [10], com aumento do linfedema da mama a ser observado. Em operações com remoção de gânglios linfáticos no abdómen, pélvis ou região inguinal, foi descrita uma incidência média de linfedema de aproximadamente 16-20% [11–13], e dependendo da natureza radical da operação, mesmo até 50% [14]. É certo que o número de gânglios linfáticos removidos, bem como a localização, desempenham um papel importante. A obesidade pré-existente e as infecções perioperatórias aumentam a taxa de linfedema. A radioterapia é também descrita como um factor de risco. A quimioterapia não está assegurada.
O linfedema está dividido em quatro fases de acordo com Földi [15] e ISL (Sociedade Internacional de Linfologia) [16] (Tab. 1).

Diagnósticos
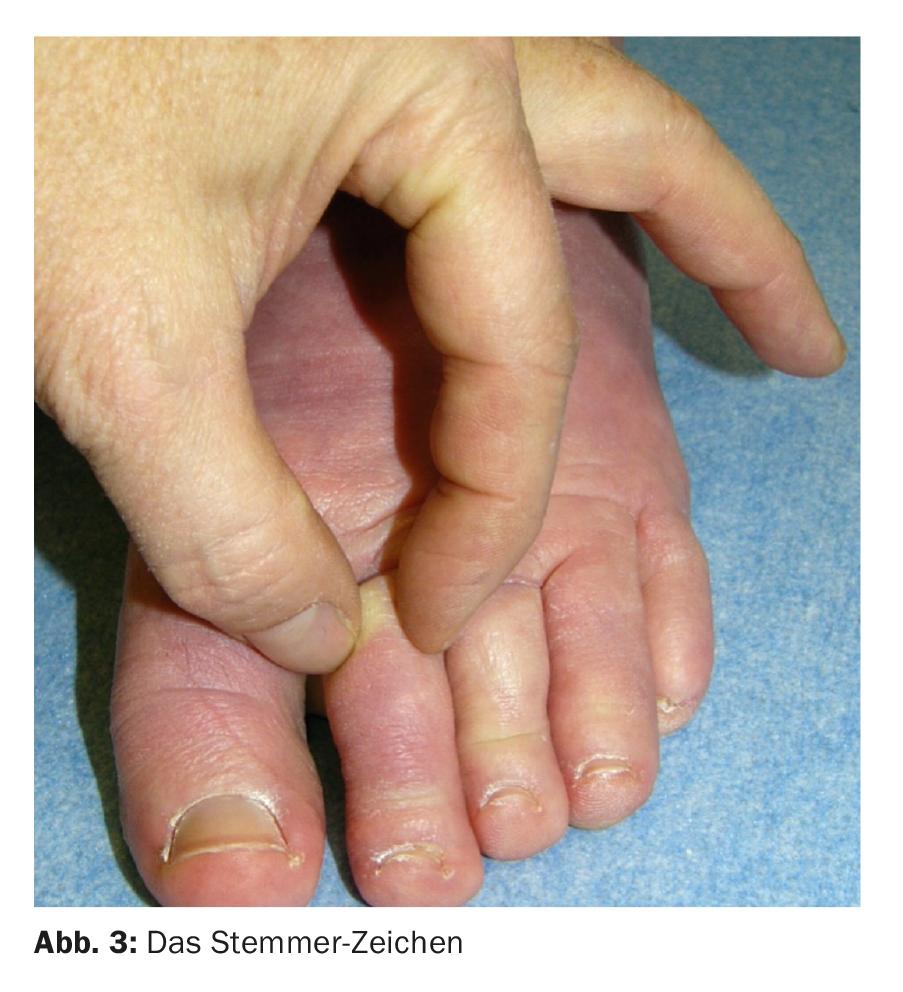
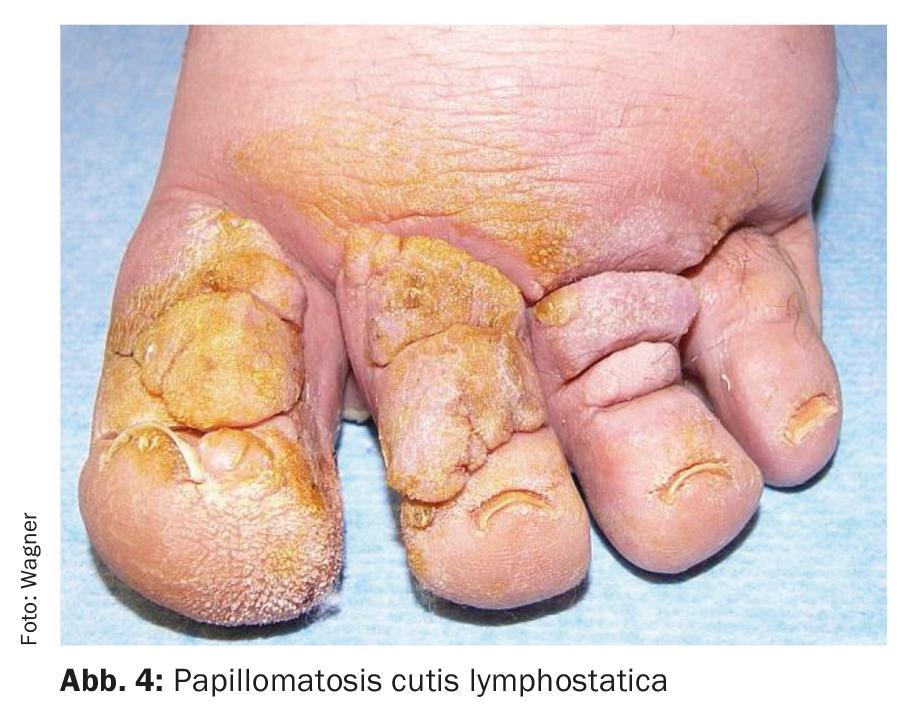
O diagnóstico básico, ou seja, anamnese, inspecção e palpação, é geralmente suficiente para estabelecer o diagnóstico, desde que o linfedema seja mesmo considerado como um diagnóstico diferencial. Evidentemente, é importante excluir outros quadros clínicos indutores de edema [17]. Isto também se aplica em particular à exclusão de linfedema secundário induzido por tumores no momento do diagnóstico. O historial médico do paciente descreve um inchaço que é regressivo no início e que normalmente não se realiza durante muito tempo, mas que depois persiste cada vez mais. Muitas vezes há também um evento desencadeante, como uma distorção ou uma picada de mosquito com inchaço que não desaparece. Isto é geralmente unilateral, se bilateral tipicamente assimétrico. Especialmente no edema primário, os dedos dos pés e dos pés são quase sempre afectados no curso e o sinal do Stemmer é positivo (dobra de pele não elevadora no segundo dedo do pé ou dorso do dedo (Fig. 3). Além disso, as dobras de pele fina sobre os dedos dos pés tornam-se escarificadas e as dobras de pele mais grossa começam a formar-se na base dos dedos dos pés. A fibrose pode ser palpada. O tecido é mole no início, mas à medida que avança torna-se cada vez mais difícil de pressionar devido à fibrose, e alterações cutâneas secundárias como a papilomatose cutis linfostática (Fig. 4) podem desenvolver-se.
Os diagnósticos instrumentais raramente são necessários. A micro linfografia de fluorescência está estabelecida na Suíça, e a cintigrafia funcional na Alemanha. A linfografia verde indocianina tornou-se estabelecida nos últimos anos para planeamento pré-operatório e controlo pós-operatório, mas não para diagnóstico. Ultra-sons, MR, linfografia directa e indirecta podem ser úteis para questões específicas, mas não servem como diagnósticos primários.
A abordagem terapêutica conservadora
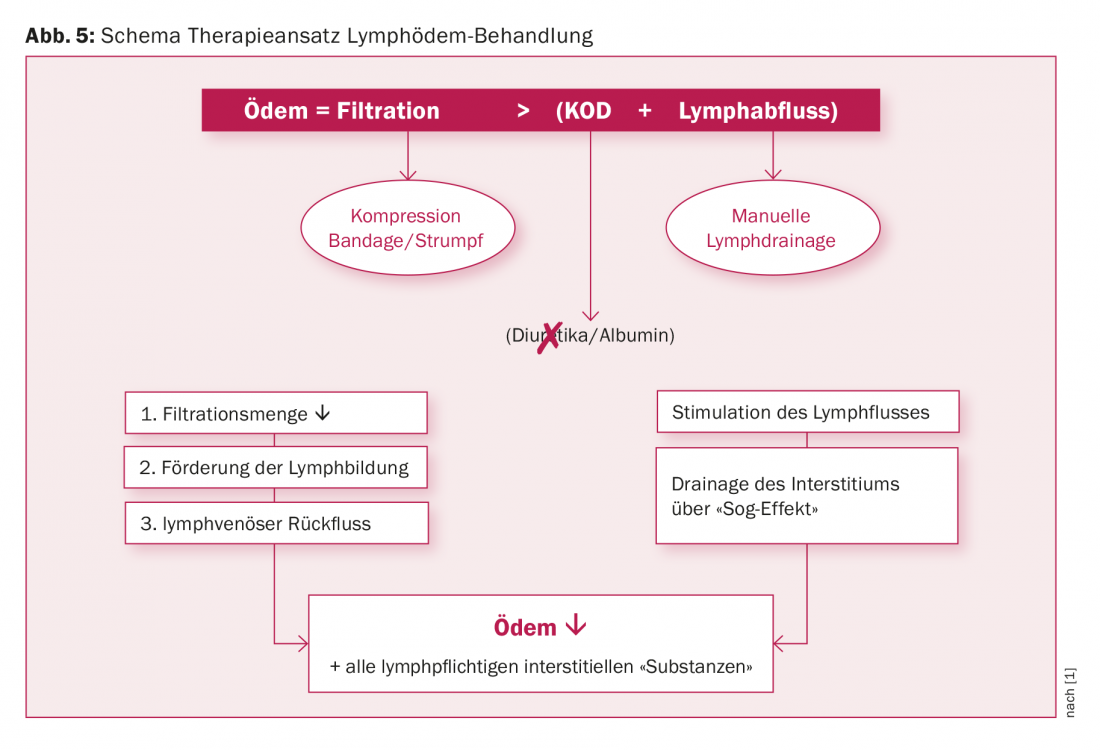
Assumindo que temos sempre edema quando a filtração é maior que a pressão osmótica coloidal e a drenagem linfática juntas, cada um destes factores pode, em princípio, ser visado (Fig. 5). No caso de linfedema, a terapia de compressão e a drenagem linfática manual são especificamente utilizadas. Os diuréticos estão contra-indicados, especialmente no paciente mais jovem, uma vez que promovem a remodelação do tecido fibrótico a longo prazo. Podem ser necessárias selectivamente no início de uma fase de descongestionamento para prevenir a insuficiência cardíaca. As infusões com albumina humana são reservadas à medicina de cuidados intensivos para indicações especiais. A drenagem linfática manual estimula os vasos linfáticos do centro para o periférico, criando um efeito de sucção, que drena o espaço intersticial. Os cursos de drenagem linfática são concebidos de modo a evitar um efeito de massagem com hiperaemia consecutiva do tecido e intensificação da filtração.
Como medida conservadora mais importante, a compressão a partir do exterior contraria a pressão de filtração para que o volume de filtração diminua em função da pressão e, portanto, também o volume linfático restante no interstício. No entanto, a compressão também desloca o fluido intersticial em direcção aos capilares linfáticos drenantes e suporta a drenagem linfática.
Terapia descongestionante física complexa
A combinação de drenagem linfática manual com terapia de compressão é chamada de descongestionamento físico complexo. É feita uma distinção entre a fase de descongestionamento e a fase de manutenção. A fase de descongestionamento consiste em reduzir o edema e amolecer o tecido fibrótico. Durante esta fase intensiva, o tratamento é idealmente diário (ou várias vezes por semana) com aplicação de uma ligadura de compressão de pequeno alongamento, o que requer muita perícia e experiência. A fase de descongestionamento pode muitas vezes ser feita em regime ambulatório. Se a clínica estiver muito avançada, ou se for necessária uma formação intensiva do paciente, recomenda-se a estadia de um paciente internado numa clínica especializada. Uma vez alcançado o objectivo, o tratamento passa à fase de manutenção, em que o tratamento é adaptado à clínica, o que muitas vezes é necessário numa base semanal. O tratamento regular é benéfico para manter a concentração de proteínas que são susceptíveis de linfa e que se acumulam no interstício tão baixa quanto possível. No entanto, a terapia de compressão consistente com uma meia de compressão é sempre obrigatória também nesta fase. A meia de compressão no paciente com linfedema deve ser do tipo “meia plana”. As meias de malha plana de compressão têm tipicamente uma costura. Fisicamente, são mais curtas do que as meias de malha circulares habituais, tendo assim uma maior rigidez e pressão de trabalho e cansando menos durante o dia. As meias de malha plana de compressão são normalmente apropriadas em lojas ortopédicas e é aconselhável receitá-las com o número MiGel 17.10…. A meia de compressão ideal é individual e deve ser trabalhada. Por vezes é melhor combinar duas meias de compressão “classe II” e colocá-las uma em cima da outra do que apenas uma meias de compressão classe IV. Por um lado, as pressões de compressão aumentam, por outro lado, a rigidez do tecido de malha em particular, o que melhor compensa o inchaço. As meias de compressão prescrita devem ser sempre verificadas por um médico. Isto mostra ao paciente a importância desta terapia e, além disso, um bom ajuste aumenta o uso de disciplina.
O paciente afectado por linfedema é um actor muito importante na terapia. Sem o seu cumprimento, um resultado duradouro é dificilmente alcançável. Isto requer que o paciente seja educado sobre a condição, cuidados de pele e a necessidade de uma terapia de compressão consistente. Dependendo da situação clínica e da possibilidade, isto inclui também o ensino da auto-bandagem, bem como simples pegas de auto-descarga. Esta formação é muito demorada e elaborada. Para além da terapia específica, o desequilíbrio muscular normalmente existente deve ser abordado fisioterapêuticamente e o paciente deve ser submetido a exercícios de descongestionamento em seco e também em água. Aquajogar ou nadar na água abaixo dos 30 graus é um excelente remédio porque, por um lado, a compressão é exercida e, por outro, o movimento na água tem uma espécie de efeito de drenagem linfática. Todas estas medidas são demoradas. A disciplina terapêutica necessária só pode normalmente ser alcançada numa rede que funcione bem em redor do paciente. Isto inclui o médico atencioso, terapeuta, armazenista, família, empregador e outras pessoas do ambiente do paciente.
Linfedema e desporto
Todos os estudos que têm investigado a actividade desportiva em doentes com linfedema sempre partiram da questão de saber se o desporto poderia fazer mal. Isto não pôde ser provado em nenhum dos estudos. Estudos individuais mostraram uma tendência para a diminuição do volume. Uma redução significativa do volume só foi encontrada com o caminhar nórdico em pacientes com linfedema do braço [18]. O desporto sob compressão é mais benéfico do que sem. No entanto, o exercício sem compressão não parece ser persistentemente prejudicial [19,20]. Dos estudos e recomendações pode-se concluir que, na realidade, não existem restrições desportivas, mas que existe uma limitação individual. Em princípio, qualquer actividade desportiva é benéfica porque normalmente ajuda a melhorar a qualidade de vida [21].
Medidas terapêuticas complementares
Muitos pacientes com linfedema necessitam de apoio adicional da psicologia clínica para promover a aceitação da condição, o que mais uma vez afecta o seu cumprimento. O facto de se tratar de uma doença crónica que requer atenção diária pode ser muito stressante. Além disso, o linfedema do braço é difícil de esconder em público ou a escolha de roupa é limitada no caso de linfedema das pernas. Entrar numa relação e incluir a sexualidade também requer muita compreensão por parte do parceiro.
Todas as medidas terapêuticas até agora enumeradas trazem uma melhoria em parte considerável na clínica, mas não conduzem a uma cura. Melhoram a qualidade de vida através do controlo dos sintomas e edemas, bem como da prevenção de complicações (erisipela, fibrose, ulceração à imobilização). O objectivo de um tratamento abrangente deve ser manter a capacidade de trabalho e a mais alta qualidade de vida possível. Isto nem sempre é fácil, pois o paciente afectado tem muitas vezes de passar muito tempo com as terapias. O desejo de opções terapêuticas adicionais é, portanto, compreensível.
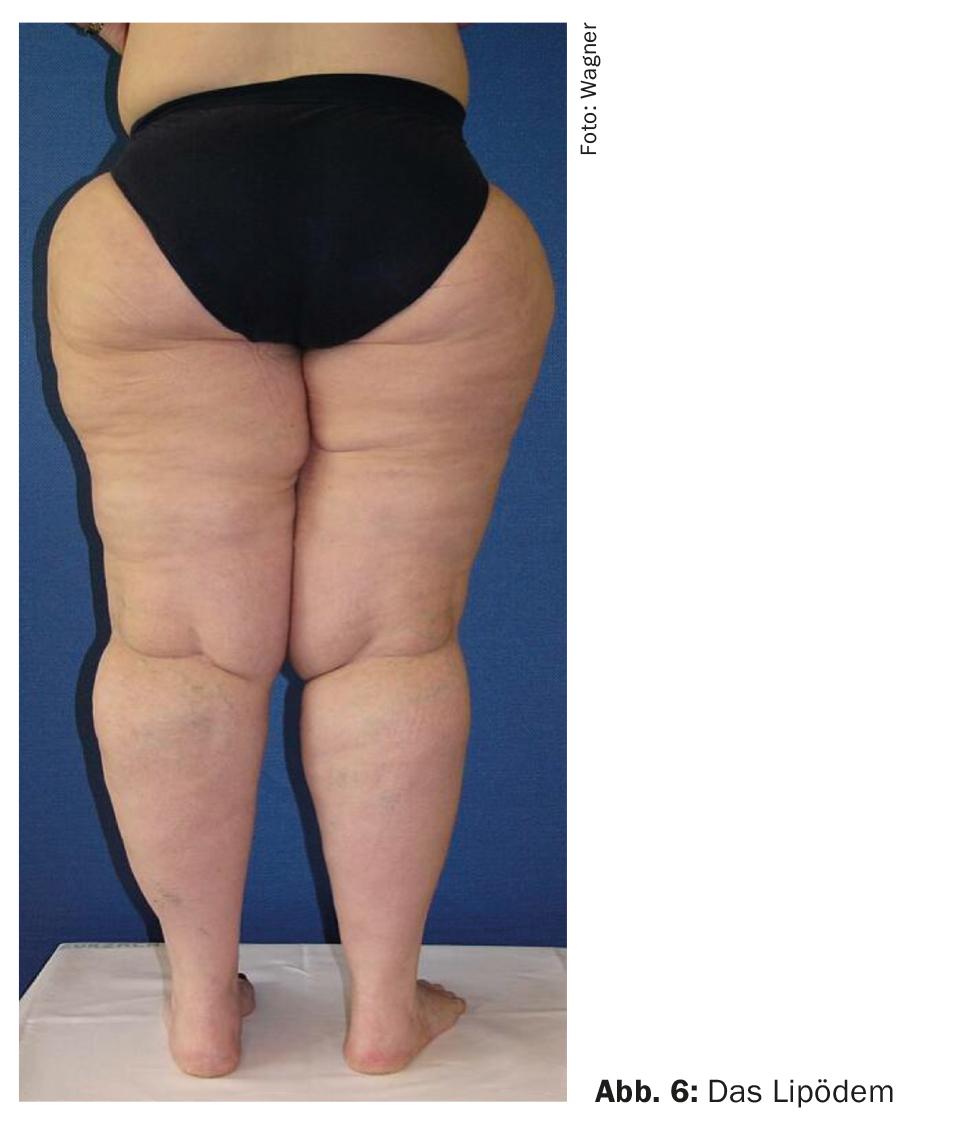
Diagnóstico diferencial de lipedema
Um diagnóstico diferencial frequentemente observado ao linfedema é de pacientes do sexo feminino com lipoedema (Fig. 6). Trata-se de uma hipertrofia e hiperplasia subcutânea das células gordas que afecta principalmente as extremidades inferiores, com uma tendência ortostática para o edema, o que com o tempo leva a dores diárias, por vezes incapacitantes. O linfedema secundário pode desenvolver-se no decurso da doença, mas também podem ser observadas dermatites ou ulcerações por estase. Normalmente, existe uma desproporção entre a parte inferior do corpo e a parte superior do corpo com uma cintura esguia. O quadro clínico do lipedema não deve ser equiparado à obesidade. Mas o ganho de peso corporal é considerado um factor de risco e leva a uma progressão que normalmente só responde frustrantemente à redução de peso por meio de medidas dietéticas. É por isso que é muito importante manter o peso constante. Devido a este factor de risco, muitos doentes com lipedema tendem a ser obesos. No entanto, é frequente ver-se uma cintura fina. A terapia conservadora inclui os mesmos elementos de CPD que para o linfedema, além de conselhos nutricionais e promoção da actividade física [1,22].
Mensagens Take-Home
- O linfedema é uma doença crónica e até agora não curável, com um grande impacto na qualidade de vida.
- O diagnóstico e o início correcto da terapia são frequentemente atrasados.
- O padrão ouro de tratamento até agora tem sido a descongestionamento físico complexo (CPD), que é a drenagem linfática manual combinada com uma compressão consistente.
- O bom cumprimento só pode ser alcançado através da educação intensiva do paciente com a aceitação da responsabilidade pessoal no tratamento da condição.
Literatura:
- GDL Guideline Lymphoedema: S2k Guideline Diagnostics and Therapy of Lymphoedema AWMF Reg. No. 058-001 www.awmf.org/uploads/tx_szleitlinien/058-001l_S2k_Diagnostik_und_Therapie_der_Lymphoedeme_2017-05.pdf
- Levick JR, Michel CC: Troca de fluidos microvasculares e o princípio revisto de Starling. Cardiovasc Res 2010; 87(2): 198-210
- Vignes S.: Linfedema desde o diagnóstico até ao tratamento. Rev Med Interne 2017; 38(2): 97-105.
- Kinmonth JB: Fibrose nos linfonodos no linfedema primário. Ann R Coll Surg Engl 1980; 62: 344-354.
- Dale RF: A herança do lamphedema primário. J Med Genetic 1985; 22(4): 274-278.
- Smeltzer DM, et al: Linfedema primário em crianças e adolescentes: um estudo de acompanhamento e revisão. Pediatria 1985; 76(2): 206-218.
- Moffatt CJ, et al: Lymphoedema: um problema de saúde subestimado. QJM 2003; 96(10): 731-738
- Neuhüttler S, Brenner E: Contribuição para a epidemiologia do linfedema. Phlebology 2003; 35: 181-187.
- Brunner U: Perimed 1985: 39-47.
- Di Sipio, et al: Incidência de linfedema unilateral do braço após o cancro da mama: uma revisão sistemática da literatura e metanálise. The Lancet Oncology 2013; 14(6): 500-515.
- Cormier JN: Linfedema para além do cancro da mama: uma revisão sistemática e uma meta-análise do linfedema secundário relacionado com o cancro Cancro. 2010; 116(22): 5138-5149.
- Todo Y: Relação estreita entre a remoção dos nódulos ilíacos circunflexos aos nódulos ilíacos externos distais e linfedema de extremidade inferior pós-operatório em tumores malignos do corpo uterino. Gynecol Oncol 2015; 139(1): 160-164.
- Yamazaki H: Relação entre a remoção dos nódulos ilíacos circunflexos distais aos nódulos ilíacos externos e linfedema de extremidade inferior pós-operatório no cancro uterino do colo do útero. Gynecol Oncol 2015; 139(2): 295-299.
- Ryan M: Etologia e prevalência de linfedema dos membros inferiores após tratamento do cancro ginecológico. Aust N Z J Obstet Gynaecol 2003; 43(2): 148-151
- Földi E, et al: Sobre o diagnóstico e terapia do linfedema. Dtsch Ärztebl 1998; 95: A-740-747.
- Documento de consenso Linfologia 2016; 49: 170-184.
- Stöberl C: Diagnóstico diferencial clínico do inchaço das pernas – um guia para a prática. Z Gefässmed 2011; 8(1): 11-18.
- Jönsson C: O efeito da marcha de vara sobre o linfedema do braço e a aptidão cardiovascular em mulheres tratadas para o cancro da mama. Um estudo piloto e de viabilidade. Praga da Teoria da Fisioterapia 2014; 30(4): 236-242.
- Singh B: Efeitos da compressão sobre o linfedema durante o exercício de resistência em mulheres com linfedema relacionado com o cancro da mama: um ensaio cruzado aleatório. Linfologia 2015; 48(2): 80-92.
- Johansson K: Exercício de resistência de baixa intensidade para pacientes BC com linfedema do braço com ou sem manga de compressão. Linfologia 2005; 38(4): 167-180.
- Brown JC: Actividade física, marcha diária, e linfedema dos membros inferiores associa-se à função física entre os sobreviventes do cancro do útero. Support Care Cancer 2014; 22(11); 3017-3025.
- S1 Guideline Lipedema AWMF Número de registo 037-012 2016; www.awmf.org/uploads/tx_szleitlinien/037-012l_S1_Lipoedem_2016-01.pdf
CARDIOVASC 2017; 16(5): 6-10