A nefroprotecção inclui intervenções que retardam o declínio da TFG ao longo do tempo, atrasando assim a insuficiência renal em fase terminal. A última intervenção é a utilização de inibidores SGLT2 em doentes com nefropatia diabética.
A insuficiência renal crónica pode ser diagnosticada de duas maneiras:
- Evidência de função renal prejudicada com uma taxa de filtração glomerular calculada (eGFR) inferior a 60 ml/min, persistindo pelo menos durante três meses.
- Evidência de danos renais crónicos (albuminúria, hematúria, provas de imagem, tais como rins policísticos) persistindo pelo menos durante três meses – independentemente do eGFR.
O diagnóstico da insuficiência renal crónica pode assim ser feito na prática com três exames simples: Determinação da creatinina (calcular o eGFR a partir disto), estado da urina com sedimento e proteinúria (urina pontual) e sonografia renal.
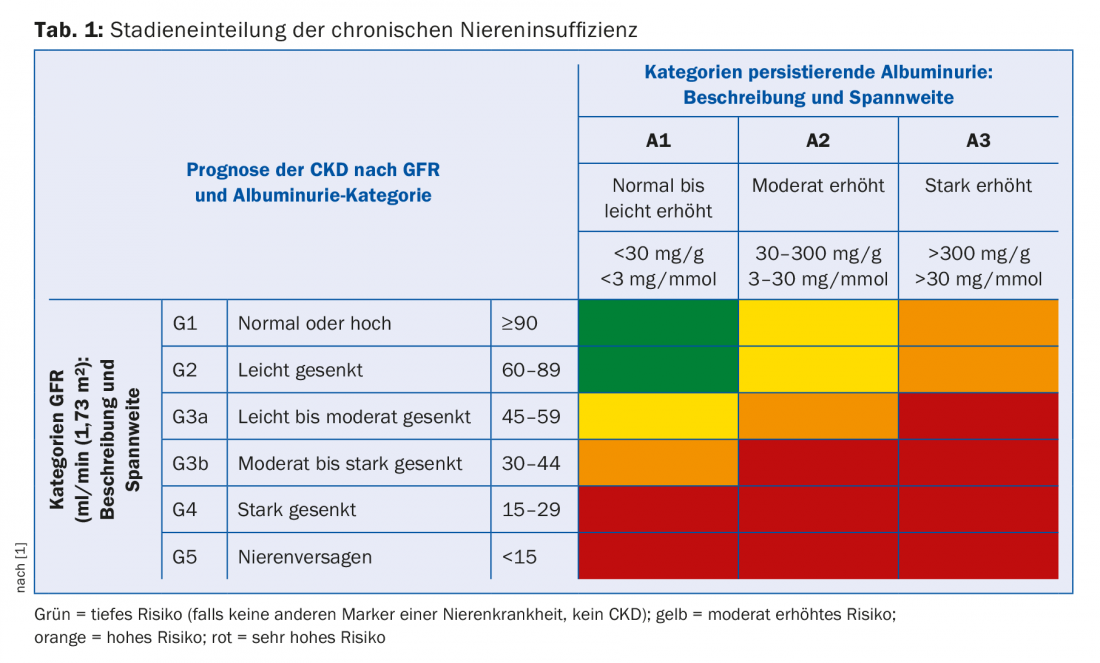
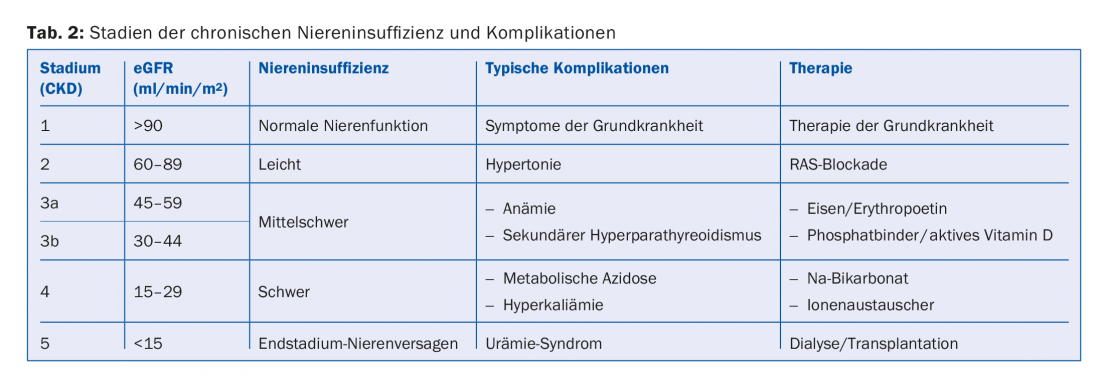
Dependendo da extensão do comprometimento da função renal e da albuminúria, o encenamento da insuficiência renal crónica tem lugar. O eGFR e a albuminúria são factores de risco independentes tanto para a mortalidade cardiovascular como para o risco de desenvolver insuficiência renal em fase terminal [1]. O estadiamento indica, portanto, com que frequência tais pacientes devem ser monitorizados e com que agressividade devem ser tratados no que respeita aos riscos cardiovasculares (tab. 1). Além disso, o grau de comprometimento da função renal indica quais as complicações secundárias que são de esperar (tab. 2). Estes devem ser activamente procurados e, se necessário, tratados.
Curso
A insuficiência renal crónica é progressiva ao longo dos anos, independentemente de a doença subjacente ainda estar activa ou não. Este fenómeno é explicado pela chamada “hipótese de Brenner”, que afirma que com a perda de um maior número de nefrónios, os restantes nefrónios compensam, pelo menos parcialmente, a perda de função e, portanto, hiperfiltram. Esta hiperfiltração, que dura muito tempo, leva a danos dos nefrónios ainda intactos. Histologicamente, a hipertrofia glomerular pode ser detectada primeiro, seguida pelo aumento da glomerulosclerose, resultando numa perda progressiva da função e no aparecimento de albuminúria.
A progressão da insuficiência renal crónica pode ser descrita individualmente por paciente com a chamada curva Mitch [2]. Se se traçar o eGFR ou o valor 1/criarinina ao longo do tempo, então resulta uma curva linearmente decrescente. Com esta curva, o risco de desenvolvimento de insuficiência renal em fase terminal pode ser estimado para um doente individual (Fig. 1A). Isto facilita a discussão com o doente e permite fazer preparativos atempados para o início de um procedimento de substituição renal.
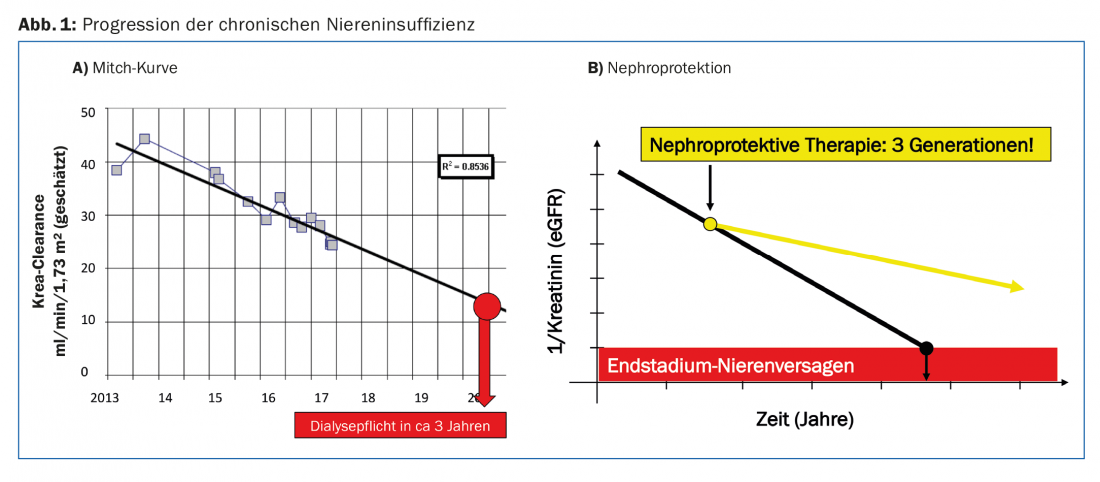
Como médicos, gostaríamos de ter uma influência favorável sobre a progressão da insuficiência renal crónica. Por “medidas nefroprotectoras” entendemos todas as intervenções que abrandam o declínio do eGFR ao longo do tempo. Até à data, não houve qualquer intervenção para acabar completamente com este desperdício. Mas se a queda na curva do Mitch puder ser achatada apenas um pouco, o paciente pode ganhar vários anos de tempo livre de diálise (Fig. 1B).
Nefroprotecção
Primeira geração – bloqueio do sistema renina-angiotensina: O sistema renina-angiotensina (RAS) está crucialmente envolvido na regulação do fluxo sanguíneo renal e, portanto, na perfusão dos glomérulos individuais. A angiotensina influencia directamente o tom dos eferens do vaso. Mais angiotensina leva à constrição dos eferens do vaso e, portanto, a um aumento da pressão de filtração no leito capilar glomerular. Por um lado, isto permite a auto-regulação da filtração glomerular sobre uma vasta gama de flutuações da pressão sanguínea. Por outro lado, também conduz à hiperfiltração acima referida no âmbito da hipótese do Brenner. O bloqueio do RAS com inibidores da ECA, bloqueadores dos receptores de angiotensina tipo 1 (sartans) ou inibidores de renina leva à dilatação do vaso eferente no glomérulo. Isto reduz a pressão de perfusão glomerular e protege o leito capilar glomerular. Ao mesmo tempo, porém, a taxa de filtração glomerular por nefrónio e a taxa de filtração global diminui. O início do bloqueio do EAR num doente com insuficiência renal conduz sempre, portanto, a um aumento da creatinina. Tal aumento pode ser tolerado até 25%, desde que subsequentemente se mantenha estável a este nível. O aumento da creatinina é funcional e prova que a pressão de perfusão glomerular poderia de facto ser reduzida. Se o bloqueio do RAS for interrompido novamente, a creatinina cai novamente pelo mesmo valor. Se o nível de creatinina não estabilizar após a introdução do bloqueio RAS, deve ser novamente parado e deve ser procurada uma estenose da artéria renal.
Vários ensaios aleatorizados nos anos 90 mostraram que o bloqueio RAS pode retardar a progressão da insuficiência renal crónica, tanto na nefropatia diabética como na não diabética [3]. O bloqueio RAS é assim agora a base de qualquer intervenção nefroprotectora e deve ser tornado mais agressivo quanto mais alta for a proteinúria. As substâncias individuais devem ser doseadas ao máximo; o duplo bloqueio RAS deve ser estritamente evitado [4].
Segunda geração – correcção da acidose metabólica: O rim é o órgão principal para a excreção de ácidos fixos, e estes acumulam-se com a crescente restrição da função renal. A insuficiência renal crónica está portanto geralmente associada à ocorrência de acidose metabólica, especialmente nas fases avançadas a partir do CKD G3b.
A acidose metabólica tem vários efeitos desfavoráveis. Prejudica a saúde óssea e promove a ocorrência de hipercalemia, o que por sua vez aumenta o risco de arritmias cardíacas. No entanto, se a própria acidose metabólica influencia a progressão da insuficiência renal crónica não era clara durante muito tempo. Nos anos 2000, foram publicados vários ensaios randomizados que investigaram o efeito do tratamento da acidose metabólica com bicarbonato de sódio na progressão da insuficiência renal crónica. Para surpresa de muitos nefrologistas, foi demonstrado que em várias fases da insuficiência renal crónica (CKD G2, G3 e G4), a progressão pode ser retardada e a ocorrência de insuficiência renal em fase terminal atrasada com esta simples medida [5]. Assim, é agora uma recomendação geral que a acidose metabólica com um bicarbonato de sódio <20 mmol/l deve ser tratada com bicarbonato de sódio. Isto também melhora a hipercalemia, que por sua vez permite a manutenção do bloqueio RAS mais eficiente.
As limitações desta intervenção são frequentemente a tolerabilidade (o bicarbonato de sódio causa flatulência), o elevado número de comprimidos (para conseguir um bicarbonato de soro >20 mmol/l, por vezes são necessários seis a oito comprimidos por dia) e a carga de sódio, o que pode levar a um aumento do edema e/ou aumento da pressão arterial.
Terceira geração – bloqueio do cotransportador de sódio/glucose SGLT2 no túbulo proximal: Nos últimos anos, um novo grupo de medicamentos antidiabéticos orais tem sido testado em vários ensaios aleatórios: Estes são inibidores do cotransportador de sódio/glucose no tubo proximal (SGLT2, “transportador de sódio-glucose 2”). Estes fármacos induzem glucosúria. Isto resulta num melhor HbA1c e num balanço calórico negativo que leva a uma perda líquida de peso. Ao mesmo tempo, porém, o bloqueio do SGLT2 leva também à natriurese. Estas substâncias são assim uma nova classe de diuréticos que, ao contrário dos diuréticos de laço e dos tiazídicos, não actuam no nefrónio distal mas sim no túbulo proximal.
Os inibidores SGLT2 têm sido testados até agora principalmente em pacientes com diabetes tipo 2 e um perfil de risco cardiovascular aumentado (frequentemente na prevenção secundária). Foi demonstrado um benefício altamente significativo na mortalidade por todas as causas (empagliflozina) e na mortalidade cardiovascular (empagliflozina, canagliflozina). Devido ao efeito diurético, as re-hospitalizações devidas à insuficiência cardíaca descompensada poderiam também ser significativamente reduzidas [6,7].
Os estudos de acompanhamento também demonstraram agora um efeito positivo altamente significativo nos pontos terminais renais duros (novo início da macroalbuminúria, duplicação da creatinina sérica, ocorrência de falha renal em fase terminal). O efeito é da mesma ordem de grandeza do bloqueio RAS num grupo de doentes que, na sua maioria, já é tratado com bloqueadores RAS [8]! O mecanismo de nefroprotecção ainda não foi clarificado em pormenor. Contudo, é postulado um efeito através da macula densa com dilatação dos vas afferens. Foi demonstrado o mesmo aumento de creatinina funcional no início do tratamento com subsequente estabilização da função renal que com o bloqueio RAS [9].
Dois efeitos secundários clínicos devem ser notados com esta classe de substância: Frequentes mas inofensivas são infecções urogenitais aumentadas, que podem ser facilmente tratadas. Uma complicação rara mas grave é a cetoacidose diabética euglicémica, que pode ocorrer com deficiência de insulina e longos períodos de jejum. Nas situações clínicas enumeradas no quadro 3, os inibidores SGLT2 não devem, portanto, ser utilizados ou utilizados apenas com grande precaução ou temporariamente em pausa.

Conclusão
Após o bloqueio do RAS e a terapia da acidose metabólica, uma terceira medida nefroprotectora está agora disponível há dois anos: a utilização de inibidores SGLT2. Actualmente, isto só é aprovado para doentes com nefropatia diabética (separador 4) . Uma vez que o mecanismo de nefroprotecção muito provavelmente não tem nada a ver com a influência no metabolismo da glucose, mas sim com o efeito diurético destas substâncias, pode-se assumir que também funcionariam em nefropatia não diabética. Os estudos correspondentes estão actualmente em curso.

Mensagens Take-Home
- A insuficiência renal crónica tem um curso progressivo que pode ser descrito com a curva de Mitch.
- Por medidas nefro-protectoras entendemos intervenções que podem retardar o declínio do TFG ao longo do tempo e assim atrasar a insuficiência renal em fase terminal.
- A base de qualquer nefroprotecção é a utilização de inibidores do sistema renina-angiotensina (inibidores da ECA, bloqueadores dos receptores AT1, inibidores da renina). Estes devem ser doseados de acordo com a tolerância, mas não combinados.
- O tratamento da acidose metabólica com bicarbonato de sódio é nefroprotector e deve ser iniciado com um bicarbonato de soro <20 mmol/l.
- A última intervenção é a utilização de inibidores SGLT2 em doentes com nefropatia diabética. Têm um efeito diurético sobre o túbulo proximal e são cardio-protectores e nefro-protectores.
Literatura:
- Stevens PE, Levin A: Avaliação e gestão da doença renal crónica: sinopse da doença renal: melhorar os resultados globais 2012 directriz da prática clínica. Ann Intern Med 2013; 158: 825-830.
- Mitch WE, et al: Um método simples de estimar a progressão da insuficiência renal crónica. Lancet 1976; 2: 1326-1328.
- Lewis EJ, et al: O efeito da inibição da angiotensina-conversão enzimática sobre a nefropatia diabética. O Grupo de Estudo Colaborativo. N Engl J Med 1993; 329: 1456-1462.
- Luft FC: Perspectiva de terapia de bloqueio RAS combinada: off-TARGET, dis-CORD, MAP-to-nowhere, ALTITUDE baixo, e NEPHRON-D. Am J Nephrol 2014; 39: 46-49.
- de Brito-Ashurst I, et al: A suplementação de bicarbonato retarda a progressão do CKD e melhora o estado nutricional. J Am Soc Nephrol 2009; 20: 2075-2084.
- Zinman B, et al: Empagliflozin, Cardiovascular Outcomes, and Mortality in Type 2 Diabetes. N Engl J Med 2015; 373: 2117-2128.
- Neal B, et al: Canagliflozin e Eventos Cardiovasculares e Renais na Diabetes Tipo 2. N Engl J Med 2017; 377: 644-657.
- Wanner C, et al: Empagliflozin e Progressão da Doença dos Rins na Diabetes Tipo 2. N Engl J Med 2016; 375: 323-334.
- Anders HJ, et al: Nephron Protection in Diabetic Kidney Disease (Protecção Nephron na doença renal diabética). N Engl J Med 2016; 375: 2096-2098.
PRÁTICA DO GP 2018; 13(4): 22-25
CARDIOVASC 2019; 18(5): 6-9