A sua heterogeneidade levou a que a asma fosse considerada como um termo abrangente e não como uma doença em si mesma. Engloba vários aspectos e características que se podem sobrepor, dificultando a gestão da asma e exigindo uma fenotipagem precisa. Mas tenha cuidado: uma vez diagnosticado um fenótipo, este não permanece necessariamente fixo – pode mudar ao longo da vida.
Atualmente, é feita uma distinção básica com base na extensão da inflamação do tipo 2 e diferencia-se entre asma T2-alta e T2-baixa. Dr. Fabio L.M. Ricciardolo, Departamento de Asma Grave e Doenças Pulmonares Raras, Hospital Universitário San Luigi Gonzaga, Turim, e colegas [1] escrevem que vários fenótipos estão subordinados a cada uma destas duas formas.
A classificação dos fenótipos de asma em T2-alto e T2-baixo baseia-se atualmente na predisposição atópica e em pelo menos um dos biomarcadores: imunoglobulina E (IgE) sérica elevada, níveis elevados de óxido nítrico exalado fraccionado (FeNO) e eosinofilia no sangue (B-EOS) e/ou na expetoração (S-EOS).
Asma T2-alta
Os fenótipos T2-elevados têm uma resposta imunitária-inflamatória comum conduzida por linfócitos Th2 (imunidade adaptativa) e ILCs (células linfóides inatas) do grupo 2 (ILC2, imunidade inata). As características da inflamação T2 são as citocinas T2, como a IL-5, IL-4, IL-13, IL-9, a prostaglandina D2 (PGD2) e os eosinófilos, cuja elevada expressão pode ser detectada nas vias respiratórias (lúmen ou parede brônquica) e no sangue periférico dos doentes. De facto, o termo asma eosinofílica é sinónimo de asma T2 alta, inclui fenótipos alérgicos e não alérgicos e afecta cerca de 50% dos doentes com asma grave.
A asma alérgica desenvolve-se após a exposição a vários aeroalergénios que causam a ativação de células dendríticas (DCs). As DCs na camada subepitelial actuam como células apresentadoras de antigénios e podem reconhecer e processar alergénios. Assim que são activadas, ocorre a chamada fase precoce e depois a fase tardia da reação alérgica.
Para além da inflamação das vias respiratórias, a asma T2-alta é acompanhada por alterações estruturais das vias respiratórias (remodelação). Estas alterações incluem a metaplasia das células caliciformes, o que leva a um aumento da produção de muco e à consequente formação de tampões de muco. Um estudo recente demonstrou que as vias respiratórias de doentes com asma grave e inflamação T2 têm uma maior presença de tampões de muco, desempenhando os eosinófilos um papel fundamental na formação desses tampões.
Asma alérgica de início precoce
Os factores desencadeantes e os sintomas típicos da asma infantil são os alergénios e outros estímulos ambientais, como as infecções virais, os poluentes, os agentes oxidantes e o fumo do tabaco. Provocam uma cascata imunitária e inflamatória, que é responsável pela broncoconstrição aguda. Esta asma de início precoce (EOA) é normalmente caracterizada por atopia com a presença de IgE específica para alergénios em circulação e é caracterizada pela chamada “marcha atópica”, que é uma progressão da dermatite atópica para rinite alérgica e asma.
A EOA pode durar uma vida inteira. Os estudos que analisaram os factores determinantes desta persistência apontaram o tabagismo materno durante a gravidez, as infecções do trato respiratório superior e inferior, a atopia, a sibilância causada por infecções por rinovírus e a eosinofilia sanguínea na primeira infância como factores de risco para uma função pulmonar inferior, asma e asma grave na infância em idade escolar, na adolescência e na idade adulta jovem.
Asma não alérgica de início tardio
A asma não alérgica começa na idade adulta e pode ser definida como asma de início tardio (LOA). Tal como a asma alérgica, a LOA também se caracteriza por uma assinatura imunitária e inflamatória T2 pronunciada e é caracterizada pela ausência de atopia e da consequente sinalização por IgE.
A LOA pode manifestar-se em diferentes graus de gravidade, sendo que a forma grave conduz a uma pior função pulmonar, a uma obstrução mais grave das vias aéreas e a um aumento da eosinofilia, apesar do tratamento com doses elevadas de corticosteróides inalados (ICS), escrevem os autores. Foram encontradas concentrações elevadas de ILC2 nas vias respiratórias e no sangue periférico de doentes com asma grave não alérgica, caracterizada por eosinofilia descontrolada na expetoração e resistência aos esteróides, o que indica um mecanismo que envolve possivelmente a IL-33.
Asma analgésica
A doença respiratória exacerbada pela aspirina (DRAE) ocorre em estreita associação com sintomas respiratórios que se desenvolvem rapidamente após a toma de analgésicos como o ácido acetilsalicílico ou um inibidor não esteroide da ciclooxigenase-1 (COX-1). As reacções aos AINEs, a asma e os pólipos nasais são características da síndrome (tríade de Samter). Tanto em adultos como em crianças, a asma alérgica ou a rinite alérgica podem manifestar-se antes da hipersensibilidade ao analgésico, mas a AERD não é considerada uma doença alérgica, uma vez que não produz anticorpos IgE específicos. Cerca de 8-26% dos doentes com RSC e pólipos nasais têm simultaneamente DRAE, enquanto a prevalência é de cerca de 7% em todos os doentes com asma e duas vezes mais elevada nos doentes com asma grave.
T2 – asma baixa
A asma T2-baixa inclui todas as formas de asma sem as características da asma T2-alta. Com base no perfil inflamatório das vias respiratórias, é feita uma distinção entre asma neutrofílica (neutrofilia na expetoração com baixa eosinofilia), mista (elevada neutrofilia e eosinofilia na expetoração) e paucigranulocítica (baixa neutrofilia e eosinofilia na expetoração). A asma T2 baixa pode variar em termos de gravidade, sendo que os fenótipos mistos e neutrofílicos tendem a ter uma maior gravidade e taxas de exacerbação. Atualmente, não existem moléculas validadas como biomarcadores, embora os estudos com amostras de sangue/vias respiratórias de doentes com asma apresentem resultados encorajadores, segundo o Prof.
As causas da inflamação neutrofílica das vias aéreas incluem infecções bacterianas e virais, sendo estas últimas a causa das exacerbações da asma. Foi observada uma maior frequência de exacerbações e uma maior incidência de SRC e infecções virais em doentes com inflamação neutrofílica.
Em doentes com asma expostos a doses elevadas de CI e/ou a um tratamento prolongado com corticosteróides orais (CO), a utilização de corticosteróides pode levar a um fenótipo não eosinofílico. No entanto, os estudos revelaram que os doentes com um fenótipo molecular, incluindo os doentes com asma eosinofílica grave, eram mais susceptíveis de tomar OCS do que os doentes com um fenótipo molecular neutrofílico. Além disso, vários estudos de biópsia brônquica mostraram um estado reduzido ou estável dos neutrófilos após o tratamento com corticosteróides.
Asma do fumador
O fumo do tabaco pode desencadear processos patogénicos e conduzir a um fenótipo associado a uma série de características: deterioração acelerada da função pulmonar, mau controlo da asma, exacerbações mais frequentes, menor qualidade de vida, taxas de hospitalização mais elevadas e um maior risco de comorbilidades, como o cancro. Foi relatado que a asma em fumadores está associada a uma inflamação T2 baixa.
A resistência aos esteróides associada ao tabagismo e a exclusão dos fumadores com asma da maioria dos ensaios clínicos representam um grande desafio no tratamento deste fenótipo.
Asma induzida pela obesidade
A asma induzida pela obesidade tem normalmente uma forma grave em que os doentes são frequentemente resistentes aos esteróides. As alterações nas características clínicas e funcionais, como a hiperresponsividade das vias aéreas (AHR), podem ser melhoradas através da perda de peso. A obesidade é uma condição patológica caracterizada por uma inflamação sistémica que envolve macrófagos. Pensa-se que os macrófagos são responsáveis pela inflamação do tecido adiposo, o que leva à libertação de TNF-α, leptina e IL-6 na corrente sanguínea. 62% dos doentes obesos com asma têm níveis plasmáticos baixos de IL-6. Um estudo mostrou que níveis elevados de IL-6 estavam associados a asma grave e a perturbações metabólicas, tanto em doentes obesos como em não obesos.
Asma nos idosos
A asma relacionada com a idade surge quando a doença se manifesta pela primeira vez após os 65 anos de idade. Estes doentes têm uma taxa de morbilidade e mortalidade mais elevada. Há muitas razões para isso, incluindo comorbilidades, consciência inadequada dos sintomas da asma, potencial declínio cognitivo e efeitos adversos da polifarmacoterapia. Os processos de envelhecimento que alteram a estrutura e a fisiologia dos pulmões também têm um efeito na asma e no seu desenvolvimento. As alterações relacionadas com a idade incluem o estreitamento das vias aéreas periféricas, a dilatação alveolar, o aumento da rigidez da parede torácica, a redução da força dos músculos respiratórios e a diminuição da função pulmonar. A fisiopatologia exacta deste fenótipo não é clara, o que torna o seu tratamento muito difícil, escrevem os autores. São necessários mais estudos para esclarecer a possível relação com a resistência aos corticosteróides em doentes com asma mais velhos.
Asma pós-menopausa
Uma maior proporção de rapazes é afetada pela asma na infância. Esta situação altera-se na idade adulta, onde a percentagem de mulheres é mais elevada. Para além dos factores genéticos, este desenvolvimento é também atribuído às hormonas: Concentrações elevadas de estrogénio e progesterona podem modular a expressão e a atividade das células imunitárias, das citocinas inflamatórias e dos glucocorticóides, o que leva à indução de uma reação Th2 com eosinófilos e a um aumento do FeNO na fase pré-menstrual. É provável que este facto contribua para a gravidade e o agravamento dos sintomas da asma, das exacerbações e da hospitalização durante a menstruação, a perimenopausa e a gravidez.
Estudos sobre a asma da menopausa demonstraram um risco acrescido de asma em mulheres magras que tomam terapêutica hormonal de substituição, bem como uma redução da função pulmonar e um aumento dos sintomas de asma em mulheres pós-menopáusicas em comparação com doentes pré-menopáusicas. São necessários mais estudos para investigar os mecanismos internos da asma pós-menopausa.
Sobreposição dos fenótipos
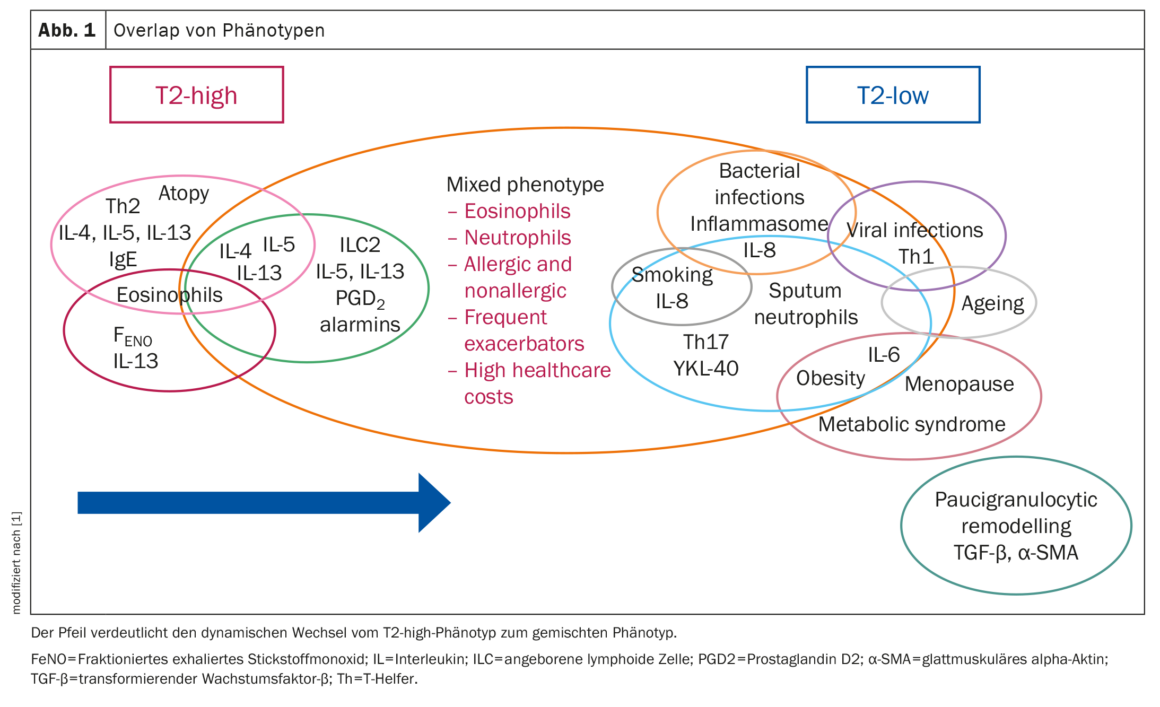
A identificação do fenótipo da asma é crucial para o tratamento da doença, explicam o Prof. No entanto, várias vias de sinalização molecular podem estar interligadas e sobrepor-se entre diferentes fenótipos, o que pode resultar em resultados clínicos inesperados. Vários estudos forneceram provas de uma interação entre vias que anteriormente se pensava serem mutuamente exclusivas (Fig. 1).
Num estudo, foi observada uma sobreposição em >70% dos doentes, com combinações de fenótipos relacionados com T2, não relacionados com T2 e mistos T2/não relacionados com T2, tendo o último grupo apresentado os piores resultados clínicos. Foram detectadas sobreposições do fenótipo T2 em várias combinações de subtipos alérgicos, eosinofílicos e T2-alto. O fenótipo alérgico foi o fenótipo individual mais comum, mas também o que ocorreu mais frequentemente em simultâneo com outros fenótipos. O EOA persistente e as alergias foram associados ao maior risco de desenvolver DPOC, enquanto o LOA e as alergias foram associados a um maior risco de multimorbilidades, incluindo diabetes, obesidade e doenças cardiovasculares.
A asma e as comorbilidades relacionadas podem ter mecanismos moleculares comuns, exposições comuns ou predisposições genéticas comuns, segundo a hipótese dos autores. As comorbilidades (DPOC, DRGE, doenças cardiovasculares), que estão normalmente associadas a uma assinatura de inflamação T2 baixa, podem assim também desenvolver-se em doentes com um estado T2 inicialmente elevado.
As alterações e a possível evolução para um fenótipo diferente podem resultar num mau controlo clínico, na insensibilidade aos esteróides e no agravamento da gravidade. Ao definir o fenótipo da asma com base nos biomarcadores actuais, os médicos devem, por conseguinte, ser mais cautelosos e procurar também sobreposições entre diferentes fenótipos, especialmente em doentes com asma insensíveis aos esteróides e difíceis de tratar, concluem os investigadores.
Literatura:
- Ricciardolo FLM, Guida G, Bertolini F, et al: Sobreposição de fenótipos na história natural da asma. European Respiratory Review 2023; 32: 220201; doi: 10.1183/16000617.0201-2022.
InFo PNEUMOLOGY & ALLERGOLOGY 2024; 6(1): 36-38