As múltiplas manifestações da doença do lúpus eritematoso sistémico (LES) são essencialmente uma consequência de auto-anticorpos, complexos imunes e citocinas. As novas terapias intervêm especificamente na imunopatogénese da doença autoimune complexa. Durante muito tempo, o belimumab foi o único medicamento biológico aprovado especificamente para o LES. Entretanto, um outro anticorpo monoclonal, o anifrolumab, foi aprovado nesta área de indicação e muitos outros candidatos a medicamentos estão atualmente a ser investigados. No que diz respeito a uma estratégia de tratamento personalizada, a identificação de biomarcadores está a tornar-se cada vez mais importante.
Tendo em conta o espetro alargado de opções de tratamento, é cada vez mais importante identificar fenótipos específicos de LES que respondam a uma determinada estratégia terapêutica, explicou o Prof. Martin Aringer, MD, University Hospital Dresden (D) [1]. De acordo com os actuais critérios de classificação EULAR/ACR, o critério de entrada para o lúpus eritematoso sistémico (LES) é a deteção de anticorpos antinucleares (ANA) positivos [2,3,13]. Outros parâmetros imunológicos, como os factores do complemento – os níveis séricos do complemento (C3/C4) estão frequentemente diminuídos na doença ativa – são também importantes, mas têm uma sensibilidade inferior à dos ANA, pelo que fazem simplesmente parte dos critérios ponderados**. Estes últimos estão associados a domínios que estão associados a diferentes manifestações de LES.
** Valor de corte de 10 pontos
As células B e as vias de sinalização do interferão no centro da investigação
A etiopatogénese do LES ainda não está totalmente esclarecida. Mas nas últimas décadas, foram identificados alguns mecanismos que estão correlacionados com o LES [4]. Trata-se, nomeadamente, de
- Factores que contribuem para a ativação das células B ou para a sobrevivência das células B auto-reactivas
- Perturbações na eliminação de material celular apoptótico que contém muitos auto-antigénios associados ao LES.
- Influência crónica do interferão como “sinal de perigo viral
Parte-se do princípio de que os auto-anticorpos patogénicos actuam em parte diretamente nas células e podem ativar os macrófagos sob a forma de complexos imunes e com a ajuda do complemento, que alimentam a reação inflamatória através de citocinas pró-inflamatórias. Além disso, os auto-anticorpos contribuem para a sobrevivência dos linfócitos auto-reactivos e para a formação de mais auto-anticorpos através da citocina das células B BLyS/BAFF, bem como dos interferões, num ciclo de feedback positivo [4]. Nas últimas décadas, foram desenvolvidos vários novos fármacos imunomoduladores. E espera-se que os estudos “poli-ómicos” em grande escala (genómica, proteómica e metabolómica) forneçam mais informações relevantes para a terapia sobre os mecanismos imunológicos centrais [5].
Os produtos biológicos como um farol de esperança – a seleção de terapias passa para o centro das atenções
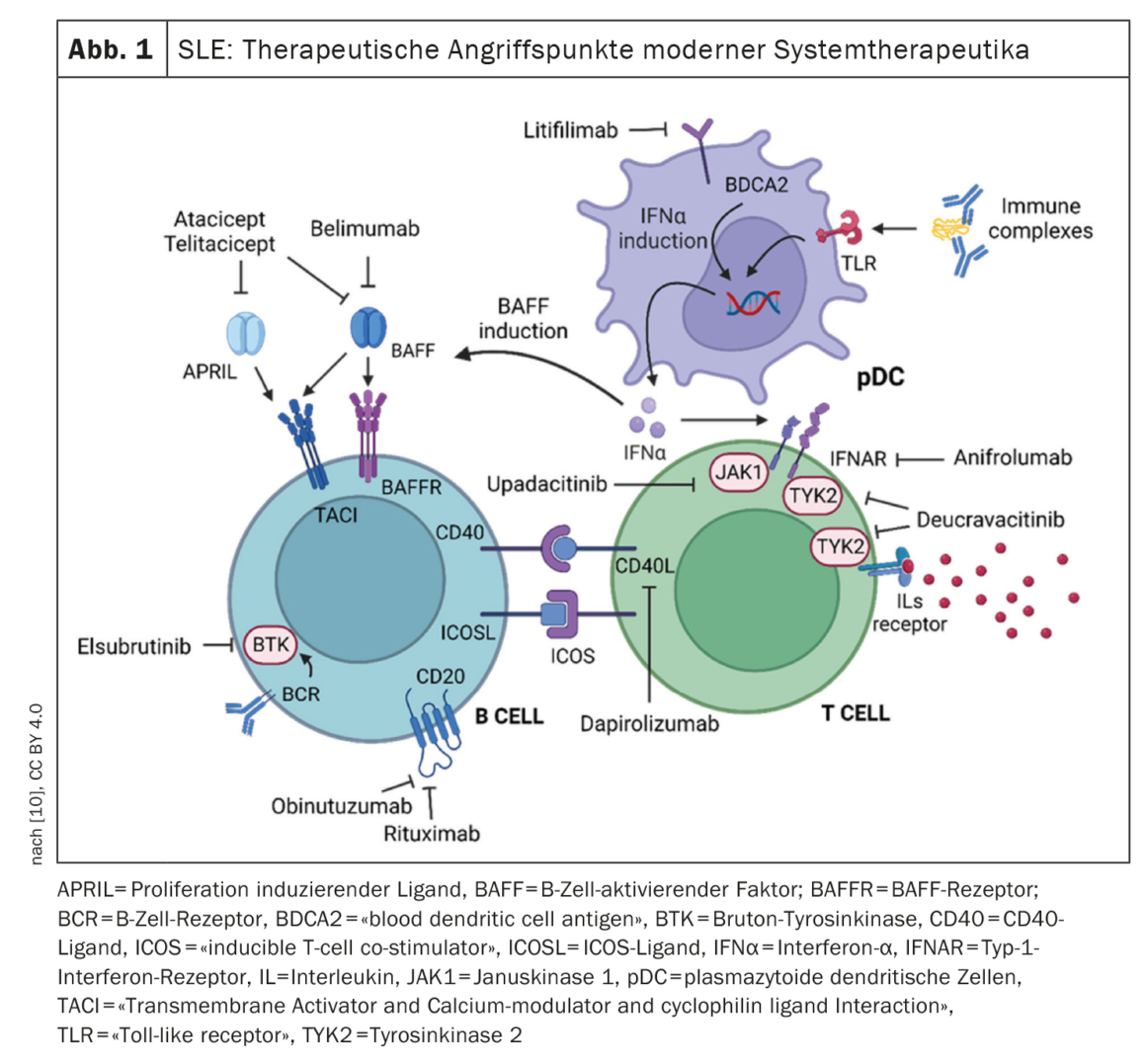
O LES é considerado uma doença autoimune mediada por células B. O rituximab é uma terapia de depleção de células B que impede a formação de plasmablastos. Apesar da evidência de eficácia em alguns estudos, o rituximab não foi oficialmente aprovado na Suíça na área de indicação do LES. No entanto, mediante pedido, a companhia de seguros de saúde pode conceder uma aprovação de custos [6]. O primeiro medicamento biológico aprovado especificamente para o LES foi o belimumab, um inibidor da enzima BLyS. Ao inibir BAFF/BLyS, o belimumab provoca um bloqueio seletivo da ativação das células B. O belimumab reduz o número de células B naïve e activadas e, consequentemente, o número de plasmablastos, o que leva a uma diminuição dos níveis de auto-anticorpos e a uma melhoria dos níveis de complemento C3 e C4 [7]. Os produtos biológicos podem catalisar a redução dos sintomas. Mas não só: “O belimumab e o anifromulab podem ajudar a eliminar gradualmente os glucocorticóides e foram testados em diferentes populações de estudo”, afirma o Professor Dimitrios T. Boumpas, médico do Departamento de Medicina da Universidade Nacional e Kapodistrian de Atenas [8]. O anifrolumab foi aprovado com base nos resultados dos ensaios TULIP [9]. Foi demonstrado que a eficácia do anifrolumab está positivamente correlacionada com níveis séricos elevados de IFN [9]. Tanto o belimumab como o anifrolumab demonstraram ser superiores em comparações com placebo em doentes com LES com marcadores serológicos desviantes na linha de base (C3/C4 e/ou anti-ds DNA). O belimumab foi testado em ensaios aleatórios em diferentes populações. Para além dos produtos biológicos já aprovados belimumab e anifrolumab, existem dados promissores de fase II sobre iberdomida, litifilimab e deucravacitinib. Além disso, estão a ser investigados vários outros candidatos a medicamentos [10] (Fig. 1) .
Congresso: Reunião Anual da EULAR
Literatura:
- “Dr. Martin Aringer, Hospital Universitário de Dresden, Reunião Anual da EULAR, 31.05.-03.06.2023.
- Aringer M, et al: 2019 European League Against Rheumatism/American College of Rheumatology critérios de classificação para lúpus eritematoso sistémico. Arthritis Rheumatol 2019; 71: 1400-1412.
- Aringer M, et al: 2019 European League Against Rheumatism/American College of Rheumatology critérios de classificação para lúpus eritematoso sistémico. Ann Rheum Dis 2019; 78: 1151-1159.
- Aringer M, Finzel S, Voll RE: Imunopatogénese do lúpus eritematoso sistémico. Z Rheumatol 2022. https://doi.org/10.1007/s00393-022-01214-4
- Aringer M, et al: Um vislumbre do futuro do lúpus eritematoso sistémico. Ther Adv Musculoskelet Dis 2022; 14: 1759720X221086719.
- Revista para pessoas afectadas pelo Lúpus Eritematoso, 1/2017; www.lupus-suisse.ch,(último acesso em 23.06.2023)
- Hiepe F: Novos conhecimentos sobre a patogénese do LES e as suas implicações para o desenvolvimento de novos conceitos terapêuticos. Ato Reumatol 2020; 45: 328-333
- “How to treat Lupus”, Professor, Dimitrios T. Boumpas, MD, Reunião Anual da EULAR, 31.05.-03.06.2023.
- Morand EF, et al; Investigadores do ensaio TULIP-2. Ensaio de Anifrolumab em Lúpus Eritematoso Sistémico Ativo. N Engl J Med 2020; 382(3): 211-221.
- Venturelli V, Isenberg DA: Targeted Therapy for SLE-What Works, What Doesn’t, What’s Next. Journal of Clinical Medicine 2023; 12(9): 3198.
www.mdpi.com/2077-0383/12/9/3198,(último acesso em 23.06.2023) - Ruiz-Irastorza G, Gertsias G: Rheumatology (Oxford) 2020; 59(Suppl. 5): v69-v81.
- Choi ST, et al: Análise de subescalas de qualidade de vida em pacientes com lúpus eritematoso sistémico: associação com depressão, fadiga, atividade da doença e danos. Clin Exp Rheumatol 2012; 30: 665-672.
- Fanouriakis A, et al: Atualização de 2019 das recomendações da EULAR para a gestão do lúpus eritematoso sistémico. Ann Rheum Disease 2019; 78: 736-745.
- Miyazaki C, et al: Padrões de tratamento e custo médico de pacientes com lúpus eritematoso sistémico no Japão: um estudo retrospetivo de base de dados de reclamações. J Med Econ 2020; 23: 786-799.
HAUSARZT PRAXIS 2023; 18(7): 32-33 (publicado em 12.7.23, antes da impressão).