O metilfenidato tem sido utilizado no tratamento do ADHD há décadas. Há diferentes hipóteses sobre como exactamente este psicoestimulante desdobra os seus efeitos. Um destes relaciona-se com o metilfenidato que afecta a neurotransmissão dopaminérgica nos núcleos acumbens e redes neuronais associadas. Para saber mais, uma equipa de investigação realizou um estudo de imagem.
O metilfenidato (MPH) é o medicamento de eleição para o tratamento da perturbação de hiperactividade com défice de atenção clinicamente relevante (ADHD) [1]. Ritalin® é a marca da mais antiga e mais comum preparação de MPH. Outros medicamentos utilizados na Suíça que também contêm a substância activa MPH são Medikinet MR®, Equasym®, Focalin® e Concerta® [2]. É feita uma distinção entre preparativos de acção curta e longa. É frequentemente utilizada uma preparação de MPH de curta duração no início do tratamento, por exemplo, o comprimido de Ritalin® 10 mg. O MPH nesta forma é rapidamente absorvido pelo corpo e começa a ter efeito após cerca de 30 minutos. Após 3-4 horas, o efeito desvanece-se rapidamente. Além disso, existe a possibilidade de administrar estimulantes numa forma de acção prolongada. Aqui, o princípio activo é libertado do comprimido com um atraso, e o efeito é mantido durante 7 a um máximo de 14 horas, dependendo da preparação. No entanto, a informação sobre a duração da acção é apenas uma orientação; a terapia pode ser adaptada da melhor forma possível às necessidades da criança [3].
Exame de ressonância magnética num desenho de crossover
Os investigadores realizaram um estudo cruzado aleatório, controlado por placebo e duplo-cego no Hospital Universitário de Fukui (Japão) [4]. A idade média das 27 crianças com TDAH era de 10,6 anos (SD 1,8; faixa etária: 7,3-15,5 anos). Nos 49 sujeitos de controlo sem TDAH, a idade média era de 11,1 anos (SD 2,3; faixa etária 6,1-15,6 anos). Os critérios de inclusão são mostrados na caixa. As crianças com ADHD foram digitalizadas duas vezes com ressonância magnética funcional em repouso sob condições de metilfenidato e placebo. Durante a primeira consulta, foram administrados MPH (1,0 ± 0,1 mg/kg) ou placebo (lactose) com libertação osmótica (OROS), como em estudos anteriores em condições de dupla ocultação. Cinco a oito horas após a administração, quando a concentração de MPH no sangue é máxima, as crianças foram submetidas a um exame de fMRI em estado de repouso e realizaram um teste de desempenho contínuo padronizado fora do aparelho de fMRI. Na segunda consulta (dentro de 1 a 6 semanas após a primeira consulta), as crianças com TDAH foram submetidas a um exame de fMRI em estado de repouso e realizaram o teste de desempenho após tomarem a segunda medicação: as crianças que tinham tomado OROS-MPH na primeira consulta receberam o placebo na segunda consulta em condições de dupla ocultação e vice-versa.
O grupo de controlo, ou seja, os participantes no estudo sem TDAH, completaram o mesmo scan fMRI em repouso uma vez sem OROS-MPH ou placebo.

Foi demonstrado que o metilfenidato modula a actividade neuronal
Foi demonstrado que o metilfenidato (MPH) aumentava a actividade neuronal espontânea nos núcleos acumbens e nas redes de saliência e de modo padrão [4].
- No teste de desempenho, o MPH reduziu significativamente os erros de omissão, o tempo médio de reacção e a variabilidade da resposta intra-individual durante uma tarefa (IIRV) no grupo ADHD (cada p<0,001).
- A modulação induzida pelo metilfenidato da actividade neuronal espontânea na rede de modo padrão previu o efeito de tratamento em termos de variabilidade da resposta intra-individual (IIRV) (r=-0,46, p=0,016).
- Relativamente aos efeitos do MPH na actividade neuronal espontânea no núcleo acumbens, a amplitude das flutuações de baixa frequência (ALFF) no núcleo direito acumbens foi significativamente maior na condição de ADHD-MPH do que na condição de ADHD-placebo (p<0,05, Bonferroni-corrigido, Cohen’s d=0,55).
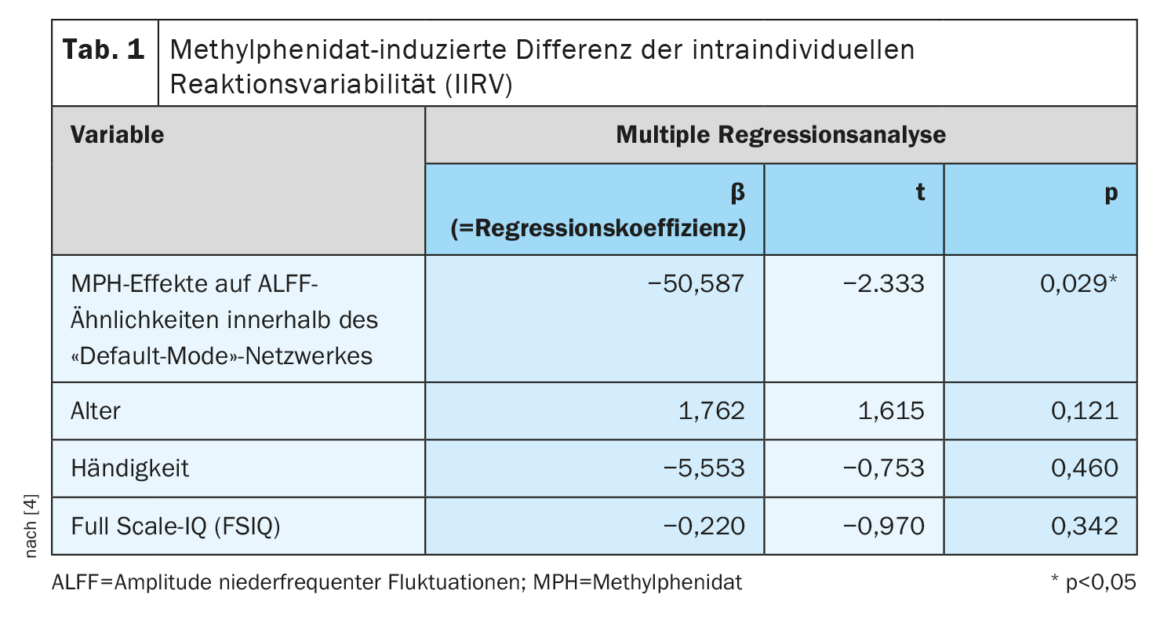
- ALFF foi significativamente mais elevado nas redes de saliência (SN) e no modo de rede padrão (DMN) na condição ADHD-MPH do que na condição ADHD-placebo (SN: p<0,05, Cohen d=0,57; DMN: p<0,01, Cohen d=0,66; Bonferroni corrigido em cada caso). Não houve diferença significativa na rede frontoparietal esquerda e direita (p>0,05). A análise de regressão linear múltipla revelou que apenas a modulação MPH do padrão de semelhança ALFF dentro da rede de modo padrão estava significativamente associada aos efeitos da droga na variabilidade da resposta intra-individual (Tabela 1) . Isto indica que se trata de um mecanismo de acção neurobiológica crucial.
Estas descobertas expandem a actual compreensão dos mecanismos neurobiológicos subjacentes ao tratamento de MPH em crianças com TDAH e, de acordo com os autores do estudo, podem no futuro permitir que biomarcadores clinicamente úteis sejam derivados para avaliar o sucesso do tratamento.
Literatura:
- Praxis Suchtmedizin Schweiz, www.praxis-suchtmedizin.ch/praxis-suchtmedizin/index.php/de/medikamente/einleitung-mh, (último acesso 10.02.2023)
- Swissmedic: Arzneimittelinformation, www.swissmedicinfo.ch, (último acesso 10.02.2023)
- «Die medikamentöse Behandlung von Kindern und Jugendlichen mit einer Aufmerksamkeitsdefizit-Hyperaktivitätsstörung ADHS», März 2022,
www.pukzh.ch/sites/default/assets/File/
Informationen%20Stimulanzien%20und%20Ritalin.pdf, (último acesso 10.02.2023) - Mizuno Y, et al.: Methylphenidate Enhances Spontaneous Fluctuations in Reward and Cognitive Control Networks in Children With Attention-Deficit/Hyperactivity Disorder. Biological Psychiatry: Cognitive Neuroscience and Neuroimaging, available online 23 October 2022, www.sciencedirect.com/science/article/pii/S2451902222002476, (último acesso 10.02.2023)
HAUSARZT PRAXIS 2023; 18(2): 24–25
InFo NEUROLOGIE & PSYCHIATRIE 2023; 21(2): 30–31