Embora a demência não seja uma das doenças neurológicas mais comuns, é já hoje um problema relevante e tornar-se-á significativamente mais importante devido à evolução demográfica.
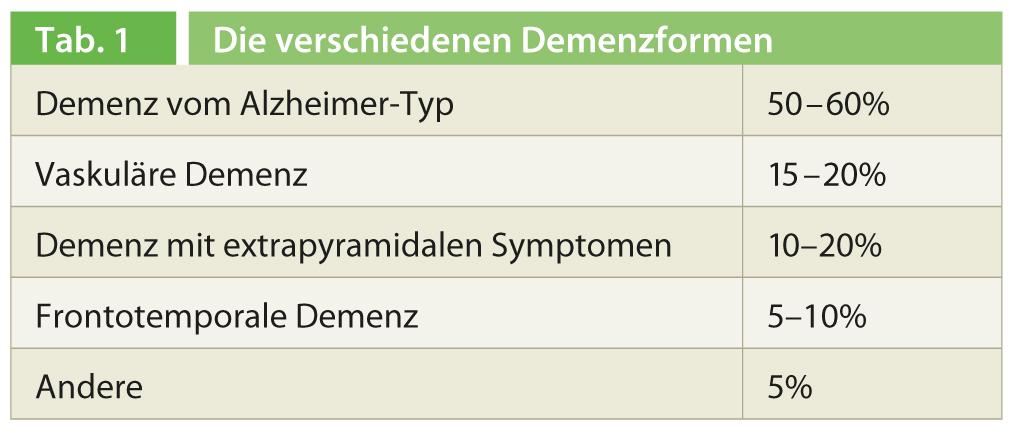
A demência é uma doença cerebral crónica progressiva com perturbações em várias esferas cognitivas tais como memória, pensamento, orientação, compreensão, cálculo, capacidade de aprendizagem, linguagem, fala e julgamento. A consciência das pessoas com demência não é turvada e a percepção sensorial é preservada; por outro lado, mudanças no controlo emocional, comportamento social e/ou motivação podem ser observadas com os correspondentes efeitos na vida quotidiana. De acordo com a definição do CID-10, esta condição deve persistir durante um período de pelo menos seis meses para que se possa fazer um diagnóstico de demência. Para além da cognição, a demência afecta várias competências quotidianas e funções corporais. Com 50-60%, a demência do tipo Alzheimer é de longe a forma mais comum de demência (Quadro 1).
Diagnósticos
“No diagnóstico da demência, é procurado como praticante. Conhece os pacientes e as suas famílias, e é normalmente o primeiro ponto de contacto quando o comportamento de uma pessoa muda”, diz o Prof. Hans Jung, MD, Hospital Universitário de Zurique. Para além do historial médico e do historial de outros, as seguintes medidas podem ser facilmente realizadas para um rastreio inicial da demência em qualquer prática:
- a recolha de um relatório interno, neurológico e psicopatológico orientadores,
- Testes laboratoriais básicos (electrólitos, valores da tiróide, valores renais, vitamina B12, ácido fólico, VIH, sífilis) e
- um ou mais testes curtos padronizados (Mini-Mental-State, Teste do Relógio).
Se necessário, é também aconselhável organizar a imagiologia. Dependendo da situação, outras medidas de diagnóstico, tais como testes neurofisiológicos mais detalhados, podem ser tomadas em cooperação com um especialista. “Especialmente em pacientes mais jovens – e com isso quero dizer pacientes com idade inferior a 65 ou 70 (!) – bem como em casos de incerteza diagnóstica, o diagnóstico do LCR, um EEG ou outras imagens com PET ou SPECT também podem ser indicados”, continua o Prof. Jung. No diagnóstico do LCR, os valores de inflamação, tau, phospho-tau, β-amilóide e proteína 14-3-3) são de particular interesse.
Os sintomas precoces, tais como ligeiras deficiências cognitivas que afectam apenas a memória, podem, em determinadas circunstâncias, ser presságios da demência de Alzheimer. 20-30% dos pacientes com o chamado MCI (Mild Cognitive Imp airement) acabam por desenvolver a demência por Alzheimer. Teoricamente, seria possível identificar pacientes que desenvolverão demência por Alzheimer nesta fase inicial através de marcadores específicos no líquido cefalorraquidiano e no PET/SPECT, mas isto não é prático enquanto não houver tratamento preventivo disponível.
Opções terapêuticas
Apesar da investigação intensiva, até à data só estão disponíveis medicamentos para tratamento sintomático, para além do apoio psicossocial aos pacientes e suas famílias. Podem ser demonstrados efeitos positivos significativos nos sintomas da demência para os inibidores da acetilcolinesterase (rivastigmina, galantamina, donezepil), bem como para a memantina. As primeiras são indicadas para a demência de Alzheimer leve a moderada, as segundas para a demência de Alzheimer moderada a grave.
Com a ajuda de inibidores de acetilcolinesterase, a transmissão colinérgica no cérebro, que é reduzida na demência de Alzheimer, pode ser novamente melhorada. Embora o curso da doença não possa ser interrompido, a condição pode ser significativamente melhorada e estabilizada, de modo a que o início da independência e a necessidade de cuidados possam ser adiados [1, 2]. Se existirem défices relevantes, um ensaio com estes medicamentos deve, portanto, ser realizado relativamente cedo após o diagnóstico.
Efeitos colinérgicos secundários como náuseas, vómitos e diarreia são relativamente comuns entre os inibidores da acetilcolinesterase, mais frequentemente com a rivastigmina, embora isto só se aplique à formulação oral. Sob a mancha de rivastigmina, que está disponível há vários anos, a taxa de efeito secundário é significativamente mais baixa e apenas minimamente mais alta do que sob placebo [3]. Além disso, o adesivo está disponível em duas doses (9,5 mg/24h e 13,3 mg/24h), de modo a que um benefício adicional em termos de eficácia possa ser alcançado com a dose mais elevada do adesivo enquanto a taxa de efeito secundário permanece a mesma [4].
A Memantine é particularmente eficaz nas fases média e tardia da demência de Alzheimer e pode contribuir para uma melhoria significativa da situação dos cuidados, influenciando positivamente as perturbações comportamentais. “Estudos mostram claramente que uma combinação de memantina com um inibidor de acetilcolinesterase seria útil, mas infelizmente esta combinação ainda não foi aprovada, razão pela qual se tem de a requerer individualmente em cada caso”, concluiu o orador [5].
Fonte: Lunchsymposium, Medidays 2013, 2-6 de Setembro de 2013, Hospital Universitário de Zurique.
Literatura:
- Birks J: inibidores da colinesterase para a doença de Alzheimer. Cochrane Database of Systematic Reviews 2006: CD005593.
- Birks J: Os inibidores da colinesterase (ChEIs), donepezil, galantamina e rivastigmina são eficazes para a doença de Alzheimer leve a moderada. Resumos Cochrane. Publicado online: 16 de Maio de 2012.
- Winblad B, et al: Preferência do cuidador pelo adesivo de rivastigmina em relação às cápsulas para o tratamento da provável doença de Alzheimer. Int J Geriatr Psiquiatria 2007; 22: 485-491.
- Cummings J, et al: Estudo aleatório, duplo-cego, grupo paralelo, 48 semanas para a eficácia e segurança de uma mancha de rivastigmina de dose superior (15 vs. 10 cm2) na doença de Alzheimer. Dement Geriatr Cogn Disord 2012; 33: 341-353.
- Farrimond LE, et al: Memantine and cholinesterase inhibitor combination therapy for Alzheimer’s disease: a systematic review. BMJ Open 2012;2. pii: e000917.
HAUSARZT PRAXIS 2013, Vol. 8, no. 9











