Na reunião anual da ASCO deste ano foram apresentados alguns estudos empolgantes sobre carcinoma de células renais. Especialmente no caso de tumores localizados, a prática clínica poderá mudar num futuro próximo. Pela primeira vez, os inibidores de pontos de controlo parecem ser uma opção eficaz para a terapia adjuvante. E há também novas descobertas no tratamento da primeira e segunda linha do carcinoma avançado de células renais.
Há anos que a investigação tem vindo a investigar potenciais terapias adjuvantes para o carcinoma das células renais – até agora sem sucesso. Infelizmente, nenhum progresso pôde ser alcançado através do uso de inibidores da tirosina cinase. Por exemplo, há uma série de estudos que mostraram não ter ou ter apenas um benefício mínimo de sobrevivência do tratamento adjuvante com sunitinibe, sorafenibe, pazopanibe e axitinibe – com uma toxicidade considerável [1–5]. Na reunião anual da ASCO, a Keynote-564 foi o primeiro estudo a apresentar um tratamento adjuvante promissor após a nefrectomia. Isto poderá mudar em breve a prática clínica para sempre. Actualmente, só se recomenda o seguimento do tumor após a nefrectomia, independentemente do tamanho e da classificação do tumor. No entanto, sabe-se há algum tempo que estes factores têm uma influência significativa sobre o prognóstico [6]. Por conseguinte, é evidente que especialmente os doentes do grupo de alto risco – por exemplo, aqueles com sarcomatóides desdiferenciados ou grandes tumores – poderiam beneficiar de tratamento adjuvante após a nefrectomia.
Terapia adjuvante: concentração nos inibidores de pontos de controlo
Enquanto no decurso da última década foram investigados principalmente os inibidores de tirosina quinase no contexto do adjuvante, agora o foco está agora na imunoterapia utilizando inibidores de ponto de controlo. Actualmente, estão em curso quatro ensaios que investigam o uso de pembrolizumab, atezolizumab e nivolumab como monoterapia ou em combinação com ipilimumab (tab. 1). Embora os critérios de inclusão fossem ligeiramente diferentes para todos os estudos, o foco está sempre nos doentes dos grupos intermediários e de alto risco. Uma característica especial tanto do estudo Keynote 564 como do estudo IMmotion010 é que os doentes após uma cirurgia metastática bem sucedida dentro do primeiro ano após o diagnóstico primário também poderiam ser incluídos.
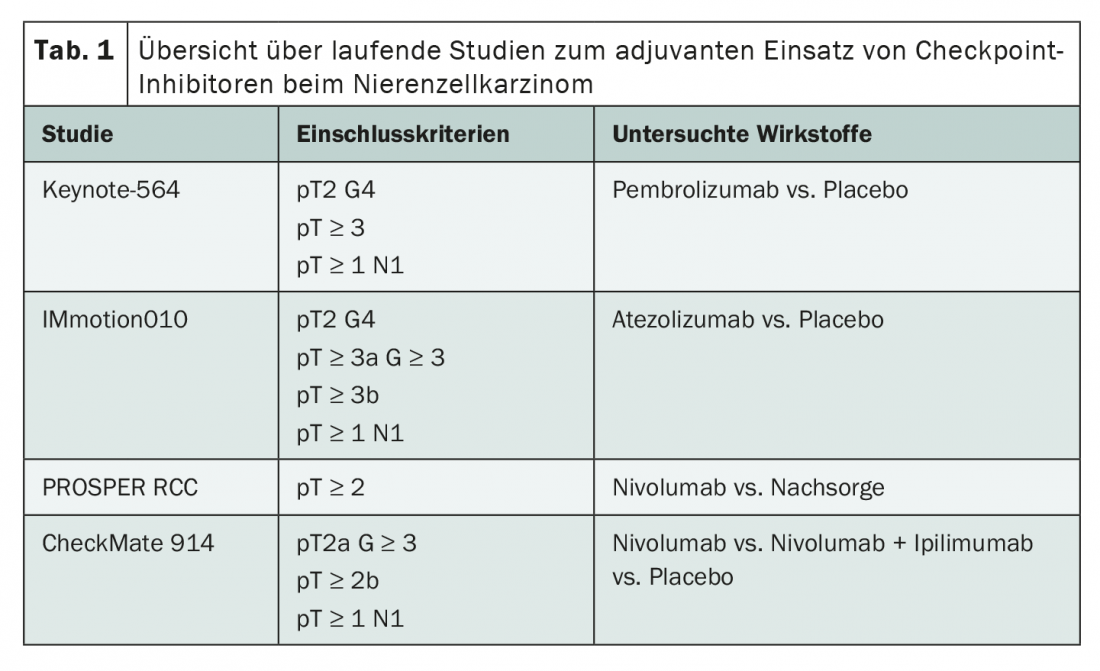
Os resultados iniciais da Keynote-564 foram agora apresentados na reunião anual da ASCO [7]. No estudo da fase III, os pacientes incluídos receberam pembrolizumab ou placebo durante um ano após a nefrectomia. O tempo médio de seguimento foi de 24,1 meses. Tanto a sobrevivência sem doença (DFS) como a sobrevivência global (OS) mostraram vantagens estatisticamente significativas do tratamento adjuvante com pembrolizumab – apesar do período de seguimento ainda relativamente curto. Assim, a taxa DFS a 24 meses era de 77,3%, em comparação com 68,1% no braço de controlo (hazard ratio 0,68, p=0,001). A taxa de OS a 24 meses era de 96,6% no grupo de intervenção e 93,5% com placebo (hazard ratio 0,54, p=0,0164). Estes efeitos estavam presentes e eram semelhantes em todos os subgrupos. Os pacientes que tinham sido anteriormente submetidos a metastasectomia com sucesso pareciam beneficiar particularmente da imunoterapia adjuvante. Não houve surpresas no que respeita à compatibilidade. Como se esperava dos estudos de monoterapia, ocorreram efeitos secundários graves em cerca de 20% dos doentes, o que correspondeu ao espectro conhecido de efeitos secundários do pembrolizumabe. Faltam ainda dados mais maduros do ensaio Keynote 564, bem como os resultados iniciais dos outros ensaios de imunoterapia, a fim de avaliar os efeitos reais do tratamento. Contudo, após muitos anos sem sucesso, poderia agora surgir uma opção para a terapia adjuvante do carcinoma de células renais, especialmente para doentes de alto risco.
Carcinoma avançado de células renais: terapia de primeira linha em transição
Foram também apresentadas várias descobertas na Reunião Anual da ASCO no domínio da terapia de primeira linha para o carcinoma avançado de células renais. Com a introdução de várias terapias combinadas de imunoterapêutica e inibidores da tirosina quinase, o tratamento está em curso. Actualmente, são recomendadas diferentes terapias dependendo do perfil de risco (Tab. 2) [8]. Recentemente, o inibidor de tirosina quinase de terceira geração (TKI) cabozantinibe também foi aprovado em combinação com nivolumab para tratamento de primeira linha; esta opção ainda não está coberta na directriz. Existe também uma boa base de dados para o tratamento com lenvatinib + pembrolizumab, embora a aprovação ainda esteja pendente [9,10]. Actualmente, o lenvatinib só é aprovado na Suíça para terapia de segunda linha após os inibidores VEGF [11].
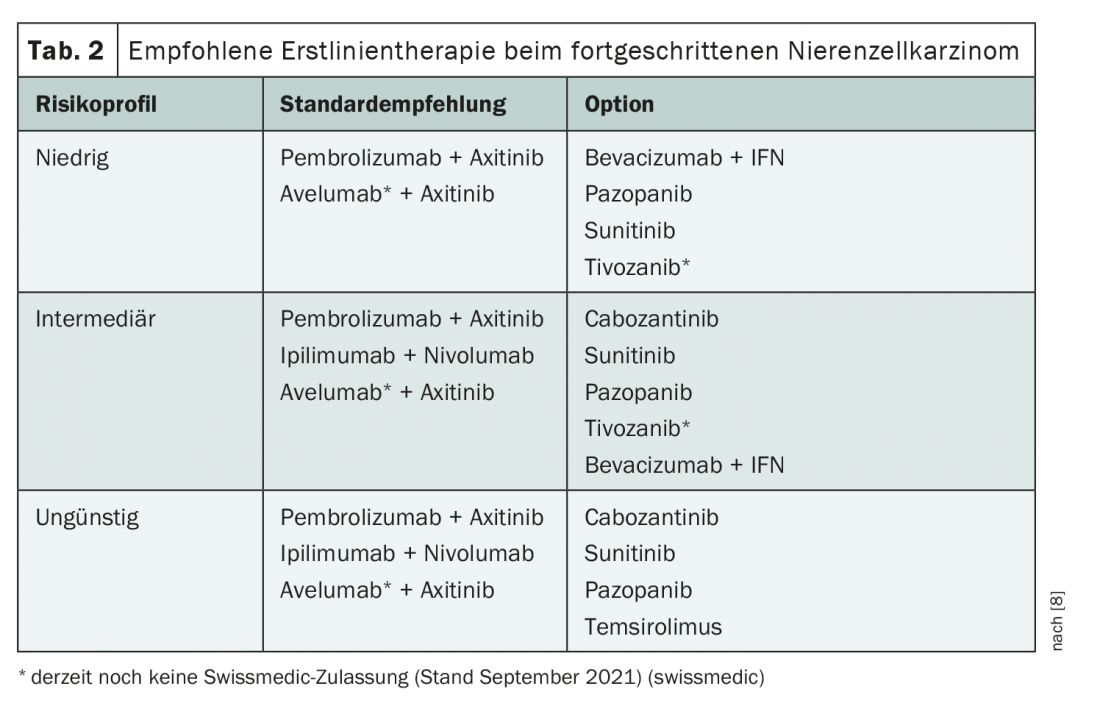
Entre as diferentes opções, o foco está actualmente na questão de saber se as combinações TKI-imunoterapeuticas (IO) também podem manter-se a longo prazo com a combinação IO-IO nivolumab/ipilimumab, para a qual já existe um período de seguimento mais longo. Até agora, os dados para as combinações nivolumab/ipilimumab, axitinib/pembrolizumab, cabozantinib/nivolumab e também para a combinação ainda não aprovada lenvatinib/pembrolizumab mostram resultados semelhantes em relação à sobrevivência com uma razão de perigo de cerca de 0,66 em comparação com a monoterapia usando sunitinib [9,12–16]. Contudo, falta um acompanhamento a longo prazo para as combinações IO-TKI. Um foi apresentado para axitinib/pembrolizumab na reunião anual da ASCO deste ano [15]. Houve taxas semelhantes de OS e PFS nos diferentes momentos, como nos ensaios da combinação nivolumab/ipilimumab da IO-IO. Após 36 meses, a taxa de PFS com ambas as terapias era de cerca de 30% [14,15]. Esta é certamente uma boa notícia, mas ainda estão por ver mais dados sobre a duração da resposta. O resultado final é que o seguimento da combinação TKI-IO axitinib/pembrolizumab mostra dados consistentes até agora, sem novas preocupações de segurança.
Além disso, os dados sobre as novas combinações TKI-IO lanvatinib/pembrolizumab e cabozantinib/nivolumab foram apresentados na reunião anual da ASCO. Embora estes sejam claramente superiores à terapia solaritinibe apenas em doentes intermédios e de alto risco, os doentes com perfis de risco favoráveis têm demonstrado até agora um prolongamento significativo da PFS, mas sem efeito de OS [10,17]. Isto pode ser devido ao período de seguimento relativamente curto, mas indica que o benefício da estratégia dupla é potencialmente maior nos grupos intermediários e de alto risco do que na população de baixo risco. Se as combinações com TKIs de terceira geração irão substituir outras combinações de TKI-IO no futuro – por exemplo, aquelas com axitinib – continua a ser uma questão em aberto no presente.
Notícias da segunda linha
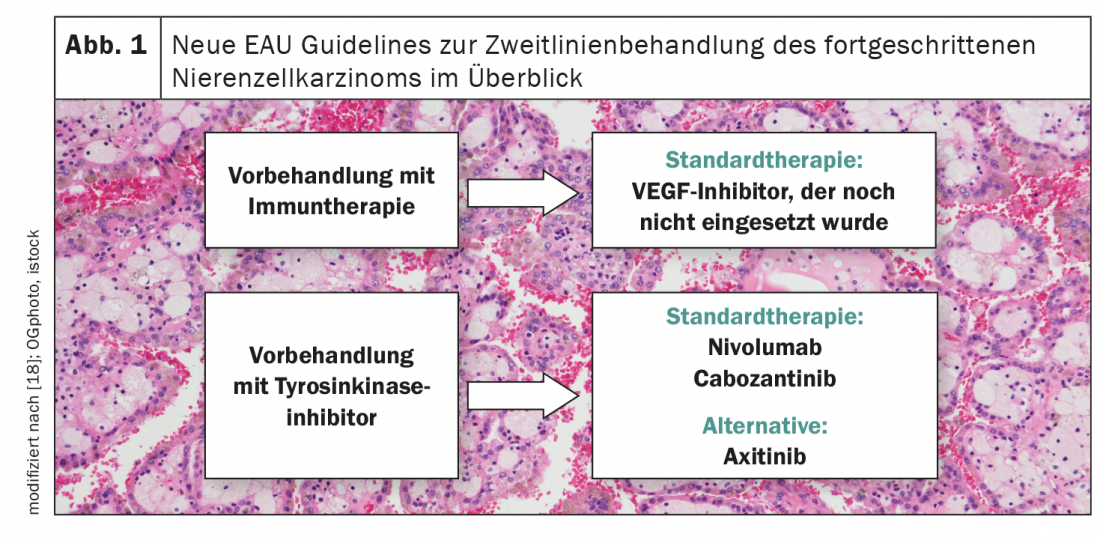
Após o insucesso da terapia de primeira linha, ainda há uma falta de recomendações sólidas no carcinoma de células renais, especialmente se a imunoterapia foi utilizada na primeira linha de tratamento (Fig. 1) [18]. Até agora, existem três estudos prospectivos neste cenário – todos com um único braço. Enquanto se observou um PFS mediano de 8,8 meses com tratamento com axitinibe, este foi de 7,4 meses com terapia de pazopanibe e 6,8 meses com administração de solaritinibe [19-21]. O estudo CANTATA apresentado na Reunião Anual da ASCO investigou a eficácia do cabozantinib/telaglenastat na segunda linha e comparou esta terapia de combinação com o cabozantinib/placebo [22]. Embora não houvesse benefício em adicionar telaglenastat, o cabozantinibe provou ser um candidato promissor para a terapia de segunda linha do carcinoma avançado de células renais. Assim, o PFS mediano no braço de controlo foi de 9,3 meses com uma taxa de resposta objectiva de cerca de 30%.
Congresso: Reunião Anual da ASCO
Literatura:
- Ravaud A, et al: Adjuvant sunitinib em carcinoma de células renais de alto risco após nefrectomia. N Engl J Med. 2016; 375(23): 2246-2254.
- Eisen TQG, et al: Análise de Eficácia Primária resulta do ensaio SORCE (RE05): Sorafenibe adjuvante para carcinoma de células renais em risco intermédio ou elevado de recidiva: um ensaio internacional, aleatório e duplo-cego fase III conduzido pela UTC MRC na UCL. ESMO Congress 2019, Proffered Paper 2 – Genitourinary tumours, non-prostate, Abstract #2483.
- Motzer RJ, et al: Ensaio Fase III Aleatório de Pazopanibe Adjuvante Versus Placebo após Nefrectomia em Pacientes com Carcinoma de Células Renais Localizadas ou Localmente Avançadas. J Clin Oncol. 2017; 35(35): 3916-3923.
- Haas NB, et al: Adjuvant sunitinib ou sorafenib para carcinoma de alto risco, não-metastático de células renais (ECOG-ACRIN E2805): um ensaio duplo-cego, controlado por placebo, aleatorizado, fase 3. Lanceta. 2016; 387(10032): 2008-2016.
- Gross-Goupil M, et al: Axitinib vs placebo em doentes com alto risco de carcinoma recorrente de células renais (CCR): Resultados do ensaio ATLAS. ESMO Congress 2018, Proffered paper session – Genitourinary tumours, non prostate, Abstract #1286.
- Gettman MT, et al: Pathologic staging of renal cell carcinoma: significance of tumour classification with the 1997 TNM staging system. O cancro. 2001; 91(2): 354-361.
- Choueiri TK, et al: Pembrolizumab versus placebo como terapia adjuvante pós-nefrectomia para doentes com carcinoma de células renais: estudo aleatório, duplo-cego, fase III KEYNOTE-564. Reunião Anual ASCO 2021, Abstract #LBA5.
- AWMF: S3-Leitlinie Diagnostik, Therapie und Nachsorge des Nierenzellkarzinoms, Langversion 2.0, Stand August 2020.
- Motzer R, et al: Lenvatinib mais pembrolizumab ou everolimus para carcinoma avançado de células renais. N Engl J Med. 2021; 384(14): 1289-1300.
- Grünwald V, et al.: Análise do estudo CLEAR em doentes (pts) com carcinoma avançado de células renais (RCC): Profundidade de resposta e eficácia para subgrupos seleccionados nos braços de tratamento com lenvatinibe (LEN) + pembrolizumab (PEMBRO) e sunitinibe (SUN). Reunião Anual da ASCO 2021, Resumo #4560.
- www.swissmedicinfo.ch (último acesso: 15.09.2021)
- Albiges L, et al.: Nivolumab plus ipilimumab versus sunitinib para o tratamento de primeira linha do carcinoma avançado de células renais: seguimento prolongado de 4 anos do ensaio CheckMate 214 fase III. ESMO Aberto. 2020; 5(6): e001079.
- Choueiri TK, et al: Nivolumab + cabozantinib vs sunitinib em tratamento de primeira linha para carcinoma avançado de células renais: Primeiros resultados do ensaio CheckMate 9ER fase III aleatorizado. Anais de Oncologia. 2020; 31: S1142-1215.
- Motzer RJ, et al: Resultados de sobrevivência e avaliação de resposta independente com nivolumab mais ipilimumab versus sunitinib em doentes com carcinoma renal avançado: 42 meses de seguimento de um ensaio clínico aleatório de fase 3. J Imunotermia do cancro. 2020; 8(2).
- Rini BI, et al: Pembrolizumab (pembro) mais axitinibe (axi) versus sunitinibe como terapia de primeira linha para o carcinoma avançado de células renais claras (ccRCC): Resultados do seguimento de 42 meses da KEYNOTE-426. Reunião Anual ASCO 2021, Resumo #4500.
- Plimack ER, et al: Pembrolizumab mais axitinibe versus sunitinibe como terapia de primeira linha para o carcinoma avançado de células renais (CCR): Análise actualizada da KEYNOTE-426. Journal of Clinical Oncology. 2020; 38(15_suppl).
- Apolo AB, et al: Nivolumab plus cabozantinib (N+C) versus sunitinib (S) para carcinoma avançado de células renais (aRCC): Resultados por características da doença de base no ensaio CheckMate 9ER fase 3. Reunião Anual da ASCO 2021, Resumo #4553.
- Ljungberg B, et al.: EAU Guidelines: Renal Cell Carcinoma 2021. https://uroweb.org/guideline/renal-cell-carcinoma/ (último acesso 15.09.2021).
- Ornstein MC, et al: Regime de axitinibe individualizado para doentes com carcinoma de células renais metastásicas após tratamento com inibidores de ponto de controlo: um estudo multicêntrico, de braço único, fase 2. Lancet Oncol. 2019; 20(10): 1386-1394.
- Powles TB, et al: Um estudo fase II de doentes com carcinoma renal avançado ou metastático (mRCC) recebendo pazopanibe após tratamento prévio com inibidores de ponto de controlo. Anais de Oncologia. 2020; 31: S564.
- Grande E, et al: ensaio INMUNOSUN-SOGUG: Um estudo prospectivo de fase II para avaliar a eficácia e segurança do sunitinib como tratamento de segunda linha (2L) em doentes (pts) com cancro de células renais metastásicas (CCR) que receberam antecipadamente uma combinação baseada em imunoterapia. Journal of Clinical Oncology. 2020; 38(15_suppl).
- Tannir NM, et al: CANTATA: Análise primária de um ensaio global, aleatório, controlado por placebo (Pbo), duplo-cego de telaglenastat (CB-839) + cabozantinibe versus Pbo + cabozantinibe em doentes com carcinoma renal avançado/metastático (mRCC) (pts) que progrediram em terapias inibidoras do ponto de controlo imunitário (ICI) ou anti-angiogénicas. Reunião Anual da ASCO 2021, Resumo #4501.
InFo ONCOLOGy & HEMATOLOGy 2021; 9(4): 33-34