A demência vascular (VaD) é a segunda causa mais comum de demência após a demência de Alzheimer e, portanto, a forma não neurodegenerativa mais comum de demência. Não se trata de uma doença singular. De particular importância clínica é a microangiopatia cerebral frequentemente associada à hipertensão, que pode levar à demência vascular isquémica subcortical (SIVD). Esta é provavelmente a forma mais bem caracterizada de VaD e caracteriza-se menos por perturbações da memória do que por perturbações nas funções executivas e na velocidade de processamento. O diagnóstico é baseado em particular em exames anamnésticos, clínicos e de imagem. Em qualquer caso, deve ser feito numa fase inicial.
Num futuro próximo, no contexto da evolução demográfica nas nações industriais ocidentais, é de esperar uma prevalência crescente de doenças demenciais. Devido às implicações médicas e socioeconómicas resultantes, a “Estratégia Nacional para a Demência 2014-2017” suíça foi recentemente adoptada pelo Gabinete Federal de Saúde Pública [1].
Para além da demência de Alzheimer (AD), que é a causa mais comum de demência, as demências vasculares (VaD) desempenham um papel importante como segunda forma mais comum e causa mais frequente de formas não neurodegenerativas de demência [2,3]. Os homens – em contraste com a AD – são afectados cerca do dobro das vezes que as mulheres. As possíveis causas de VaD estão resumidas no Quadro 1 para referência. AD e VaD, bem como a demência mista, são responsáveis por até 80% das demências. Estas últimas incluem não raras sobreposições entre AD e VaD. Os processos vasculares também desempenham um papel significativo no desenvolvimento da demência no contexto da AD [4–7], de modo que hoje em dia ambas as formas são também consideradas como um continuum.
Classificação da demência vascular
O VaD não é uma doença única, mas um termo geral para uma variedade de doenças cerebrovasculares que podem levar a uma deficiência cognitiva e mesmo à demência (Quadro 1).

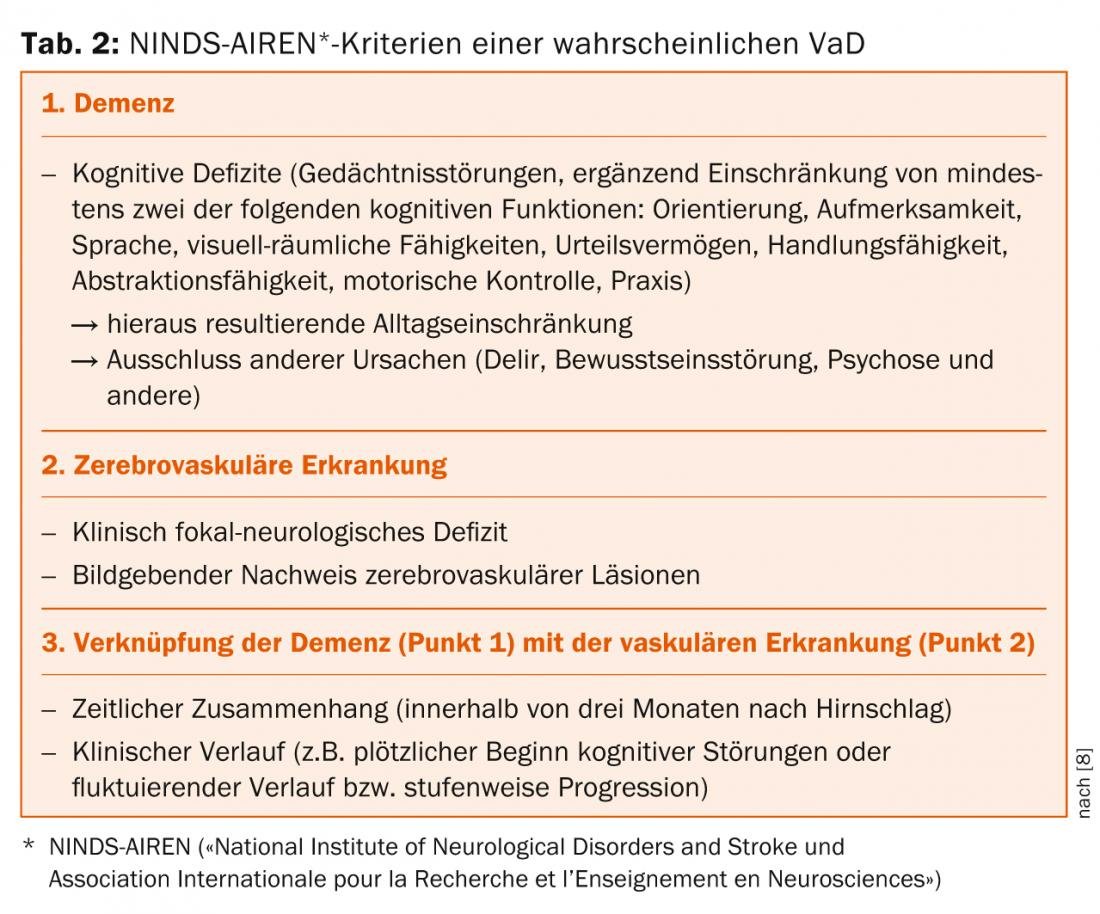
Os chamados critérios NINDS-AIREN [8], que se baseiam na presença de demência e doença cerebrovascular (Tab. 2 ), são ainda hoje utilizados como o sistema válido para o diagnóstico de VaD. Além disso, são utilizados critérios normalizados para a classificação e diagnóstico de perturbações cognitivas vasculares [9].
Microangiopatia cerebral
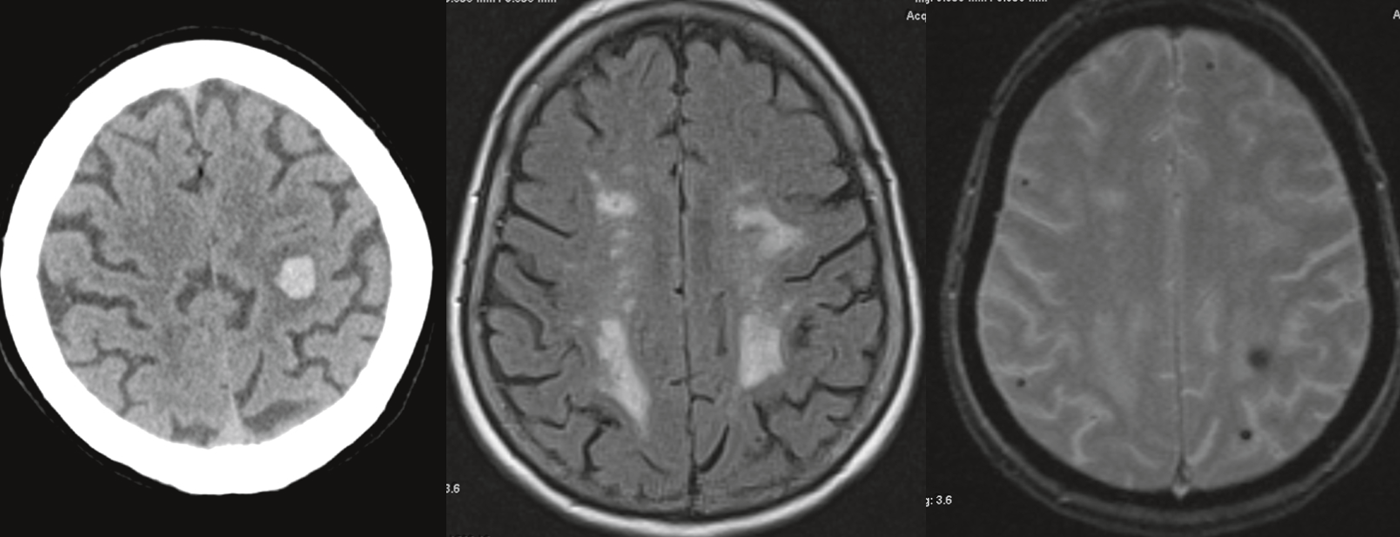
A causa mais comum de VaD é a microangiopatia cerebral, que está particularmente associada à hipertensão arterial. Para além desta forma esporádica, existem também formas hereditárias mais raras de microangiopatia, nas quais existe geralmente um historial familiar positivo de derrames cerebrais ou distúrbios cognitivos – possivelmente sem factores de risco vascular existentes. Cerca de um terço de todos os derrames isquémicos são causados por microangiopatia cerebral. Estas levam a lesões cerebrais isquémicas típicas que podem ser visualizadas por ressonância magnética: Ocorrem enfartes subcorticais lacunares. (Fig. 1a) bem como as alterações leucencefalopáticas vasculares na área do canal medular. (Fig.1b). Além disso, podem por vezes ser encontradas microhemorragia, que na microangiopatia são frequentemente localizadas na área das estruturas mais profundas (por exemplo, os gânglios basais).
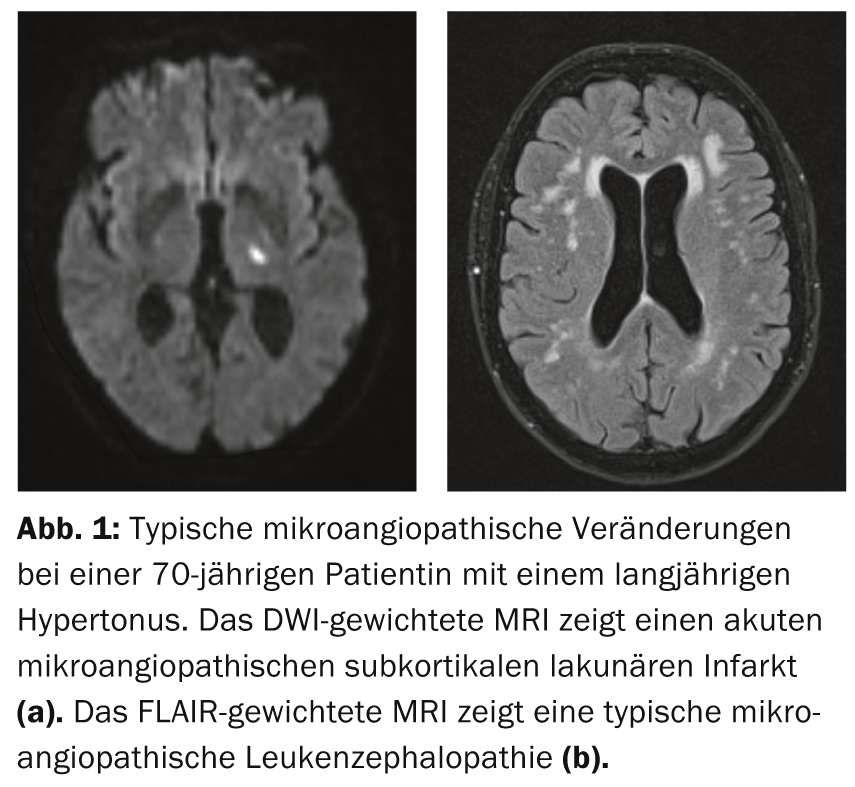
Para além dos sinais e sintomas clínicos físicos (défices neurológicos focais, perturbações de micturição, perturbações da marcha), as perturbações cognitivas estão clinicamente em primeiro plano nas microangiopatias. Estes ocorrem frequentemente de forma flutuante e insidiosamente progressiva e não têm de ser associados a um derrame clinicamente tangível. Devido à patologia na área dos pequenos vasos cerebrais arteriais que penetram subcorticamente, a chamada demência vascular isquémica subcortical (SIVD) ocorre no contexto da isquemia medular. Esta é considerada a forma mais comum de VaD e é, portanto, de particular importância na prática clínica. Em comparação com a AD, caracteriza-se muito menos pela perda de memória, mas principalmente por perturbações nas funções executivas e velocidade de processamento [10]. Na sua forma pura, é assim muitas vezes clinicamente distinta da AD. Em última análise, a microangiopatia também conduz à atrofia cerebral, que está associada à progressão dos défices cognitivos [11]. Em particular, a hipertensão arterial é um factor de risco para a atrofia cerebral devido à microangiopatia. Este facto reforça a relevância clínica de ajustar a tensão arterial e os factores de risco vascular em geral.
Diagnósticos e diagnósticos diferenciais
A classificação diagnóstica da microangiopatia cerebral e da VaD associada baseia-se em parâmetros anamnésticos, clínicos e de imagem. Uma visão geral pode ser encontrada no quadro 3.

Uma avaliação inicial das deficiências cognitivas já é muitas vezes possível durante a entrevista de história clínica. Uma história externa de parentes é de grande importância aqui, entre outras coisas no que diz respeito a possíveis restrições diárias. Em particular, as deficiências cognitivas devem ser inquiridas, o que indica perturbações da atenção, capacidade de concentração e perturbações das funções executivas. Os procedimentos de teste curto cognitivo estão disponíveis como diagnósticos básicos para a avaliação inicial de orientação e quantificação de deficiências cognitivas. Estes podem ser bem utilizados na rotina clínica e podem também servir como parâmetros de acompanhamento, se necessário. Aqui, por exemplo, o Mini-Mental-Test, o DemTect, TFDD (teste para detecção precoce de demência com delimitação de depressão) ou a versão em língua alemã do MoCA (“Montreal Cognitive Assessment”) devem ser mencionados, embora estes procedimentos de teste não se destinem especificamente ao VaD. Alternativamente, para as perturbações cognitivas vasculares, são propostos dois testes mais curtos (5 e 30 minutos) para uso clínico de rotina [9], que são mais capazes de captar os défices característicos na microangiopatia acima mencionados. O chamado teste de triagem também é útil para este fim.
O exame neurológico clínico mostra frequentemente reflexos primitivos desinibidos (reflexo palmomental, reflexo de preensão, etc.) e reflexos posturais debilitados. Para além dos défices neurológicos focais relacionados com isquemia, as perturbações motoras extrapiramidais podem também tornar-se aparentes em fases avançadas da doença.
O diagnóstico por imagem por RM (tab. 3) visa por um lado detectar lesões vasculares frescas (DWI) ou mais antigas (T2/FLAIR) (fig. 1).
Em particular, as lesões medulares isquémicas típicas que podem ser detectadas na avaliação T2/FLAIR devem ser mencionadas aqui, as quais podem ocorrer nas mais variadas formas até uma leucoencefalopatia confluente. Tais mudanças são um achado comum com a idade. Além disso, há a questão dos defeitos de substâncias lacunares (T1) e hemorragias ou microhaemorragias (T2*/SWI).
Além disso, a imagiologia é utilizada para excluir outras patologias cerebrais que podem levar a uma síndrome demencial (por exemplo, NPH, lesões inflamatórias, tumores, atrofia regional ou global no decurso de uma doença neurodegenerativa).
Um importante diagnóstico diferencial de microangiopatia cerebral – especialmente em pessoas idosas – é a angiopatia amilóide cerebral (CAA) (Fig. 2), que também pode levar à VaD. Uma delimitação diagnóstica diferencial é particularmente importante porque a AAC está associada, em particular, a hemorragias cerebrais e tem, portanto, consequências terapêuticas directas, por exemplo, no que respeita à utilização de inibidores de agregação plaquetária num doente com uma leucoencefalopatia vascular.
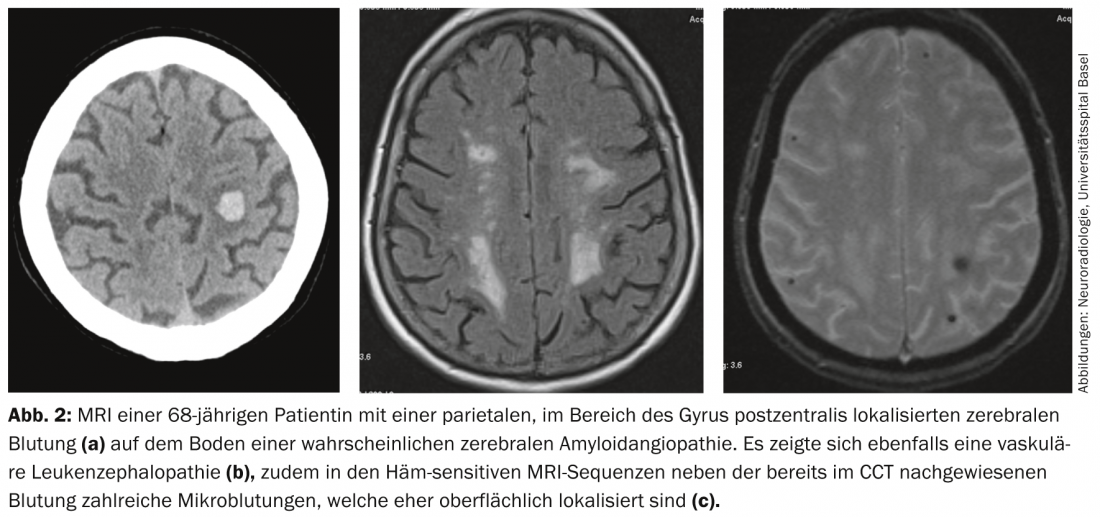
Por vezes o diagnóstico diferencial de lesões medulares isquémicas isquémicas microangiopáticas de outras causas não vasculares de leucoencefalopatia pode ser um desafio.
Os diagnósticos diferenciais importantes estão listados no quadro 4. As doenças inflamatórias e metabólicas são particularmente dignas de menção aqui. Se necessário, outros testes, em particular líquido cefalorraquidiano (LCR), química de laboratório e testes serológicos, devem ser considerados para o diagnóstico diferencial de uma génese microangiopática-vascular de uma leucoencefalopatia.

Terapia
Doenças vasculares subjacentes: O tratamento em VaD destina-se particularmente ao controlo precoce de doenças vasculares e factores de risco existentes, e em microangiopatia particularmente no controlo da pressão sanguínea. O que é importante aqui é o controlo da pressão sanguínea per se, e não a utilização de grupos específicos de substâncias, em que os anti-hipertensivos que actuam no sistema renina-angiotensina podem ter um papel especial a desempenhar neste contexto. Uma vez que a ocorrência de um AVC clinicamente manifesto é per se um factor de risco para a VaD, o controlo do factor de risco no sentido da profilaxia primária das doenças cerebrovasculares é importante. O mesmo se aplica à prevenção secundária do AVC, uma vez que o AVC recorrente provoca um aumento significativo do risco de AVC [12]. A profilaxia secundária com medicação de acordo com as recomendações das directrizes actuais desempenha assim também um papel importante em relação às perturbações cognitivas vasculares.
Para a utilização profiláctica primária de, por exemplo, inibidores de agregação plaquetária para a terapia/profilaxia da demência, não há dados claros disponíveis hoje em dia, pelo que não é actualmente recomendado. Isto também se aplica à utilização de estatinas. Deve ser dado aconselhamento sobre factores modificáveis do estilo de vida, especialmente o consumo de álcool e nicotina e a actividade física. A terapia dos factores e doenças vasculares desempenha assim um papel global importante na prevenção e tratamento da demência, até porque as abordagens terapêuticas à AD como doença neurodegenerativa são limitadas até à data.
Terapia sintomática: Se houver evidência de demência mista, a terapia sintomática como na AD é actualmente recomendada, desde que não haja contra-indicações vasculares, por exemplo, ao uso de inibidores de colinesterase. No caso de sintomas concomitantes neuropsiquiátricos, o uso de neurolépticos atípicos, em particular, deve ser revisto criticamente, tendo como pano de fundo um risco potencialmente aumentado de complicações cerebrovasculares. Os neurolépticos convencionais também devem ser evitados devido a potenciais efeitos secundários anticolinérgicos e motores extrapiramidais. Os sintomas de depressão não devem ser tratados com antidepressivos anticolinérgicos (tais como tricíclicos); os inibidores selectivos de recaptação de serotonina (SSRIs) são uma opção aqui.
Resumo
O termo VaD não descreve uma doença singular, mas sim uma síndrome demencial geral baseada em doenças cerebrovasculares. A microangiopatia cerebral é a causa mais comum de VaD. Está frequentemente associada à hipertensão arterial e conduz, em particular, a uma deficiência cognitiva subcortical. Assim, o perfil das perturbações cognitivas difere da DA, mas sobreposições e híbridos não são invulgares.
A imagiologia cerebral desempenha um papel de diagnóstico crucial juntamente com a avaliação clínica neurológica. O diagnóstico precoce das causas vasculares da deficiência cognitiva deve levar ao início de medidas terapêuticas ou preventivas. A microangiopatia cerebral pode ter um impacto negativo significativo no curso da doença de Alzheimer existente. Isto sublinha a importância do diagnóstico e da terapia precoces.
Os AVC isquémicos são um importante factor de risco para a ocorrência de distúrbios cognitivos vasculares. O controlo optimizado do factor de risco primário preventivo, bem como a profilaxia secundária, são portanto de grande importância terapêutica também no que diz respeito à VaD.
PD Nils Peters, MD
Literatura:
- Estratégia Nacional de Demência 2014-2017, Gabinete Federal de Saúde Pública (FOPH) e Conferência Suíça de Ministros Cantonais da Saúde (GDK). Berna, Novembro de 2013.
- Roman GC, Kalaria RN: Envelhecimento do Neurobiol 2006; 27: 1769-1785.
- Stevens T, et al: Br J Psychiatry 2002; 180: 270-276.
- Heyman A, et al: Neurology 1998; 51: 159-162.
- O’Brien JT, et al: Dificuldades cognitivas vasculares. Lancet Neurol 2003; 2: 89-98.
- GC Romano: Neuroepidemiologia 2003; 22: 161-164.
- Snowdon DA, et al: JAMA 1997; 277: 813-817.
- Roman GC, et al: Neurology 1993; 43: 250-260.
- Hachinski V, et al: Stroke 2006; 37: 2220-2241.
- Peters N, et al: Am J Psychiatry 2005; 162: 2078-2085.
- Peters N, et al: Neurology 2006; 66: 1517-1522.
- Pendlebury ST, Rothwell PM: Lancet Neurol 2009; 8: 1006-1018.
InFo NEUROLOGIA & PSYCHIATRY 2014; 12(3): 18-21