O carcinoma do endométrio é o sexto cancro mais frequente nas mulheres em todo o mundo e tem um mau prognóstico, sobretudo em termos de resultados a longo prazo. O tempo médio de sobrevivência global é inferior a três anos. A gestão eficaz da terapia é particularmente indicada para pacientes com cancro do endométrio primário avançado ou recorrente. Agora, os resultados do estudo estão a alimentar a esperança de um novo tratamento combinado.
O carcinoma do endométrio (CE) é um tumor maligno do útero com origem na camada mucosa interna do útero. A doença afecta predominantemente as mulheres pós-menopáusicas, com um pico de idade entre os 65 e os 85 anos. A menarca precoce, a menopausa tardia, a baixa paridade ou a síndrome dos ovários poliquísticos são descritos como factores de risco endógenos. Os factores de risco exógenos incluem a terapia de substituição de estrogénios não cíclica isolada, a terapia com tamoxifeno e a radioterapia prévia. A CE envolve normalmente adenocarcinomas do revestimento uterino. Os adenocarcinomas serosos e de células claras ou os carcinomas de células escamosas ocorrem apenas raramente. É feita uma distinção entre o carcinoma de tipo I dependente de estrogénios e o carcinoma de tipo II independente de estrogénios. No entanto, os marcadores imuno-histoquímicos e moleculares estão também a desempenhar um papel cada vez mais importante.
A tipagem molecular permite uma terapia mais precisa
A subtipagem molecular permite uma estratificação individualizada do risco e uma escolha mais precisa da terapêutica. Como parte do projeto The Cancer Genome Atlas (TCGA), foram identificados quatro subtipos moleculares de CE utilizando a sequenciação de nova geração (NGS):
- POLE: mutação do gene da polimerase epsilon (POLE), função de revisão prejudicada durante a replicação do ADN, fenótipo ultramutado
- MSI-H/dMMR: reparação deficiente da incompatibilidade (dMMR) devido a mutações, elevada instabilidade de microssatélites (MSI-H), fenótipo hipermutado
- Número de cópias elevado/TP53abn: elevado número de alterações somáticas do número de cópias, principalmente mutações TP53 (TP53 anormal)
- Número de cópias baixo/NSMP: várias mutações, sem perfil molecular específico (NSMP)
Partindo desta base, foram desenvolvidas nos últimos anos substâncias específicas (por exemplo, Dostarlimab, Lenvatinib). Os tumores MSI-H representam 25–30% dos carcinomas do endométrio. A expressão aumentada do recetor 1 de morte celular programada (PD-1) e dos seus ligandos (PD-L1 e PD-L2) e a elevada carga de mutações tumorais associadas aos tumores dMMR-MSI-H tornam-nos potencialmente susceptíveis às terapêuticas anti-PD-1 e anti-PD-L1.
CE primária avançada ou recorrente
A carboplatina mais paclitaxel é a quimioterapia padrão para o tratamento de primeira linha da CE primária avançada ou recorrente. No entanto, os resultados a longo prazo ainda não são satisfatórios. Antes da aprovação dos agentes-alvo, não existiam estratégias de tratamento eficazes para os doentes que tinham falhado a quimioterapia à base de platina. Dostarlimab é um inibidor ativo do ponto de controlo imunitário que tem como alvo o recetor PD-1. Com base nos resultados do estudo GARNET, o medicamento foi aprovado para o cancro do endométrio avançado ou recorrente dMMR-MSI-H. Os investigadores foram agora mais longe: a quimioterapia citotóxica pode ter efeitos imunomoduladores, como a interrupção das vias de sinalização imunossupressoras e o aumento da resposta das células T citotóxicas. Por conseguinte, era razoável supor que a combinação de quimioterapia e imunoterapia poderia ter um efeito sinérgico no microambiente tumoral. Por conseguinte, o estudo ENGOT-EN-6-NSGO/GOG-3031/RUBY investigou a eficácia e a segurança do dostarlimab em combinação com carboplatina e paclitaxel em comparação com placebo mais carboplatina e paclitaxel em doentes com CE primária avançada ou recorrente.
No estudo de Fase III, multicêntrico e em dupla ocultação, 494 doentes (118 dos quais tinham dMMR-MSI-H-EC) foram aleatorizados numa escala de 1:1 e receberam 500 mg de dostarlimab ou placebo por via intravenosa em combinação com carboplatina e paclitaxel de três em três semanas durante os primeiros seis ciclos, seguidos de 1000 mg de dostarlimab ou placebo por via intravenosa de seis em seis semanas até três anos ou até à progressão da doença, interrupção do tratamento devido a efeitos tóxicos, desistência do doente, decisão do investigador de retirar o doente ou morte. Os objectivos primários foram a sobrevivência livre de progressão em doentes com dMMR-MSI-H-EC primário avançado ou recorrente e na população em geral, bem como a sobrevivência global na população em geral. Os parâmetros secundários incluíram a sobrevivência livre de progressão determinada por uma revisão central independente e cega, a resposta objetiva, o controlo da doença, a duração da resposta, o tempo até à segunda progressão da doença, os resultados comunicados pelos doentes e as análises farmacocinéticas e de imunogenicidade.
Sobrevivência prolongada sem progressão
A taxa de sobrevivência global após 24 meses foi de 71,3% com o dostarlimab e de 56,0% com o placebo. Na população dMMR-MSI-H, a sobrevivência sem progressão estimada foi de 61,4% no grupo do soro e de 15,7% no grupo do placebo. Na população total, foi de 36,1% contra 18,1%. Os acontecimentos adversos mais comuns foram náuseas (53,9% versus 45,9%), alopécia (53,5% e 50,0%) e fadiga (51,9% e 54,5%). Foi assim demonstrado que os doentes com CE primária avançada ou recorrente beneficiam significativamente da combinação de dostarlimab, carboplatina e paclitaxel em termos de um menor risco de progressão da doença.
Leitura adicional:
- Mirza MR, Chase DM, Slomovitz BM, et al.: Dostarlimab for Primary Advanced or Recurrent Endometrial Cancer. N Engl J Med 2023; 388: 2145–2158.
- www.leitlinienprogramm-onkologie.de/fileadmin/user_upload/LL_Endometriumkarzinom_Langversion_3.01_.pdf (último acesso em 05.01.2024)
- www.gelbe-liste.de/krankheiten/endometriumkarzinom (último acesso em 05.01.2024)
- www.krebsgesellschaft.de/onko-internetportal/basis-informationen-krebs/krebsarten/andere-krebsarten/gebaermutterkoerperkrebs.html (último acesso em 05/01/2024).
HAUSARZT PRAXIS 2024; 19(1): 41
InFo ONKOLOGIE & HÄMATOLOGIE 2024; 12(1): 26
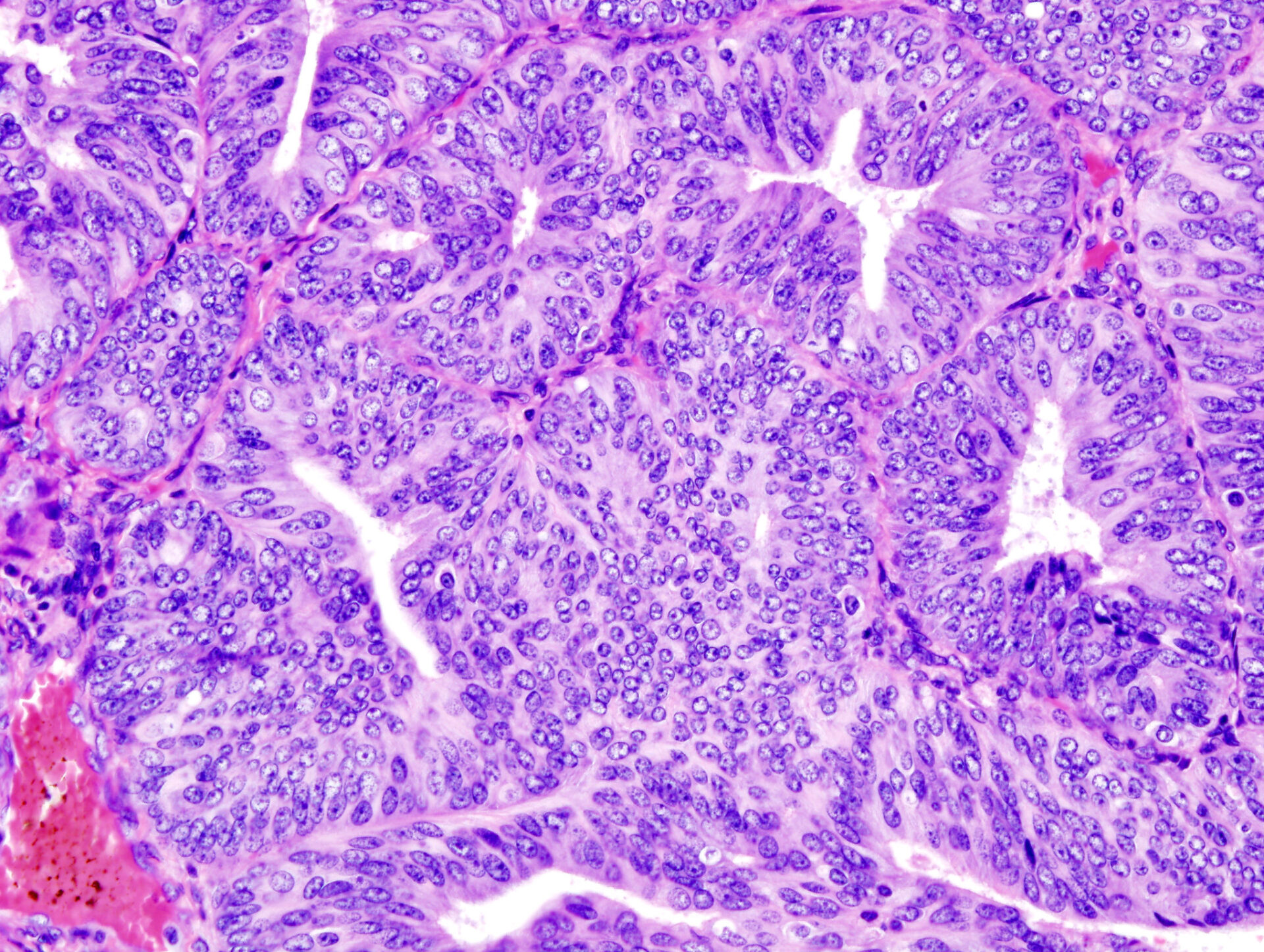
Imagem da capa: Representação histopatológica de adenocarcinoma endometrióide demonstrada em biopsia endometrial. Coloração de hematoxilina-eosina.
© KGH, wikimedia