O anticorpo monoclonal dupilumab bloqueia o componente recetor comum da interleucina (IL)-4 e da IL-13, os principais factores de inflamação do tipo 2. Está autorizado na Suíça desde 2019, e novos estudos analisaram a sua eficácia e segurança em doentes com DPOC moderada a grave com inflamação T2 e em crianças com asma moderada a grave não controlada. Os resultados foram apresentados no Congresso DGP 2024.
As exacerbações da DPOC estão associadas a um risco acrescido de novas exacerbações, a uma deterioração da função pulmonar e a uma elevada morbilidade e mortalidade. As doenças de DPOC com inflamação de tipo 2 são particularmente afectadas.
O BOREAS foi um estudo de fase 3, de 52 semanas, aleatorizado, em dupla ocultação, sobre a eficácia e a segurança do dupilumab 300 mg bissemanal em doentes com DPOC com eosinófilos no sangue ≥300 células/µl. Idealmente, já deveriam ter recebido uma terapêutica tripla composta por um corticosteroide inalado (ICS), um β2-agonista de longa ação (LABA) e um antagonista muscarínico de longa ação (LAMA). Isto aplica-se a 98% da população, como explicou o Dr. Henrik Watz, do Instituto de Investigação Pneumológica da Clínica Pulmonar de Grosshansdorf (Alemanha) [1]. Em casos excepcionais, como quando a ICS estava contra-indicada, a combinação LAMA/LABA também foi permitida. As exacerbações já deveriam ter ocorrido durante o tratamento como um indicador da necessidade de terapia adicional. O historial de asma foi um critério de exclusão.
939 doentes com eosinófilos no sangue ≥300 células/µl foram incluídos no BOREAS e aleatorizados 1:1 para dupilumab 300 mg (n=468) ou placebo (n=471) por via subcutânea (SC) uma vez de 2 em 2 semanas (q2w) durante 52 semanas. Os doentes tinham entre 40 e ≤80 anos de idade. O endpoint primário foi a taxa anualizada de exacerbações moderadas a graves desde o início do estudo até à semana 52. Os endpoints secundários incluíram a alteração no FEV1antes da broncodilatação na semana 12 e na semana 52 em comparação com a linha de base (BL), exacerbações cumulativas ao longo do tempo e a segurança ou qualidade de vida relacionada com a saúde dos doentes sob terapêutica como Resultados comunicados pelos doentes (PRO).
Taxa de exacerbação da DPOC reduzida em 30%
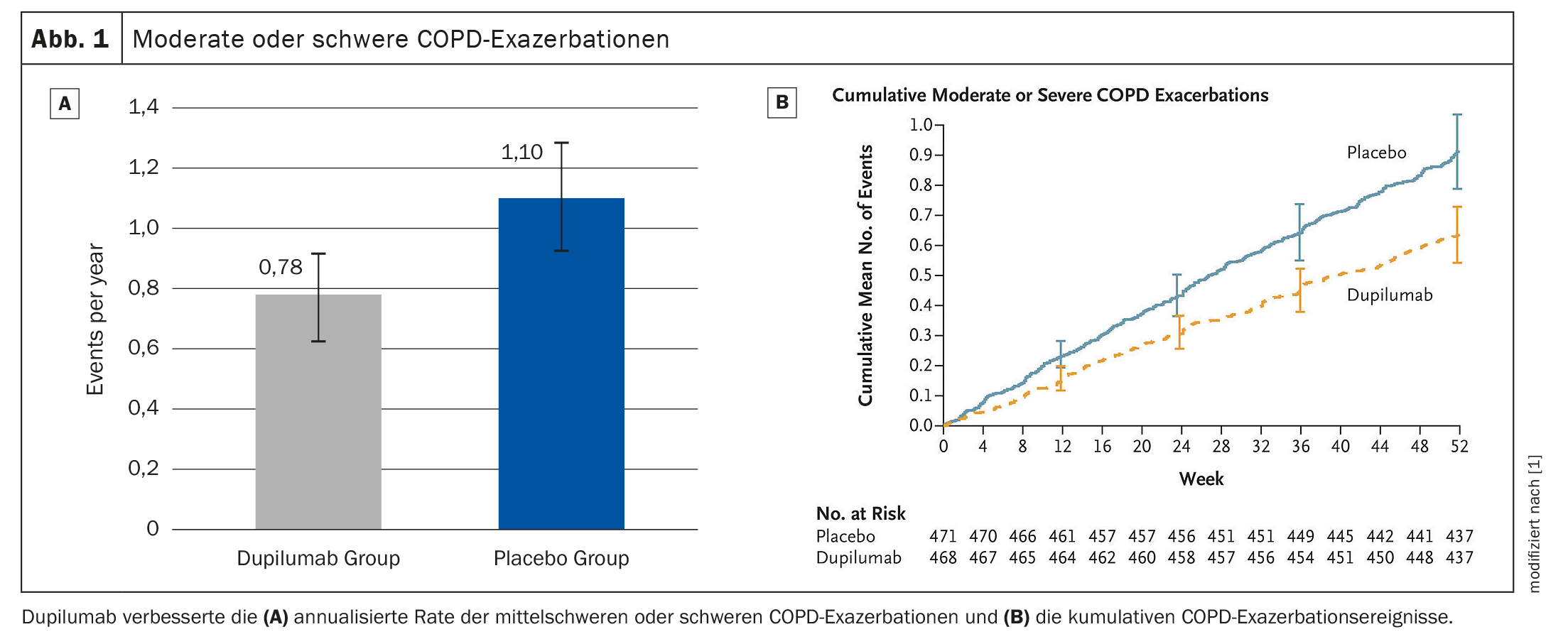
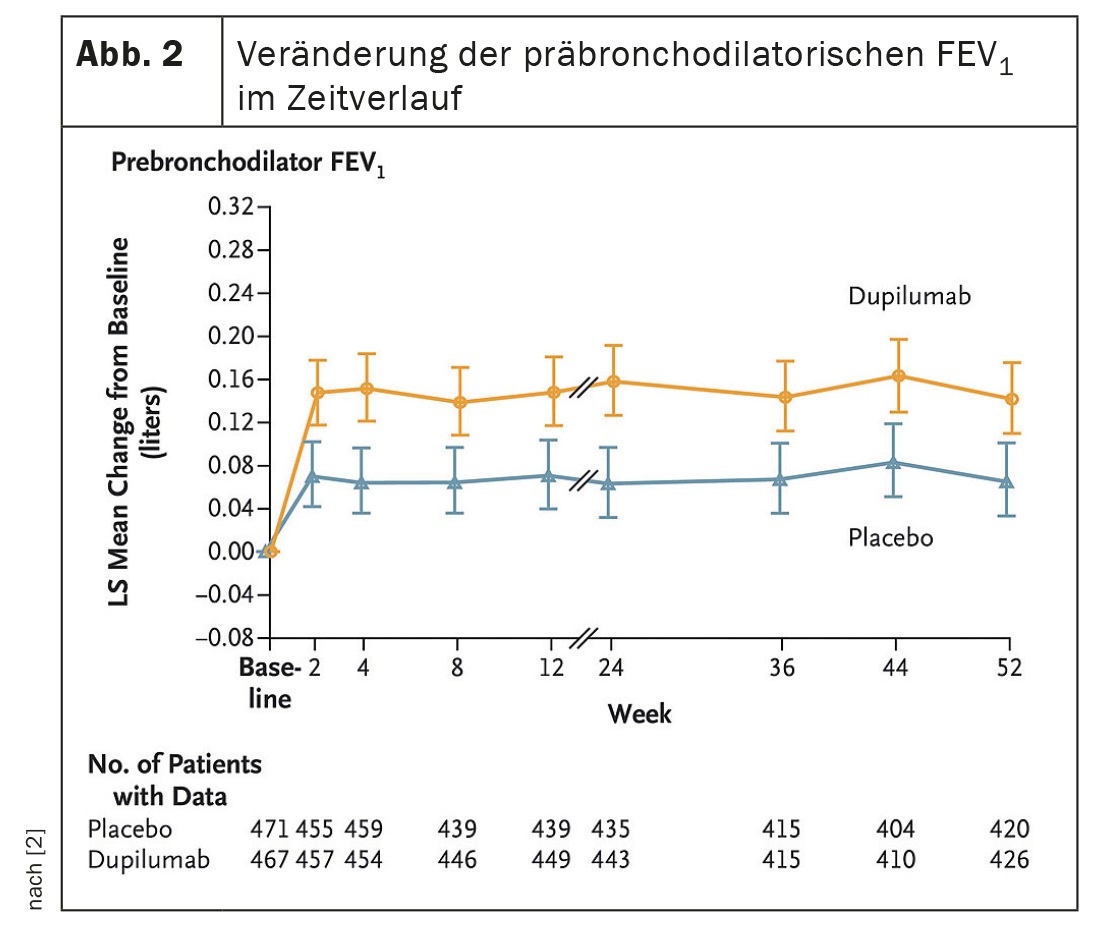
Após 52 semanas, o dupilumab reduziu a taxa de exacerbação em 30% em comparação com o grupo placebo (p=0,0005) (Fig. 1A, 1B). O anticorpo IgG4 aumentou o FEV pré-DB1 na semana 12 foi significativo (diferença LSM vs. placebo: 83 ml, p<0,0001); que persistiu até à semana 52 (83 ml, p=0,0003) (Fig. 2) . Isto tendeu a resultar num menor número anual de exacerbações associadas ao tratamento com corticosteróides sistémicos (SCS) no grupo do dupilumab- (13,57 dias [SD 13,17] em comparação com o braço placebo (19,09 dias [SD 20,65]). A segurança foi semelhante em ambos os grupos, os eventos adversos foram iguais.
Assim, o dupilumab melhorou significativamente as exacerbações moderadas a graves, a função pulmonar, a qualidade de vida e os sintomas em doentes com DPOC com inflamação T2, concluiu o Dr. Watz. A utilização de dias de SCS necessários para o tratamento de AECOPD tendeu a diminuir com o dupilumab.
Efeito a longo prazo na função pulmonar em doentes com asma pediátrica
Minimizar o comprometimento da função pulmonar é um objetivo primário no tratamento da asma pediátrica. A utilização a longo prazo de dupilumab no estudo Excursion resultou numa melhoria sustentada da função pulmonar em doentes de 6-11 anos de idade com asma tipo 2 moderada a grave não controlada que completaram o estudo Voyage; foi observada uma melhoria rápida da função pulmonar nos doentes que passaram do placebo (PBO) para o dupilumab (DPL).
No Voyage, o dupilumab reduziu significativamente as exacerbações graves e melhorou a função pulmonar ao longo de 52 semanas. O Excursion foi um estudo de extensão aberto, de braço único, com crianças que tinham participado anteriormente no Voyage. A Dr.ª Theresa Guilbert, pneumologista pediátrica do Hospital Pediátrico de Cincinnati e da Universidade de Cincinnati (EUA), apresentou uma análise post-hoc do Excursion que avaliou as melhorias numericamente mais elevadas da função pulmonar observadas nos braços DPL/DPL em comparação com os braços PBO/DPL no Excursion [3].
As crianças receberam dupilumab 100 mg ou 200 mg de 2 em 2 semanas, de acordo com o peso corporal, durante um período de um ano. Os investigadores analisaram a alteração da linha de base no estudo principal (PSBL) e a percentagem de FEV1 antes da broncodilatação ao longo de 104 semanas, bem como o impacto das características da linha de base, como a idade de início da asma, o tempo decorrido desde o diagnóstico, a dose de corticosteroide inalado (ISC) na linha de base e o controlo da asma na eficácia do dupilumab.
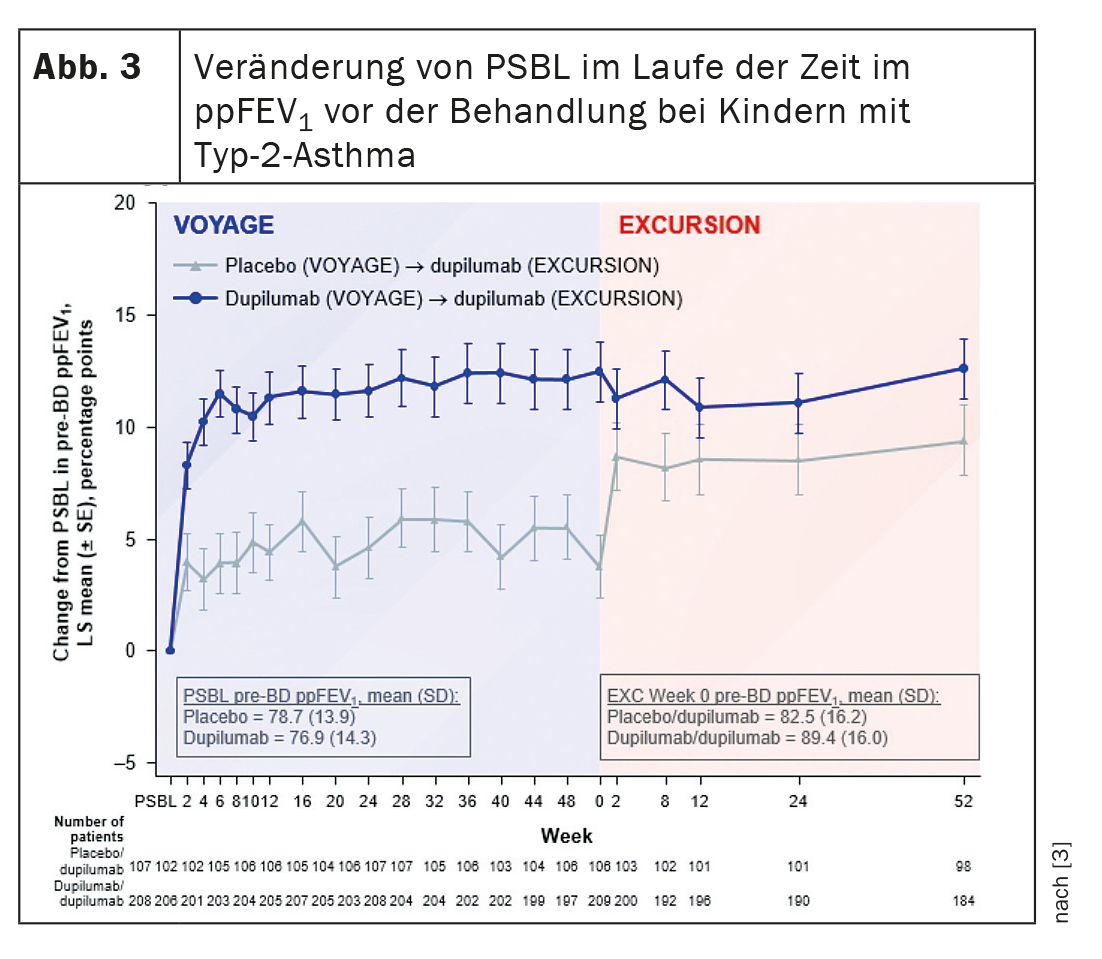
Dupilumab melhorou rapidamente a função pulmonar durante a Viagem, o que continuou durante a Excursão. No Excursion, os doentes que receberam placebo durante o Voyage apresentaram uma melhoria rápida e sustentada da função pulmonar desde o início do tratamento com dupilumab (Fig. 3) . O dupilumab foi capaz de melhorar e manter a percentagem de FEV1 prevista antes da broncodilatação durante 104 semanas, resumiu o Dr. Guilbert os resultados. A resposta da função pulmonar ao medicamento biológico durante um período de 1 a 2 anos não diferiu em função da duração da asma ou da idade no início da terapêutica.
A discussão com estes dados é que os doentes que mudaram do placebo para o dupilumab não recuperaram totalmente a sua função pulmonar, observou o Prof. Dr. Marek Lommatzsch, University Medicine Rostock (Alemanha). A questão que se coloca é: será que este efeito é real e significa que um atraso de um ano na terapia significa uma perda de função pulmonar? A Dra. Guilbert explicou que o seu grupo de investigação teve inicialmente a mesma ideia. “No entanto, não se trata de uma diferença estatística. O valor é numericamente mais elevado, mas não atinge significância estatística em comparação com o grupo placebo.” Provavelmente, são necessários números maiores para determinar esta diferença. Além disso, “há, naturalmente, muita discussão sobre se devemos falar de remissão clínica no tratamento com o advento das terapias biológicas”. Existe algum debate sobre se este procedimento é ou não adequado em pediatria.
Congresso: DGP 2024
Fontes:
- Watz H: Eficácia e Segurança do Dupilumab para a DPOC com Inflamação Tipo 2 Indicada por Eosinófilos Elevados. Sessão “Atualidade dos ensaios clínicos em asma e DPOC”. 64º Congresso da Sociedade Alemã de Pneumologia e Medicina Respiratória e.V., 20-24 de março de 2024, Mannheim (D).
- Bhatt SP, Rabe KF, Hanania NA, et al: Dupilumab para DPOC com Inflamação Tipo 2 Indicada por Contagens de Eosinófilos. N Engl J Med 2023; 389: 205-214; doi: 10.1056/NEJMoa2303951.
- Guilbert T: Efeito do Dupilumab a longo prazo na função pulmonar em doentes pediátricos com asma não controlada. Sessão “Atualidade dos ensaios clínicos em asma e DPOC”. 64º Congresso da Sociedade Alemã de Pneumologia e Medicina Respiratória e.V., 20-24 de março de 2024, Mannheim (D).
InFo PNEUMOLOGIE & ALLERGOLOGIE 2024; 6(2): 36-37 (publicado em 30.5.24, antes da impressão)