O tromboembolismo venoso (VTE) é a terceira doença cardiovascular mais comum na Europa Central. Manifestam-se como trombose venosa profunda em cerca de dois terços dos casos e com os sintomas de embolia pulmonar em cerca de um terço dos casos. Durante a idade reprodutiva, as mulheres experimentam mais frequentemente eventos de VTE do que os homens da mesma idade.
O tromboembolismo venoso (VTE) é a terceira doença cardiovascular mais comum na Europa Central. Manifestam-se como trombose venosa profunda em cerca de dois terços dos casos e com os sintomas de embolia pulmonar em cerca de um terço dos casos. Durante a idade reprodutiva, as mulheres experimentam mais frequentemente eventos de VTE do que os homens da mesma idade. Isto é principalmente atribuído a factores de risco específicos das mulheres, tais como a utilização de contraceptivos hormonais e gravidezes. Apesar deste aumento relativo do risco, o risco global de VTE permanece baixo, em cerca de 2-5 por 10 000 mulheres por ano [1].
Hormonas e hemostasia
Os estrogénios influenciam a expressão genética hepática e alteram o equilíbrio entre factores coagulatórios e anticoagulatórios no sentido de uma maior coagulabilidade. O nível da dose de estrogénio e o tipo de progestagénio em preparações combinadas determinam o risco de complicações trombóticas. O aumento das actividades dos factores trombogénicos (fibrinogénio, protrombina, factor VII, factor VIII, factor X) e a redução das actividades dos inibidores da coagulação fisiológica (antitrombina, proteína S, inibidor da via do factor tecidual [TFPI]) podem ser detectados quando são tomadas preparações hormonais [2,3]. Isto resulta em resistência à proteína C activada (a chamada resistência APC adquirida). A extensão desta resistência APC está correlacionada com o risco de VTE [4].
Contraceptivos hormonais combinados
Os contraceptivos hormonais combinados (CHCs) representam a maior proporção dos métodos contraceptivos utilizados. Já alguns anos após a sua introdução no mercado em 1960, tornou-se conhecido que as CHDs aumentam o risco de trombose venosa e, em menor grau, de trombose arterial [5]. A composição da CHD mudou ao longo dos últimos 60 anos, mas os componentes básicos não sofreram alterações. As CHDs modernas contêm uma combinação de um estrogénio (geralmente etinilestradiol numa dosagem de 20 -35 µg) e um progestogénio produzido sinteticamente. A composição determina a extensão do aumento do risco para eventos tromboembólicos (tab. 1) . Entre as CHDs, as preparações que contêm uma dose baixa de estrogénio e levonorgestrel como progestogénio têm o menor risco de VTE [6,7]. Com outros componentes progestogénicos, o risco de VTE é por vezes significativamente mais elevado. Foi descrito um risco acrescido de trombose não só para os CHD aplicáveis oralmente, mas também para as preparações combinadas aplicadas transdermalmente e transvaginalmente [8].

O risco de tromboembolismo é mais elevado nos primeiros meses de utilização e diminui significativamente durante o primeiro ano. Contudo, mesmo com uma utilização a longo prazo, as mulheres que utilizam um CHD permanecem com um risco de TEV cerca de 2 vezes maior em comparação com as mulheres que não utilizam contracepção hormonal [9]. Se a contracepção hormonal for interrompida durante várias semanas, existe um risco temporariamente mais elevado de TEV com o recomeço do que com o uso contínuo. Não parece, portanto, razoável fazer uma pausa perioperativa para reduzir o risco de TEV. Se o risco de TEV for elevado, deve ser dada profilaxia de TEV com uma heparina de baixo peso molecular ou outra substância aprovada para a indicação [1].
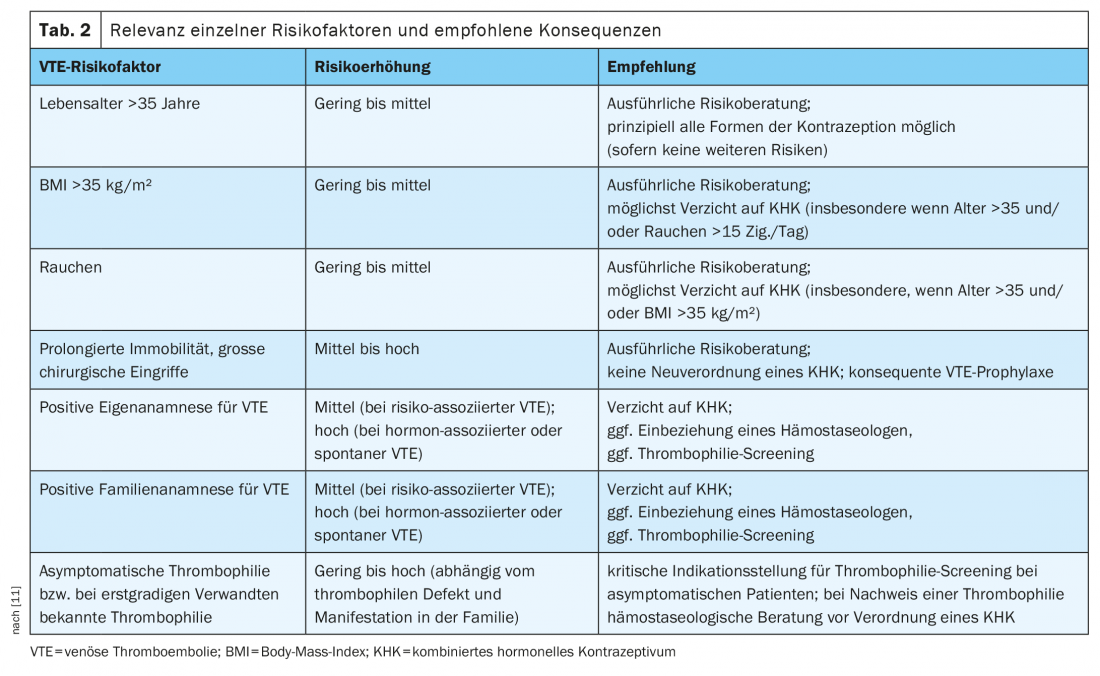
Na presença de factores de risco adicionais (por exemplo, trombofilia hereditária, historial familiar positivo, idade avançada, obesidade, tabagismo), o risco de VTE aumenta ainda mais [10]. O risco individual de TEV deve ser avaliado cada vez que uma CHD é prescrita, tomando cuidadosamente um historial médico. A directiva AWMF S3 recentemente actualizada sobre contracepção hormonal recomenda que factores como a idade, índice de massa corporal, estado de tabagismo, deficiência de mobilidade, a próxima grande cirurgia, informação sobre a história pessoal e familiar para eventos VTE e qualquer trombofilia conhecida sejam incluídos na avaliação de risco [11]. O Quadro 2 dá uma visão geral dos factores de risco e das consequências recomendadas.
Trombofilia hereditária e contracepção hormonal
Se uma história familiar positiva por si só constitui uma contra-indicação à contracepção hormonal é discutida de forma controversa. Alguns estudos demonstraram que a trombofilia hereditária juntamente com a utilização de uma CHD aumenta significativamente o risco relativo de VTE [12,13]. Existe hoje em dia acordo que o rastreio geral da trombofilia antes da primeira prescrição de um CHD não é útil. Pelo menos uma trombofilia hereditária pode ser detectada em 3-9% da população da Europa Central (Tab. 3) . As mais comuns são a heterozigosidade para uma mutação do factor V Leiden (aprox. 2-7%) ou uma mutação do protrombina G20210A (aprox. 1-2%). Apesar da elevada prevalência destas mutações, o risco absoluto de VTE nas pessoas afectadas é baixo, a menos que sejam acrescentados outros factores de risco.

Um jornal francês recente, incluindo 2214 familiares de 651 famílias com trombofilia hereditária conhecida e manifestações de TEV, calculou um risco absoluto anual de TEV de 0,36% (HR 1,91; 95% CI 1,30-2,80) para indivíduos com trombofilia leve mas sem eventos VTE anteriores próprios, e 0,64% (HR 3,78; 95% CI 2,50-5,73) para indivíduos com trombofilia grave. [14]. No entanto, o risco de VTE aumenta significativamente quando se toma uma CHD.
Outro grupo de investigação calculou um risco relativo de VTE até 45 vezes maior para a utilização de CHD em mulheres com uma mutação do factor V Leiden [15]. As mulheres com trombofilia e um historial familiar positivo não devem, portanto, ser prescritas CHD, se possível, especialmente se o paciente índice tiver tido um evento VTE numa idade jovem sem outros factores de risco ou associados a hormonas. Se a prescrição de uma CHD for inevitável devido a circunstâncias concomitantes ou comorbilidades, deve ser considerada uma avaliação hemostaseológica e a prescrição de uma CHD com levonorgestrel como componente progestogénico. A CHD deve ser evitada em casos de trombofilia grave conhecida; nestes casos, deve ser preferido um método contraceptivo sem estrogénios.
Monopreparações de progestogénio
De acordo com os conhecimentos actuais, os contraceptivos com um componente progestogénico sozinho (isto é, preparações orais com desogestrel ou levonorgestrel ou dispositivos intrauterinos contendo levonorgestrel) não aumentam significativamente o risco de VTE. Podem portanto ser utilizados em mulheres em risco acrescido de TEV ou com um historial de TEV [1,16]. Contudo, isto não se aplica ao acetato de medroxiprogesterona de depósito (DMPA; a chamada injecção de 3 meses), para o qual foi descrito um risco de VTE aproximadamente 3 vezes maior [17]. A administração de DMPA deve, portanto, ser evitada nas mulheres com risco acrescido de TEV.
Contracepção sob anticoagulação
Muitas vezes, as mulheres com TEV associado a hormonas deixam de tomar o contraceptivo imediatamente após o diagnóstico ter sido confirmado. Isto é -problemático na medida em que a descontinuação leva a hemorragias abortivas, que podem ser mais graves sob anticoagulantes de dose mais elevada na fase inicial (apixaban, rivaroxaban) ou anticoagulação sobreposta (NMH mais antagonista de vitamina K [VKA]) do que na fase de terapia de manutenção. Além disso, o risco de uma gravidez indesejada aumenta. A actual directriz AWMF S3 apela à contracepção segura para todas as mulheres em terapia anticoagulante oral [11], uma vez que tanto os anticoagulantes orais directos (DOAKs) como os VKAs são compatíveis com a placenta e, portanto, potencialmente embriotóxicos. De acordo com a avaliação actual, o efeito protrombogénico da CHD é compensado por uma anticoagulação totalmente terapêutica, de modo que a contracepção contínua com uma CHD sob protecção anticoagulante é considerada segura.
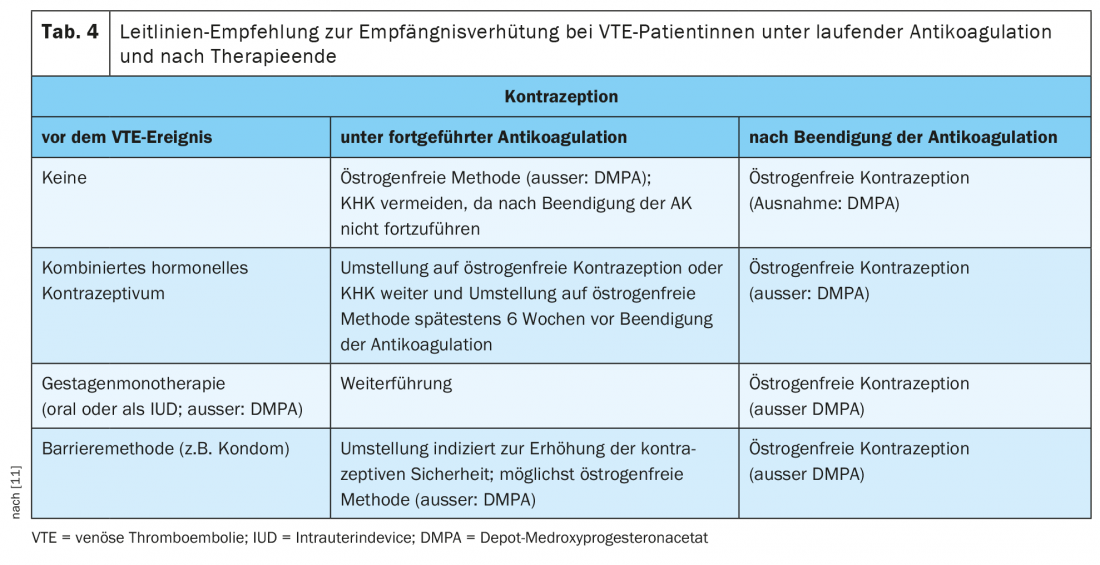
Numa análise pós-hoc subgrupo dos ensaios EINSTEIN-DVT e EINSTEIN-PE comparando o risco de recorrência em mulheres antes dos 60 anos de idade com e sem terapia hormonal continuada, não houve evidência de um aumento da taxa de recorrência de TEV com terapia hormonal continuada (3,7% vs. 4,7%; HR 0,56; 95% CI 0,23-1,39) [18]. Para minimizar o risco de TEV sob anticoagulação, a directriz AWMF S3 recomenda uma monopreparação de progestogénio (oral ou como dispositivo intra-uterino) ou um DIU de cobre como método de primeira escolha (os chamados métodos sem estrogénios). (Tab. 4). Se a paciente, juntamente com o seu médico, decidir continuar a contracepção com um CHD, recomenda-se a mudança para uma preparação com levonorgestrel como componente do progestogénio [11].
VTE associado a hormonas e risco de recidiva
De acordo com as actuais avaliações de risco, as CHDs são consideradas factores de risco fracos e transitórios [19]. Uma vez que o uso continuado de CHD após a descontinuação da anticoagulação é acompanhado de um risco presumivelmente elevado de recorrência, as CHD devem ser descontinuadas ou mudadas para contracepção sem estrogénios pelo menos 6 semanas antes da descontinuação planeada da anticoagulação.
Em princípio, as mulheres têm menor risco de recorrência após um primeiro evento de VTE do que os homens da mesma idade. No prazo de um ano, 5,3% e no prazo de 5 anos 11,1% de todas as mulheres sofrem uma recorrência. O risco de recorrência é menor após TEV associado a hormonas do que após TEV espontâneo (HR 0,5; 95% CI 0,3-0,8) [20]. Os estudos de coorte relatam um risco absoluto anual de 1,1-2,5% [21–23]. Isto é comparável a um risco médio de hemorragia sob anticoagulação totalmente terapêutica de cerca de 1-3% por ano [24]. Alguns estudos referem mesmo um risco mais elevado de hemorragias graves e clinicamente relevantes nas mulheres em comparação com os homens [10].
Em consideração dos benefícios e riscos, a anticoagulação após o VTE associado a CHD e na ausência de factores de risco persistentes é, portanto, normalmente limitada a 3 – 6 meses. Se a contracepção tiver sido continuada com uma CHD, deve ter-se o cuidado de a mudar para um método contraceptivo sem estrogénios pelo menos 6 semanas antes da cessação da anticoagulação planeada.
Técnicas reprodutivas assistidas e risco VTE
A proporção de gravidezes resultantes de técnicas de reprodução assistida (ART) tem aumentado nos últimos anos. A terapia hormonal necessária para tal aumenta o risco de TEV. Por exemplo, as mulheres que engravidaram após a fertilização in vitro (FIV) apresentam um risco cerca de 2 vezes maior do que as mulheres que engravidaram espontaneamente [25,26]. Numa análise populacional sueca de 140 458 registos de 1990 a 2008, o risco absoluto de TEV para mulheres grávidas após tratamento de FIV foi de 0,42% em comparação com 0,25% para mulheres com início espontâneo de gravidez (HR 1,77; 95% CI 1,41-2,23). O risco de TEV manteve-se mais elevado ao longo da gravidez, mas foi mais elevado no 1º trimestre (HR 4,22; 95% CI 2,46 -7,26) [25]. É particularmente elevado (1- 4%) para as mulheres que desenvolvem síndrome de hiperestimulação ovariana grave (OHSS) no curso [27,28].
Terapia de substituição hormonal e risco VTE
A terapia de reposição hormonal (HRT) é utilizada para tratar sintomas da menopausa e doenças causadas por deficiência de estrogénio. A HRT não visa manter os níveis hormonais anteriores, mas sim eliminar sintomas tais como afrontamentos, perturbações do sono, humor depressivo ou queixas urogenitais devido à atrofia da mucosa com a dose eficaz mais baixa. Como a monoterapia com estrogénios está associada a um risco acrescido de carcinoma endometrial, são normalmente utilizados preparados combinados.
Tanto as preparações de monopreparações de estrogénio como as preparações de combinação de estrogénio-progestogénio estão associadas a um risco de VTE aproximadamente 2-3 vezes maior [29]. Para as mulheres com VTE anteriores, foi mesmo descrito um aumento de risco de cerca de 4 vezes [30,31]. Tal como na contracepção hormonal, o risco de TEV aumenta com a dose de estrogénio e dependendo do componente progestogénico (Fig. 1). O risco é mais elevado no primeiro ano de utilização e permanece elevado durante o período de utilização. Aumenta com a idade e a obesidade. Ao contrário do que acontece com as CHD, o risco não parece ser aumentado com a aplicação transdérmica [32,33].

Conclusão para a prática
Conhecendo o aumento do risco de eventos tromboembólicos, uma composição com o menor risco conhecido de trombose deve ser preferida ao prescrever uma CHD. Além disso, todas as mulheres que utilizam uma CHD devem ser informadas sobre o aumento do risco de tromboembolismo. O mesmo se aplica às mulheres que utilizam métodos de inseminação artificial ou que devem ser submetidas a HRT durante a menopausa. Antes de prescrever, devem ser investigados factores de risco individuais adicionais, tais como eventos de trombose venosa e arterial na própria história do paciente ou da família, uma trombofilia conhecida, o tabagismo ou a obesidade. A mulher deve também ser informada sobre os sinais que indicam trombose ou embolia pulmonar, para que possa procurar ajuda médica imediatamente se desenvolver sintomas.
Mensagens Take-Home
- A terapia com preparados combinados de estrogénio e progestagénio aumenta o risco de tromboembolismo, pelo que a extensão do aumento do risco depende da dose de estrogénio, bem como da componente de progestagénio.
- O risco de TEV é mais elevado no primeiro ano de utilização, mas permanece elevado depois disso em comparação com as mulheres que não tomam TEV.
- De acordo com os conhecimentos actuais, as preparações monoprogestogénicas (oral ou DIU) não aumentam o risco de trombose.
- As directrizes actuais recomendam a contracepção segura em casos de TEV comprovados; a utilização contínua de CHD é possível desde que o paciente esteja em anticoagulação totalmente terapêutica.
- Após um evento VTE associado a hormonas, o risco de recidiva é baixo se a terapia com um fármaco combinado for interrompida antes de se parar a anticoagulação.
Literatura:
- Rott H: Pílulas anticoncepcionais e Riscos Trombóticos: Diferenças de Métodos Contraceptivos com e sem Estrogénio. Hamostaseology 2019; 39(1): 42-48; doi: 10.1055/s-0039-1677806.
- Tchaikovski SN, Rosing J: Mecanismos de tromboembolismo venoso induzido por estrogénio. Thrombosis Research 2010; 126(1): 5-11; doi: 10.1016/j.thromres.2010.01.045.
- Oger E, Alhenc-Gelas M, Lacut K, et al: efeitos diferenciais dos regimes de estrogénio/progesterona oral e transdérmico sobre a sensibilidade à proteína C activada entre mulheres na pós-menopausa: um ensaio aleatório. Arterioscler Thromb Vasc Biol 2003; 23(9): 1671-1676; doi: 10.1161/01.ATV.0000087141.05044.1F.
- Tans G, van Hylckama Vlieg A, Thomassen MCLGD, et al: A resistência à proteína C activada determinada com um teste baseado na geração de trombina prediz a trombose venosa em homens e mulheres. Br J Haematol 2003; 122(3): 465-470; doi: 10.1046/j.1365-2141.2003.04443.x.
- Tyler ET: Contracepção oral e trombose venosa. JAMA 1963; 185(2): 131; doi: 10.1001/jama.1963.03060020091034.
- Dragoman MV, Tepper NK, Fu R, et al: Uma revisão sistemática e meta-análise do risco de trombose venosa entre os utilizadores de contracepção oral combinada. Int J Gynaecol Obstet 2018; 141(3): 287-294; doi: 10.1002/ijgo.12455.
- Bastos M de, Stegeman BH, Rosendaal FR, et al: Contraceptivos orais combinados: trombose venosa. Cochrane Database Syst Rev 2014; (3): CD010813; doi: 10.1002/14651858.CD010813.pub2.
- Lidegaard O, Nielsen LH, Skovlund CW, et al: Venous trombosis in users of non-oral hormonal contraception: follow-up study, Dinamarca 2001-10. BMJ 2012; 344: e2990; doi: 10.1136/bmj.e2990.
- Lidegaard Ø, Nielsen LH, Skovlund CW, et al: Risk of venous tromboembolism from use of oral contraceptives containing different progestogens and oestrogen doses: Danish cohort study, 2001-9. BMJ 2011; 343: d6423; doi: 10.1136/bmj.d6423.
- Bistervels IM, Scheres LJJ, Hamulyák PT, et al: Sex matters: Practice 5P’s when treating young women with venous tromboembolism. J Thromb Haemost 2019; 17(9): 1417-1429; doi: 10.1111/junho.14549.
- Directriz AWMF S3. Contracepção hormonal. AWMF número de registo 015/015.
- van Vlijmen EFW, Wiewel-Verschueren S, Monster TBM, et al: Contraceptivos orais combinados, trombofilia e o risco de tromboembolismo venoso: uma revisão sistemática e meta-análise. J Thromb Haemost 2016; 14(7): 1393-1403; doi: 10.1111/junho.13349.
- Wu O, Robertson L, Langhorne P, et al: Contraceptivos orais, terapia de reposição hormonal, trombofilias e risco de tromboembolismo venoso: uma revisão sistemática. O Estudo Thrombosis: Risk and Economic Assessment of Thrombophilia Screening (TREATS). Thromb Haemost 2005; 94(1): 17-25; doi: 10.1160/TH04-11-0759.
- Suchon P, Resseguier N, Ibrahim M, et al: Common Risk Factors Add to Inherited Thrombophilia to Predict Venous Thromboembolism Risk in Families. TH Open 2019; 3(1): e28-e35; doi: 10.1055/s-0039-1677807.
- Hugon-Rodin J, Horellou MH, Conard, J et al: Tipo de Contraceptivos Combinados, Factor V, Mutação Leiden e Risco de Tromboembolismo Venoso. Thromb Haemost 2018; 118(5): 922-928; doi: 10.1055/s-0038-1641152.
- Klok FA, Barco S: Gestão óptima dos contraceptivos hormonais após um episódio de tromboembolismo venoso. Thrombosis Research 2019; 181: S1-S5; doi: 10.1016/S0049-3848(19)30357-3.
- van Hylckama Vlieg A, Helmerhorst FM, Rosendaal FR: O risco de trombose venosa profunda associada a contraceptivos de acetato de depósito-medroxiprogesterona injectável ou um dispositivo intra-uterino levonorgestrel. Arterioscler Thromb Vasc Biol 2010; 30(11): 2297-2300; doi: 10.1161/ATVBAHA.110.211482.
- Martinelli I, Lensing AWA, Middeldorp S, et al: Tromboembolismo venoso recorrente e hemorragia uterina anormal com uso de anticoagulante e terapia hormonal. Sangue 2016; 127(11): 1417-1425; doi: 10.1182/blood-2015-08-665927.
- Kearon C, Ageno W, Cannegieter SC, et al: Categorização dos pacientes como tendo provocado ou não provocado tromboembolismo venoso: orientação do SSC do ISTH. J Thromb Haemost 2016; 14(7): 1480-1483; doi: 10.1111/junho.13336.
- Douketis J, Tosetto A, Marcucci M, et al. Risco de recidiva após tromboembolismo venoso em homens e mulheres: meta-análise ao nível do paciente. BMJ 2011; 342: d813; doi: 10.1136/bmj.d813.
- Christiansen SC, Lijfering WM, Helmerhorst FM, et al: Diferença sexual no risco de trombose venosa recorrente e o perfil de risco para um segundo evento. J Thromb Haemost 2010; 8(10): 2159-2168; doi: 10.1111/j.1538-7836.2010.03994.x.
- Vaillant-Roussel H, Ouchchane L, Dauphin C, et al: Factores de risco de recorrência de tromboembolismo venoso associado ao uso de contraceptivos orais. Contracepção 2011; 84(5): e23-30; doi: 10.1016/j.contraception.2011.06.008.
- Eischer L, Eichinger S, Kyrle PA: O risco de recorrência em mulheres com tromboembolismo venoso enquanto utilizam estrogénios: um estudo de coorte prospectivo. J Thromb Haemost 2014; 12(5): 635-640; doi: 10.1111/junho.12528.
- van Es N, Coppens M, Schulman S, et al: Anticoagulantes orais directos comparados com antagonistas da vitamina K para o tromboembolismo venoso agudo: provas da fase 3 dos ensaios. Sangue 2014; 124(12): 1968-1975; doi: 10.1182/blood-2014-04-571232.
- Henriksson P, Westerlund E, Wallén H, et al: Incidência de tromboembolismo pulmonar e venoso em gravidezes após fertilização in vitro: estudo transversal. BMJ 2013; 346: e8632; doi: 10.1136/bmj.e8632.
- Rova K, Passmark H, Lindqvist PG: Tromboembolismo venoso em relação à fertilização in vitro: uma abordagem para determinar a incidência e o aumento do risco em ciclos bem sucedidos. Fertil Steril 2012; 97(1): 95-100; doi: 10.1016/j.fertnstert.2011.10.038.
- Sennström M, Rova K, Hellgren M, et al: Thromboembolismo e fertilização in vitro – uma revisão sistemática. Acta Obstet Gynecol Scand 2017; 96(9): 1045-1052; doi: 10.1111/aogs.13147.
- Bates SM, Greer IA, Middeldorp S, et al: VTE, trombofilia, terapia antitrombótica, e gravidez: Terapia Antitrombótica e Prevenção da Trombose, 9ª ed: American College of Chest Physicians Evidence-Based Clinical Practice Guidelines. Peito 2012; 141(2 Suppl): e691S-e736S; doi: 10.1378/chest.11-2300.
- Canonico M, Plu-Bureau G, Lowe GDO, et al: Terapia de substituição hormonal e risco de tromboembolismo venoso em mulheres na pós-menopausa: revisão sistemática e meta-análise. BMJ 2008; 336(7655): 1227-1231; doi: 10.1136/bmj.39555.441944.BE.
- Cushman M, Kuller LH, Prentice R, et al: Estrogénio mais progestina e risco de trombose venosa. JAMA 2004; 292(13): 1573-1580; doi: 10.1001/jama.292.13.1573.
- Høibraaten E, Qvigstad E, Arnesen H, et al: Aumento do risco de tromboembolismo venoso recorrente durante a terapia de reposição hormonal – resultados do ensaio de tromboembolismo venoso (EVTET) aleatorizado, duplo-cego, controlado por placebo. Thromb Haemost 2000; 84(6): 961-967.
- Roach REJ, Lijfering WM, Helmerhorst FM, et al: O risco de trombose venosa em mulheres com mais de 50 anos de idade usando contracepção oral ou terapia hormonal pós-menopausa. J Thromb Haemost 2013; 11(1): 124-131; doi: 10.1111/junho.12060.
- Renoux C, Dell’Aniello S, Suissa S: Terapia de substituição hormonal e o risco de tromboembolismo venoso: um estudo baseado na população. J Thromb Haemost 2010; 8(5): 979-986; doi: 10.1111/j.1538-7836.2010.03839.x.
- Mannucci PM, Franchini M: Variantes clássicas de genes trombofílicos. Thromb Haemost 2015; 114(5): 885-889; doi: 10.1160/TH15-02-0141.
- Linnemann B, Hart C: Diagnóstico laboratorial em trombofilia. Hamostaseology 2019; 39(1): 49-61; doi: 10.1055/s-0039-1677840.
- www.bfarm.de/DE/Arzneimittel/Pharmakovigilanz/KOK/_node.html; recuperado em: 7.12.2020.
PRÁTICA DO GP 2021; 16(1): 8-13