Este artigo dá uma visão geral das diferentes formas de dermatoses auto-imunes bolhosas e um resumo das recomendações terapêuticas e opções de tratamento actualmente válidas. Os imunossupressores clássicos influenciam os processos metabólicos das células T e B a nível celular. Além disso, várias terapias orientadas foram estabelecidas nos últimos anos.
As doenças auto-imunes com bolhas são geralmente doenças graves da pele – e frequentemente também das membranas mucosas. Caracterizam-se pelo aparecimento de autoanticorpos IgG ou IgA contra as proteínas estruturais da pele. Estas proteínas estruturais são de grande importância para a adesão celular dos queratinócitos (doenças pemphigus) ou para a adesão da epiderme à derme (doenças pemphigoides, epidermolysis bullosa acquisita, dermatitis herpetiformis).
Assim, a bolha ocorre intra-epidermalmente nas doenças pênfigo e subepidermalmente nas outras doenças auto-imunes bolhosas. A grande heterogeneidade clínica e os diferentes cursos representam também um desafio terapêutico para os dermatologistas. Os glucocorticosteróides locais e orais são o tratamento de primeira linha, excepto para a dermatite herpetiforme. As medidas de terapia aditiva são necessárias sob terapia sistémica com corticosteróides (visão geral 1). A fim de salvar os corticosteróides, estes são combinados com mais imunossupressores no curso.
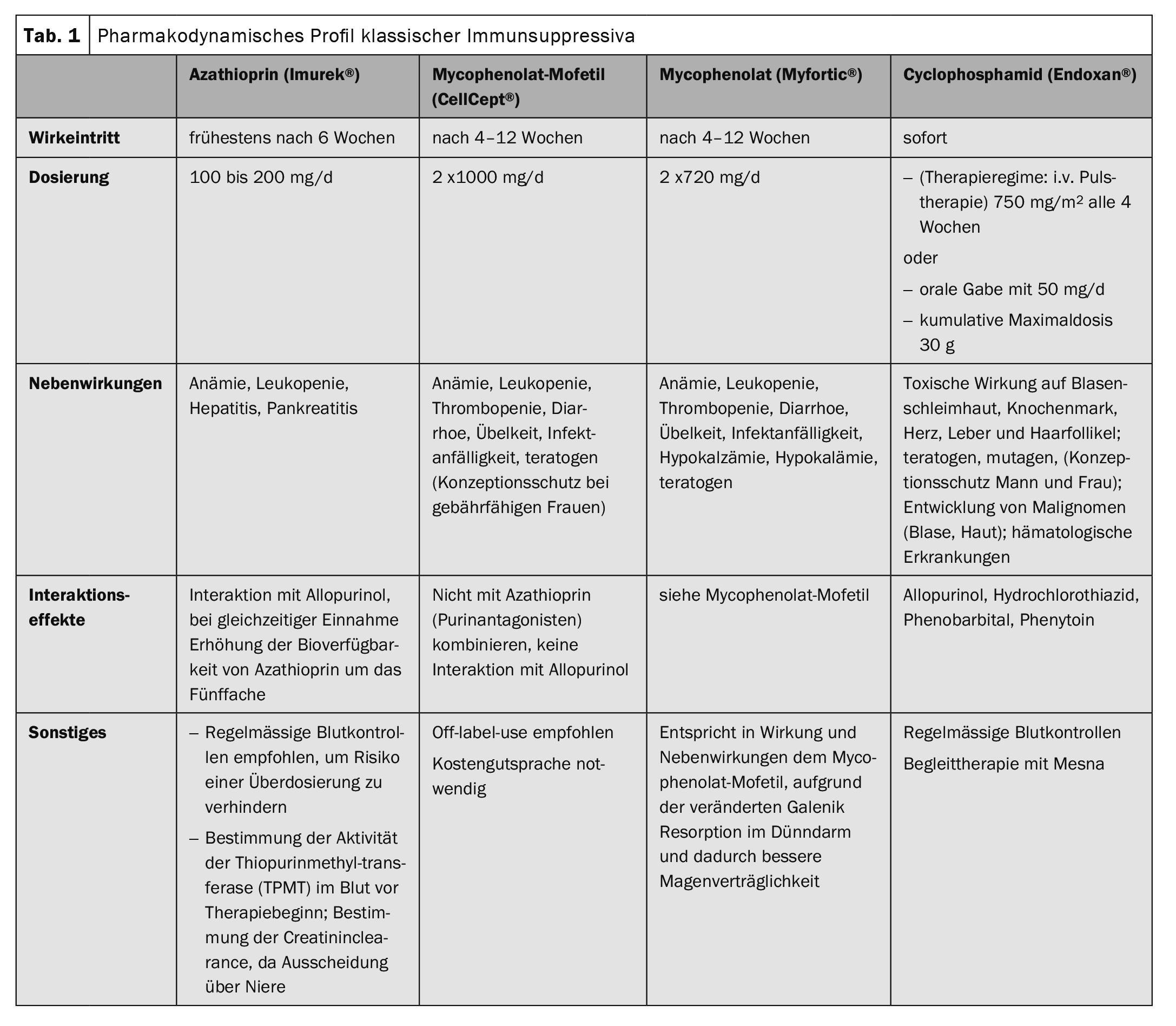
Nos últimos anos, os medicamentos imunossupressores clássicos têm sido (Tab. 1), que influenciam os processos metabólicos das células T e B a nível celular, são complementados por terapias orientadas. (Fig. 1). Essencialmente, isto envolve rituximab (Tab. 2), método de imunoadsorção (Tab. 3) e a utilização de imunoglobulinas de alta dose. (Tab. 4). Rituximab é um anticorpo quimérico anti-CD20 para esgotamento das células periféricas B que formam auto-anticorpos (Tab. 2).
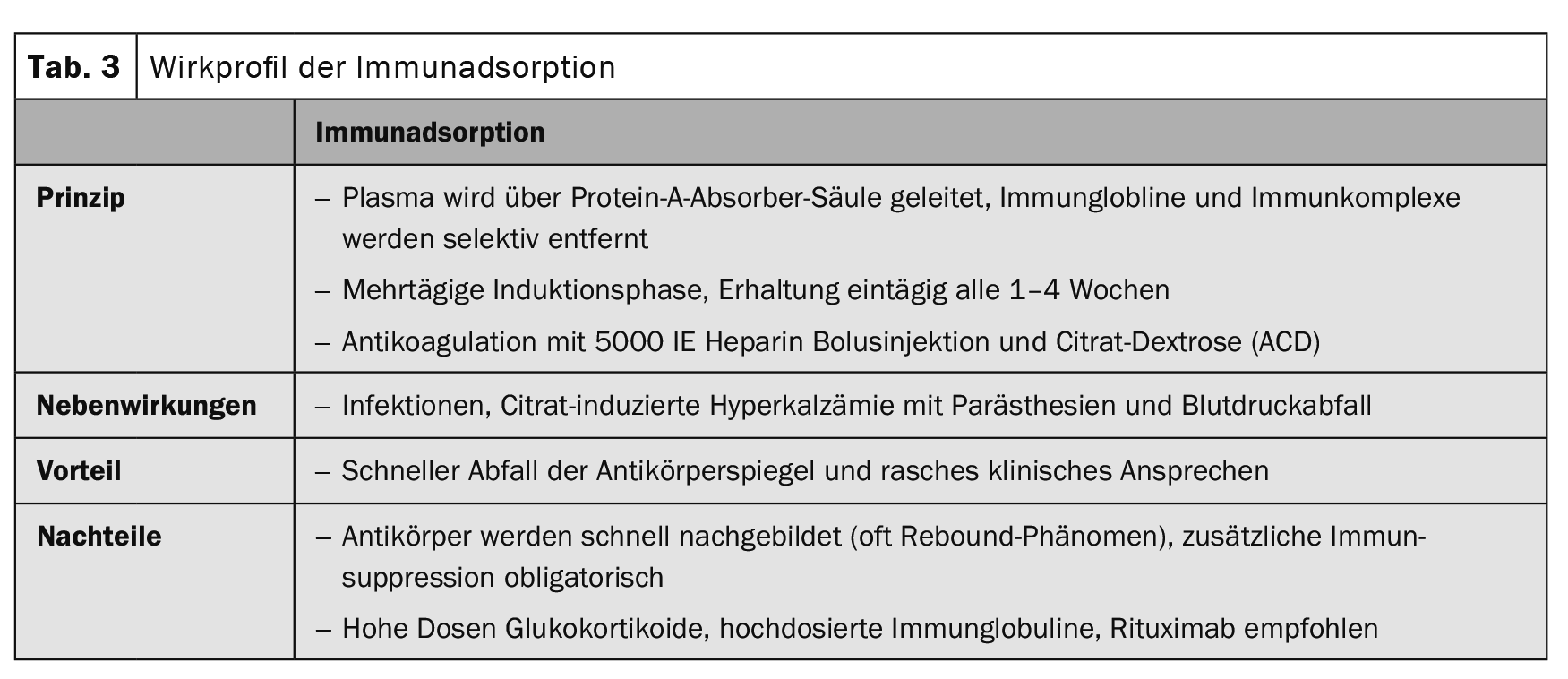
Nos procedimentos de imunoadsorção, os auto-anticorpos e os complexos imunitários são selectivamente removidos do plasma através de absorvedores de alta afinidade (Tab. 3).
As imunoglobulinas intravenosas de dose elevada destinam-se a neutralizar mediadores inflamatórios e auto-anticorpos (Quadro 4).
Durante a terapia com imunossupressores, há um risco acrescido de reactivação de infecções latentes, pelo que infecções como o VIH, hepatite B, tuberculose e infecções bacterianas crónicas devem ser excluídas antes de se iniciar a terapia. Podem ocorrer infecções oportunistas por candida e herpes (herpes simplex, varicella zoster) durante a terapia. Foi descrito um risco acrescido de distúrbios linfoproliferativos e tumores cutâneos durante a terapia a longo prazo com imunossupressores. Devido ao aumento da fotocarcinogénese, é necessária uma protecção UV e inspecções regulares da pele. Antes de iniciar a terapia imunossupressora, verificar o estado de vacinação do paciente. Vacinações com vacinas vivas durante a terapia imunossupressora são contra-indicadas, e as vacinas com vacinas atenuadas podem ter reduzido o sucesso. Em doentes com mais de 50 anos de idade, é indicada a vacinação contra a herpes zoster-subunit-tot [1].
Doenças de pênfigo
Pemphigus vulgaris, pemphigus foliaceus e pemphigus paraneoplastic pemphigus são subsumidos sob este termo guarda-chuva. Os glucocorticosteróides sistémicos estão no centro da terapia. Dependendo da gravidade da doença, as doses iniciais correspondem a 1-2 mg/kg de equivalente de prednisolona por dia. A terapia de consolidação depende da actividade da doença. Se não aparecerem novas bolhas durante 8 dias, a dose de esteróides é reduzida em 25% a cada 2-4 semanas. A partir de 30 mg de equivalente de prednisolona por dia, a redução adicional é ainda mais lenta. O objectivo é atingir o limiar de Cushing (7,5 mg de prednisolona). A fim de salvar os glucocorticosteróides, estes são combinados com outros imunossupressores (Tab. 1) . A dose do medicamento imunossupressor permanece inalterada – desde que não haja efeitos secundários – durante toda a duração da terapia.
O imunossupressor adjuvante mais comum é a azatioprina numa dosagem de 100-150 mg/d. Em caso de redução da actividade enzimática da tiopurina metiltransferase ou administração simultânea de alopurinol, a dose deve ser reduzida. As amostras de sangue devem ser colhidas antes e durante a terapia (Quadro 1).
Se ocorrerem efeitos secundários com azatioprina, micofenolato mofetil ou, no caso de efeitos secundários gastrointestinais, é utilizado ácido micofenólico . Ambos os fármacos têm um efeito de dispersão de esteróides e levam a uma remissão mais rápida (Tab. 1) .
Em cursos muito refractários, a ciclofosfamida pode ser combinada com corticosteróides. A ciclofosfamida é uma substância alquilante, ou seja, uma substância de ligação cruzada de ADN com efeitos irreversíveis na reserva ovárica e na espermatogénese, sendo por isso obsoleta em doentes mais jovens. Além disso, podem ocorrer vários efeitos secundários tóxicos e desenvolvimento de malignidades (Tab. 1) . A aprovação na UE foi, portanto, limitada às doenças auto-imunes com risco de vida em 2012.
Os ensaios clínicos prospectivos, multicêntricos e randomizados com e sem corticosteróides demonstraram a eficácia do rituximab (Quadro 2) com remissões de até 80% após 24 meses. Os títulos de autoanticorpos (anti-desmoglein I e III) caíram lentamente nas primeiras semanas após a infusão e atingiram os valores mais baixos após cerca de 180 dias. Foi observada uma resposta clínica ao fim de 2-3 meses. Com base nos estudos, rituximab foi aprovado para o tratamento inicial de pênfigo grave e moderado nos EUA em Junho de 2018 [2,3]. Foi concedida uma aprovação da UE para o pemphigus vulgaris em meados de 2019.
Os resultados do primeiro estudo sobre imunoadsorção (IA) (Tab. 3) em pênfigo foram publicados em 2007 [4]. Entretanto, foram publicados mais de 100 pacientes com diferentes protocolos terapêuticos. Em contraste com o rituximab, todas as séries de casos mostraram uma rápida diminuição de auto-anticorpos e uma rápida melhoria clínica, mas também uma elevada taxa de recaídas após um curto período de tempo. A combinação de IA com rituximab resultou em remissões rápidas e duradouras [5].
Séries de casos e relatórios de casos individuais relataram uma boa resposta após várias séries terapêuticas de imunoglobulinas intravenosas de alta dose (IVIG) (Quadro 4) em combinação com glucocorticosteróides em pênfigo vulgar e pênfigo paraneoplásico como terapia de segunda ou terceira linha após falha da terapia imunossupressora combinada. Só após vários meses de terapia é que houve uma resposta.
Penfigóide Bolhoso
A terapia do pemfigoide bolhoso deve ser adaptada à actividade da doença e às comorbilidades de cada paciente individual. Geralmente, são utilizados métodos terapêuticos mais suaves do que para as doenças de pênfigo. Em tratamentos pemfigoidais bolhosos localizados e moderados, desinfectantes e anti-inflamatórios tópicos com propionato de clobetasol duas vezes por dia são muitas vezes suficientes. No entanto, o tratamento tópico de grande área duas vezes por dia é muitas vezes impraticável em doentes idosos. O tratamento sistémico é geralmente necessário. A terapia sistémica com um equivalente inicial de 0,5 mg/kg/d de prednisolona em combinação com imunossupressores adjuvantes, tais como azatioprina, ou micofenolato mofetil, para poupar glucocorticoides, é a terapia de primeira escolha, para além do tratamento tópico (Quadro 1) . Outras terapias adjuvantes incluem o metotrexato (15 mg/semana), dapsona (100 mg/d, Separador. 5) e tetraciclina (200 mg/d) foram descritas. Numa série de casos com 20 doentes, a imunoadsorção (Tabela 3) foi capaz de mostrar uma diminuição rápida dos níveis de autoanticorpos de pemfigoide bolhoso no soro e um efeito terapêutico associado [6].
Pemfigoide de membrana mucosa
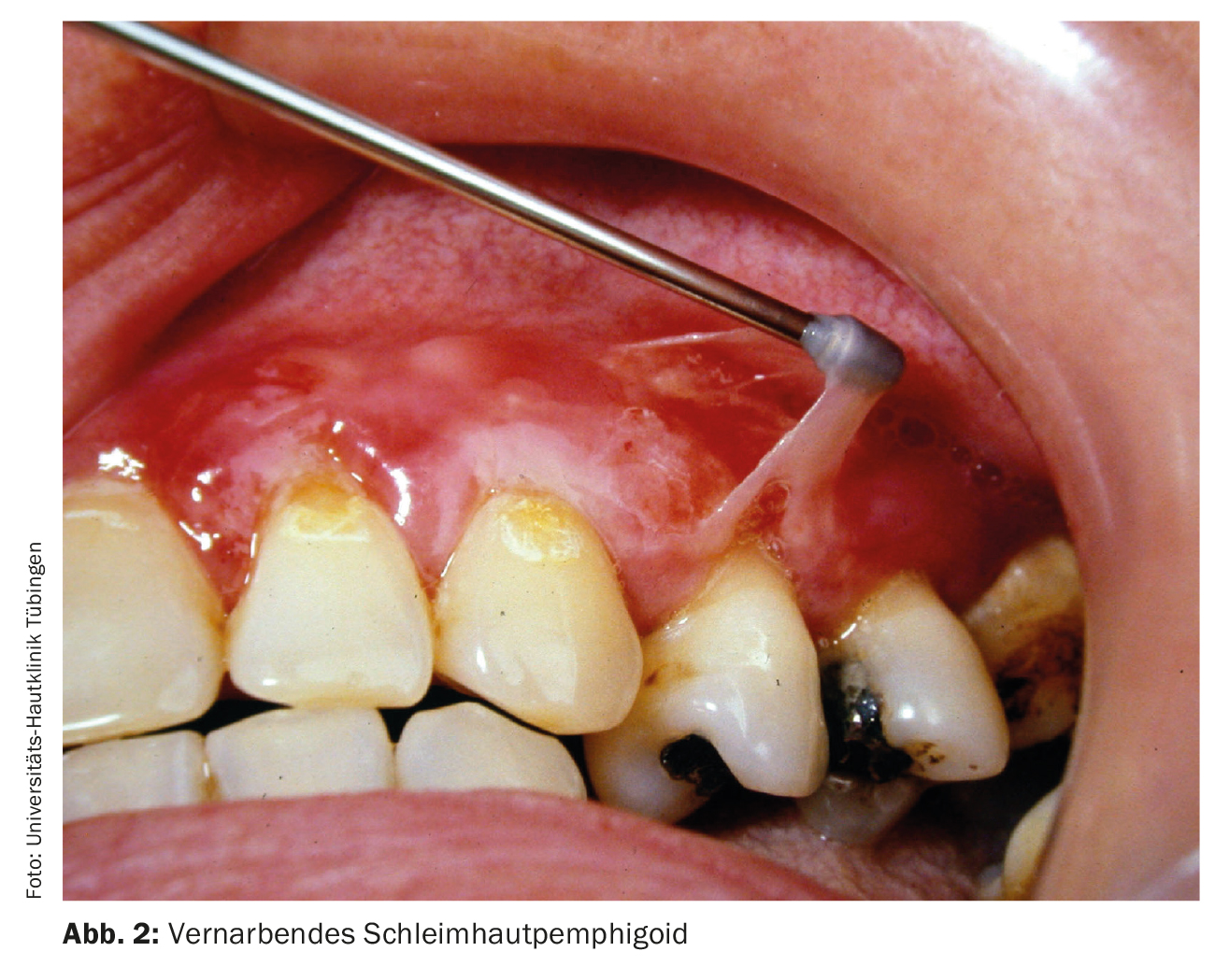
Esta dermatose auto-imune é também chamada pemfigoide cicatrizante. A doença é caracterizada por uma grande heterogeneidade clínica com e sem cicatrizes. Todas as membranas mucosas com epitélio escamoso (mucosa oral, conjuntiva, nasofaringe, esófago, vulva e recto) podem ser afectadas. A terapia depende da manifestação clínica; acima de tudo, devem ser evitadas as cicatrizes (Fig. 2). Para além das doses elevadas de glicocorticóides em combinação com imunossupressores adjuvantes, a terapia com ciclofosfamida (Tab. 1), IVIG (Tab. 4) ou rituximab (Tab. 2) também pode ser recomendada para pacientes refractários [7].
Dermatose linear de IgA
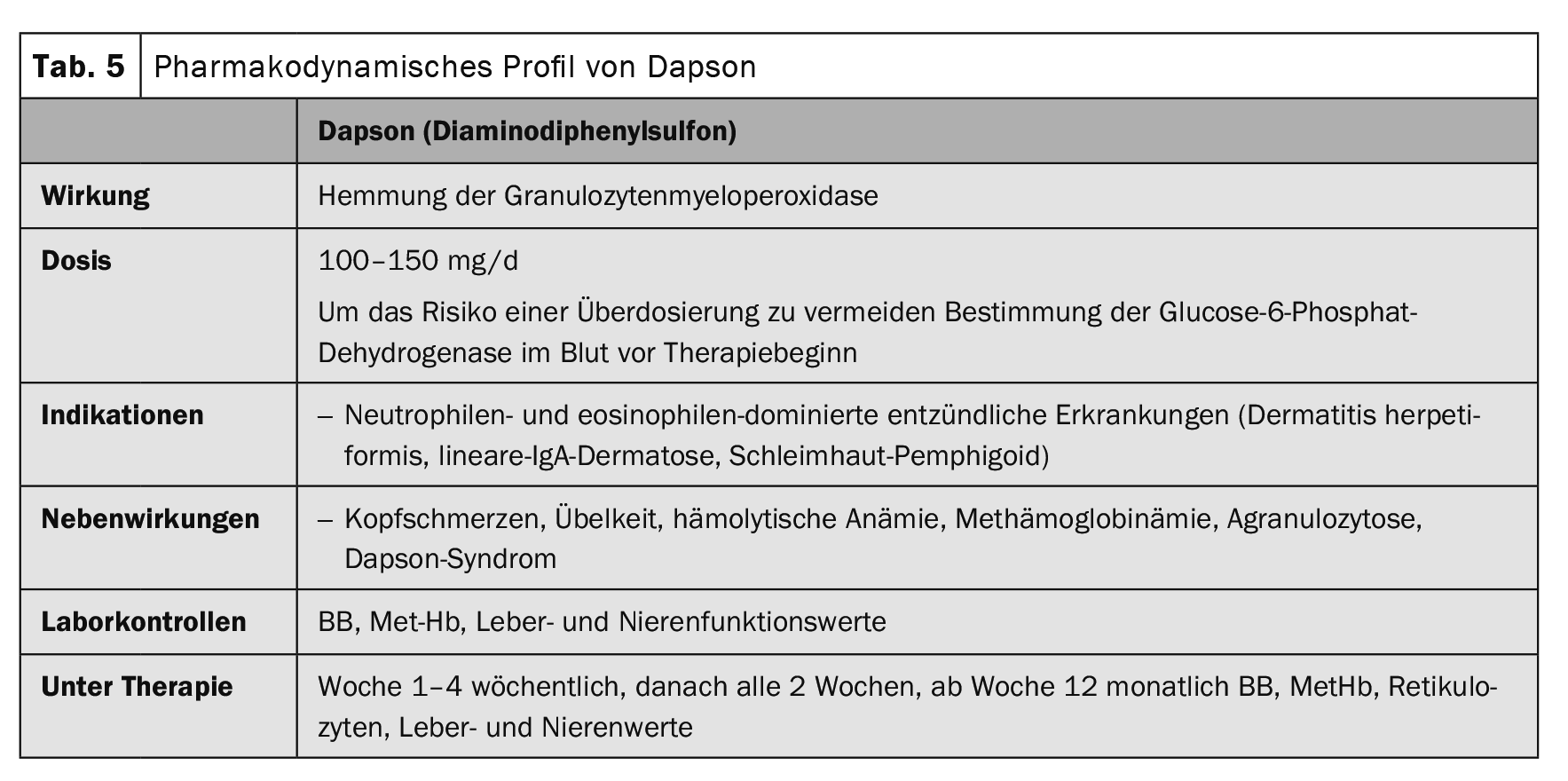
Os agentes de primeira linha para dermatoses IgA lineares são glucocorticosteróides e dapsona (Tabela 5) . Os glucocorticosteróides são muito menos eficazes nesta doença do que no pemphigus ou no pemphigoide bolhoso. Imunoadsorção (Quadro 3), IVIG (Quadro 4) e rituximab (Quadro 2) [8,9] foram descritos como eficazes nos relatórios de casos.
Epidermólise bullosa acquisita
A epidermólise bullosa acquisita mostra uma resistência marcada à terapia em muitos casos. A forma mecanobolhosa em particular é frequentemente refractária ao tratamento com glucocorticóides em combinação com imunossupressores adjuvantes tais como azatioprina ou micofenolato mofetil. (Tab. 1). Numa série de casos com 3 pacientes e em relatórios de casos individuais, foi demonstrado que Rituximab (tab. 2) como monoterapia conduz a remissões duradouras em mais de metade dos pacientes e em combinação com IVIG (tab. 4 ) ou imuno-adsorção (tab. 3 ) em mais de 75% dos pacientes. [10].
Dermatite herpetiforme Duhring
Além da doença de pele, uma enteropatia sensível ao glúten (doença celíaca) está sempre presente ao mesmo tempo, embora mais de 80% dos doentes não apresentem quaisquer sintomas gastrointestinais, mas tenham geralmente atrofia subclínica das vilosidades ou inflamação no jejuno. A terapia é baseada numa dieta sem glúten para toda a vida. Uma dieta sem glúten também previne a ocorrência de linfoma não-Hodgkin e provavelmente também de carcinomas no tracto digestivo. O efeito da dieta sem glúten na pele só aparece após vários meses, de modo que a dapsona (quadro 5) deve ser sempre utilizada inicialmente. A enteropatia subjacente não é afectada pela dapsona. Em caso de intolerância à dapsona, pode ser administrada sulfasalazina ou colchicina.
Resumo
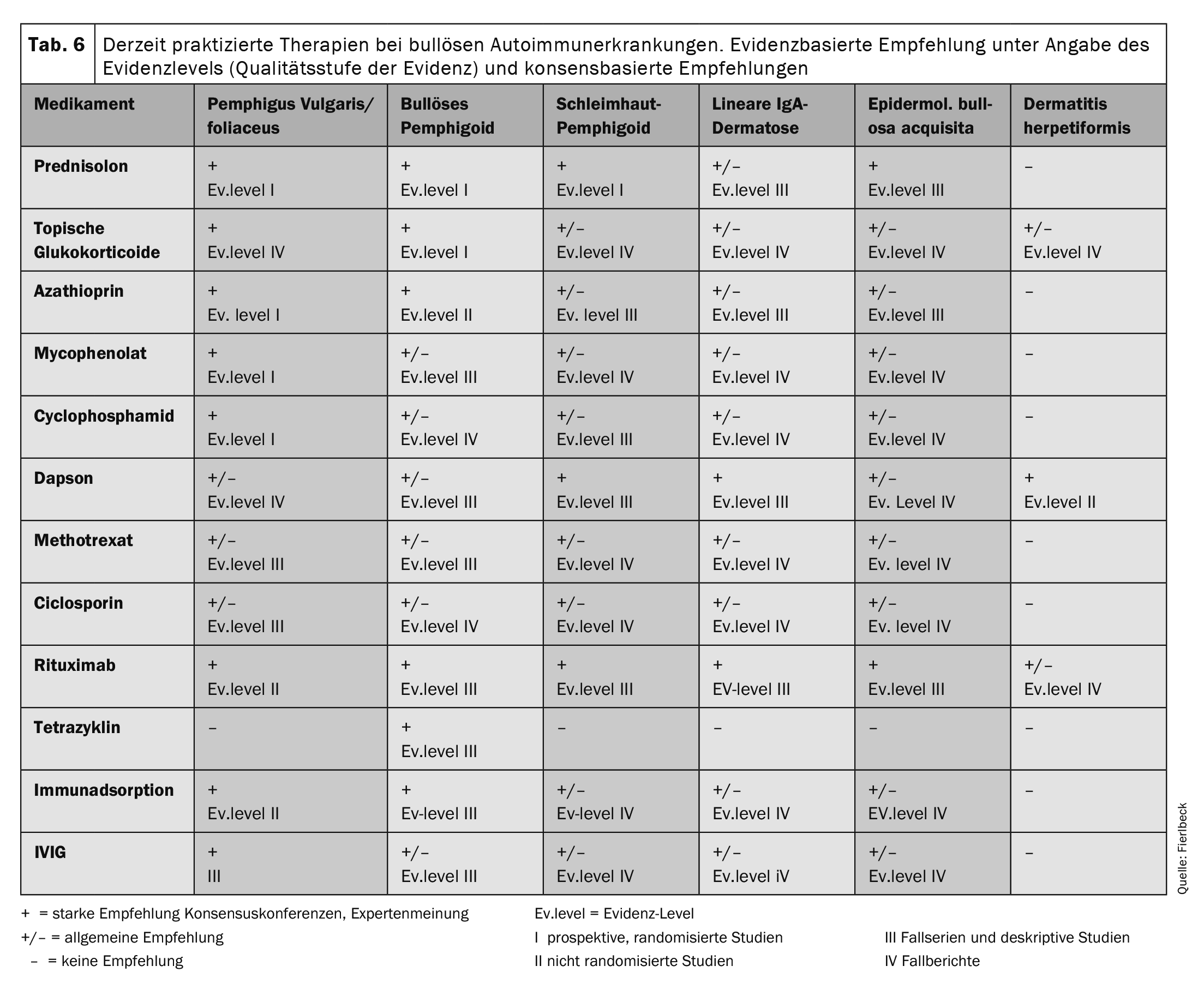
O Quadro 6 dá uma visão geral das terapias actualmente praticadas . As recomendações terapêuticas baseiam-se em estudos clínicos (nível de evidência) e recomendações gerais (conferências de consenso, opiniões de especialistas).
Mensagens Take-Home
- Os glucocorticosteróides locais e orais em combinação com azatioprina são agentes de primeira linha, excepto no caso da dermatite herpetiforme.
- No pemphigoid bullous, pode ser feito um ensaio de glucocorticosteróides tópicos potentes. Contudo, a terapia oral com baixas doses de glucorticosteróides em combinação com azatioprina é geralmente necessária.
- Em dermatoses auto-imunes bulosas graves e refractárias, é necessário Rituximab indicado. Devido ao efeito retardado do rituximab, existem combinam inicialmente glucocorticosteróides.
- A imuno-adsorção leva a uma melhoria clínica em poucos dias; é necessária uma imunossupressão adicional devido à rápida recuperação de auto-anticorpos e deterioração clínica.
- Na dermatite herpetiforme, é necessária uma dieta vitalícia sem glúten, mesmo sem a presença de enteropatia manifesta. Dapsone é a droga de primeira escolha. O efeito da dieta sem glúten só se instala após meses, a dapsona funciona em poucos dias.
Literatura:
- STIKO: Comunicação da Comissão Permanente de Vacinação (STIKO) no RKI. Justificação científica para recomendar a vacinação com a vacina total da subunidade herpes zoster. Instituto Robert Koch (RKI), Boletim Epidemiológico 50, 13.12.2018. www.rki.de
- Jolly P, et al: Rituximab de primeira linha combinado com prednisolona de curto prazo apenas para o tratamento de pênfigo. Lancet 2017; 389(10083): 2031-2040.
dx.doi.org/10.1016/SO140-6736(17)30070-3 - Murrell DF, et al: Diagnóstico e gestão de pemphigus: recomendação por um painel internacional de peritos. J Am Acad Dermatol 2018 Fev 10. pii: S0190-9622(18)30207-X. doi: 10.1016/j.jaad.2018.02.021. [Epub ahead of print]
- Zillikens D, et al: Recomendação para o uso da imunoferese no tratamento da doença bolhosa auto-imune. JDDG 2007; 5(10): 366-373.
- Behzad M, et al: O tratamento combinado com imunoadsorção e rituximab leva a uma remissão clínica rápida e prolongada em pemphigus vulgaris. Br J Dermatol 2012; 166(4): 844-852.
- Hübner F, et al: Tratamento adjuvante de pemfigoide bolhoso grave/refractário com imunoadsorção de proteína A. JDDG 2008; 16(9): 1109-1119.
- Le-Roux-Viller C, et al: Rituximab para doentes com pemfigoide de membrana mucosa refractária. Arch Dermatol 2011; 147(7): 843-849.
- Enk A, et al: Utilização de imunoglobulinas de alta dose em dermatologia. JDDG 2009; 7(9): 806-812.
- Pinard C, et al: Dermatose linear de IgA bullous dermatosis pisada com rituximab. Processo JAAD Rep. 2019; 5(2): 124-126. doi: 10.1016/j.jdcr.2018.11.004
- Bevans SL, Sami N: The Use of Rituximab in treatment of epidermolysis bullosa acquisita: Três novos casos e uma revisão da literatura. Dermatol Ther 2018; 31(6): e12726. doi: 10.1111/dth12726 [Epub 2018 Oct 3]
DERMATOLOGIE PRAXIS 2023; 30(1) : 14–19