O carcinoma hepatocelular (HCC) é o tumor primário de células hepáticas mais comum e, com a sua resistência intrínseca aos agentes quimioterápicos clássicos, apresenta um desafio no tratamento sistémico. O clínico responsável deve não só avaliar a situação tumoral com um possível efeito terapêutico – mas também um cuidadoso equilíbrio entre os benefícios do tratamento e o risco de descompensação hepática.
O carcinoma hepatocelular (HCC) é o tumor hepático primário mais comum e, com a sua resistência intrínseca aos agentes quimioterápicos clássicos, representa um desafio no tratamento sistémico [1]. Para além das opções terapêuticas até agora limitadas numericamente no tratamento sistémico, a doença hepática avançada é também predominantemente decisiva para o prognóstico. Não só os factores de risco conhecidos de cirrose hepática, como a hepatite viral HBV ou HCV, mas também o álcool desempenham um papel. Por vezes o fígado gordo, que está a aumentar na nossa região, bem como o fígado gordo não alcoólico (NAFLD), não é apenas um factor de risco de HCC. Pelo contrário, o desempenho hepático reduzido associado a isto é também um factor de prognóstico no tratamento do HCC [2]. O clínico responsável deve, portanto, não só avaliar a situação do tumor com um possível efeito terapêutico – é necessário um equilíbrio cuidadoso entre os benefícios do tratamento e o risco de descompensação hepática. Os tratamentos curativos estão reservados para as fases iniciais do HCC usando a classificação BCLC (Barcelona Clinic Liver Cancer) para BCLC 0/A e incluem cirurgia, técnicas ablativas locais ou transplante de fígado. O risco de recidiva após cirurgia ou ablação no fígado pré-dano é bastante elevado, entre 65-85%, dependendo dos estudos, e é precisamente nesta situação que diferentes opções de tratamento estão actualmente a ser investigadas em estudos controlados clinicamente [3]. Para pacientes em HCC “intermédio” ou “avançado”, a especificação da terapia é paliativa. A radioembolização transarterial (TARE) é uma aplicação que é frequentemente utilizada na fase BCLC-B. Também aqui existe um elevado risco de recorrência ou de desenvolvimento de novos focos de HCC no fígado pré-destruído. Assim, este campo terapêutico com boa função hepática preservada é também um campo de interesse actual de tratamentos sistémicos adjuvantes. Após a escolha muito limitada de opções de sistema para HCC no BCLC-C durante muito tempo com os inibidores multikinase (MKI) sorafenib na primeira linha [4] e regorafenib na segunda linha [5], os tratamentos para HCC também se expandiram nos últimos 3,5 anos com terapias combinadas de anticorpos vasculares mais inibidores do ponto de controlo imunitário (ICI) ([6,7]. Além disso, no campo do HCC “avançado” (aHCC), existe actualmente um vivo interesse de estudo em outras combinações, por vezes MKI mais ICI. Estes resultados são aguardados com expectativa, pois não só tais combinações estão a ser investigadas no tratamento de primeira linha, como também algumas combinações terapêuticas estão a ser utilizadas após imunoterapia prévia. Já em finais de 2021, uma combinação de cabozantinib mais atezolizumab em aHCC de primeira linha foi demonstrada no Simpósio virtual da ESMO Ásia com o ensaio COSMIC-312. No início de 2022, um estudo positivo com uma combinação ICI foi apresentado no Simpósio virtual ASCO GI com o estudo HIMALAYA. Gostaria agora de apresentar estes dados, bem como as perspectivas de estudos adicionais para terapias combinadas numa perspectiva simplificada.
Terapias combinadas em aHCC
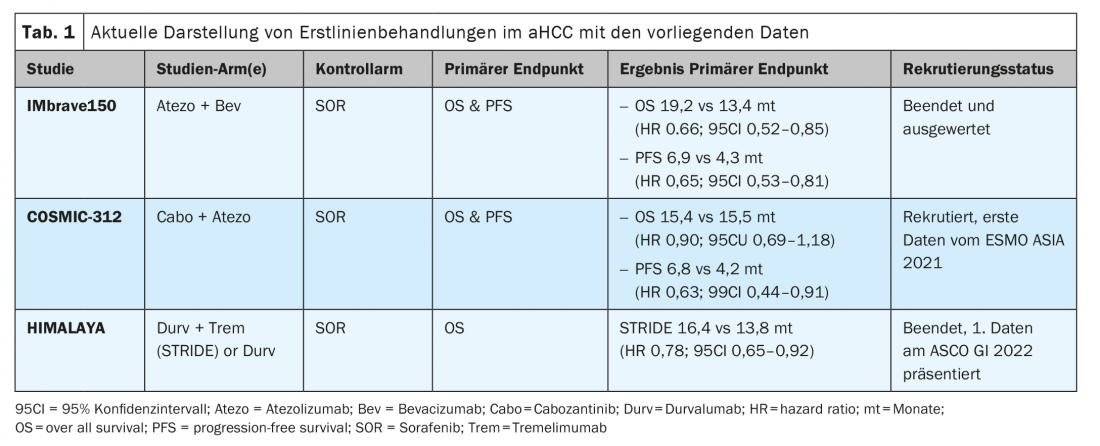
Estudo IMbrave 150 – mais resultados a longo prazo do ASCO 2021: Com o estudo IMbrave 150, foi alcançado um novo padrão terapêutico mundial na primeira linha de tratamento do aHCC no BCLC C, bem como com utilização precoce na fase BCLC B a partir de 2019. [7] Menos de um ano depois, a 16 de Novembro de 2020, a SwissMedic também concedeu aprovação para esta combinação no tratamento de primeira linha de atezolizumab mais bevacizumab na Suíça. Esta combinação conseguiu uma melhoria significativa em mOS e mPFS em comparação com o sorafenib. No ASCO GI 2021 virtual, foram apresentados os dados actuais com intervalos de seguimento mais longos [8]. Os benefícios de sobrevivência significativos pré-estabelecidos em mOS (19,2 vs 13,4 meses; HR 0,66; p=0,0009) e também mPFS (6,9 vs 4,3 meses; HR 0,65; p=0,0001) foram confirmados durante o período de observação mais longo de mais de 18 meses. A redução do risco de morte em 34% e um benefício de sobrevivência global de 5,8 meses em comparação com o sorafenibe também foram alcançados com uma melhoria e estabilização da qualidade de vida [6,9].
Estudo COSMIC-312 – resultados da ESMO Asia 2021: Outras e interessantes combinações consistem em inibidores multikinase (MKI) e inibidores de pontos de controlo (ICI). Sorafenib, cabozantinib ou lenvatinib em combinação com inibidores PD-1 estão actualmente a ser avaliados em armas de ensaio em aHCC. O ensaio COSMIC-312 (NCT03755791) foi concebido em 3 braços para o tratamento de primeira linha de aHCC. O que é interessante aqui é que as fases BCLC-B já podem ser incluídas. Um braço de estudo com monoterapia cabozantinibe (Cabo) e outro braço de estudo na combinação de cabozantinibe mais atezolizumab (Cabo-Atezo) estão a ser comparados com o sorafenibe de braço padrão para o ponto final duplo de mOS e PFS. Os resultados do primeiro estudo de 837 pacientes aleatorizados no ensaio global foram demonstrados na ESMO Asia 2021 [10]. O grupo Cabo-Atezo encontrou o ponto final PFS em comparação com o sorafenibe, mas não houve diferença na sobrevivência global nos dois braços com progressão de curva idêntica (Tabela 1) . Os dados PFS do Cabo Mono eram também significativamente superiores ao sorafenibe, mas os dados do SO ainda não foram demonstrados. Curiosamente, a hepatite B (HBV)-associada ao HCC em particular beneficia da combinação Cabo-Atezo, com um PFS HR 0,49 (95% CI 0,29-0,73). Este subgrupo HBV alcançou um benefício OS com um HR de 0,53 (95% CI 0,33-0,87). O envolvimento extra-hepático (DHE) e a invasão macrovascular (IVM) também indicou um benefício PFS para a terapia de combinação Cabo-Atezo na análise do subgrupo (HR 0,57; 95% CI 0,41-0,78). Em contraste, o HCC não associado à hepatite C (HCV) não parece beneficiar da combinação. Em particular, os asiáticos beneficiaram mais da combinação do que os doentes não asiáticos com CHC, pelo que permanece pouco claro se a infecção pelo HBV ou a etnia é um factor de confusão na análise. Os autores concluíram cautelosamente que a combinação representa uma nova opção no tratamento do HCC. No entanto, as análises finais devem ser aguardadas.
ORIENT-32 – Dados da ESMO 2021: Na ESMO 2021, foram demonstrados os resultados do ensaio ORIENT-32, outra combinação com sintilimab (Sin) e bevacizumab (Bev) versus sorafenib [11]. Na população apenas chinesa, a combinação Pecado + Bev mostrou benefícios de tratamento significativos em termos de OS (NR vs 10,4 meses) e mPFS (4,6 vs 2,8 meses). As taxas de efeito secundário de IMbrave e ORIENT-32 foram mais baixas em comparação com o sorafenibe e foram consistentes com o típico perfil de efeito secundário aVGFR e IO.
Estudo HIMALAYA – combinação de inibidores do ponto de controlo imunitário no aHCC de primeira linha: as terapias de combinação ICI também estão a ser estudadas mais intensamente no aHCC. Por exemplo, a combinação de nivolumab mais tremelimumab (Trem) no aHCC após terapia prévia de sorafenibe já tinha sido aprovada pela FDA em 2019. Outra combinação do ICI aprovada pela FDA desde Janeiro de 2021 é devaruzumab mais tremelimumab. Ambas as combinações são aplicáveis na terapia de segunda linha, mas não são suportadas pela EMA nem pelo Swissmedic. Agora, o ensaio HIMALAYA (NCT03298451) foi recentemente apresentado na ASCO GI 2022 com dados iniciais. O agora estudo de 3 braços com braço STRIDE (tremelimumab mais durvalumab) ou durvalumab mono (Durv) foi comparado contra o sorafenib como o braço padrão. O OS do endpoint primário era significativamente superior no braço STRIDE aos 16,4 meses em comparação com o braço de sorafenibe também muito bom de 13,8 meses (HR 0,78; p=0,0035). Não houve diferenças em PFS, mas houve uma impressionante média de DoR (duração da resposta) de 22,34 meses e uma população de 65,8% de doentes com uma resposta Trem+Durv no período de 12 meses. Estes resultados são muito interessantes para a combinação de inibidores de pontos de controlo e nas análises dos subgrupos até agora, quase todos os grupos foram a favor da utilização desta combinação. A grande discussão sobre a população adequada em comparação com o novo SoC (padrão de cuidados) atezolizumab mais bevacizumab é dada e não é fácil de responder. Na minha opinião, não existem biomarcadores claros para selecção ou atribuição a uma das duas combinações.
Estudos actualmente a recrutar e esperados num futuro próximo
CheckMate 9DW: Este ensaio da fase 3, NCT04039607, está a comparar a combinação de nivolumab (Nivo) mais ipilimumab (Ipi) versus sorafenibe na primeira linha, nas fases planeadas 728 aHCC BCLC-B e BCLC-C. O ponto final primário é o OS e o ensaio está actualmente aberto mas não está a recrutar devido à pandemia COVID 19 (a 28 de Janeiro de 2022 clinicaltrials.gov).
LEAP-002: Este ensaio da fase 3 (NCT03713593) está a comparar o lenvatinibe SoC com a combinação lenvatinib mais pembrolizumab. Como resultado primário, o PFS bem como o SO de ambos os grupos serão comparados. Este estudo também está activo, mas não está actualmente em curso qualquer recrutamento (em 28 de Dezembro de 2021 clinicaltrials.gov).
Estudos de recrutamento de adjuvantes
Não só o campo do aHCC está actualmente a ser intensamente investigado para um efeito de imunoterapias, mas também as fases locais após a cirurgia ou ablação. Uma terapia com placebo é utilizada como grupo de controlo em cada caso. Pembrolizumab está a ser investigado como monoterapia no estudo Keynote-937 (NCT03867084), toripalimab no estudo JUPITER-04 (NCT03859128) ou nivolumab no estudo CheckMate 9Dx (NCT03383458) como terapia adjuvante. O ensaio EMERALD-2 (NCT03847428) incide sobre durvalumab ou a combinação de durvalumab mais bevacizumab na configuração adjuvante. O ensaio ImBrave050 (NCT04102098) também está a investigar a combinação de atezolizumab mais bevacizumab em doentes de alto risco de HCC versus placebo após cirurgia ou ablação. Estes resultados são aguardados ansiosamente em geral, uma vez que os resultados positivos do estudo deslocam a utilização do ICI para uma linha precoce. Assim, no futuro, não só uma expansão do ICI com diferentes combinações em aHCC resultará numa discussão intensificada da colocação nas directrizes, mas também da sequência em caso de recidiva após cirurgia ou ablação, se o ICI tiver sido utilizado neste caso.
Perspectivas e “necessidades não satisfeitas
Os ensaios apresentados são ansiosamente aguardados tanto nas fases locais como nas fases locais avançadas do BCLC-B do HCC e, se os pontos finais forem atingidos, estabelecerão um novo padrão de cuidados. Também nas fases aHCC com BCLC B ou C, muitas perspectivas de estudo com sinais positivos são actualmente esperadas. Assim, podemos esperar uma variedade de novas combinações terapêuticas num futuro próximo. Para além desta perspectiva positiva, existem também questões directas e indirectas com requisitos actualmente (ainda) por resolver. Isto refere-se por um lado à sequência terapêutica óptima de um paciente com CHC e também à questão de diferentes terapias dependendo da hepatopatia subjacente. Em contraste, a questão dos biomarcadores adequados para prognóstico e previsão é ainda insatisfatoriamente resolvida e é também um ponto de vista das actuais questões de investigação. Em particular, a análise da resistência instrínseca ou adquirida à terapia ICI (inibição do ponto de controlo imunitário) desempenha um papel central. Para a aplicação clínica, a segurança e eficácia das terapias em pacientes CHILD-Pugh B, bem como em pacientes pós-transplante, também desempenham um papel, uma vez que isto não foi incluído nos estudos anteriores. Destas questões em aberto surge a necessidade do desenvolvimento e definição de escores clínicos e de diagnóstico para seleccionar os pacientes ideais para a melhor terapia de combinação possível.
Mensagens Take-Home
- O campo de tratamento dentro do BCLC fase C HCC expandiu-se grandemente, incluindo uma combinação de atezolizumab mais bevacizumab actualmente aprovada na Suíça.
- A função hepática e uma boa pontuação Child-Pugh é crucial para a utilização de terapias sistémicas no HCC.
- Os doentes com CHC devem ser avaliados conjuntamente por um hepatologista e um oncologista médico numa fase inicial, de modo a que seja também feita uma avaliação para a terapia sistémica da função hepática.
- O campo de tratamento do HCC está também a expandir-se nas fases iniciais do BCLC. Se possível, os pacientes devem ser incluídos nos estudos.
Literatura:
- Fulgenzi CAM, et al; Imunoterapia no Carcinoma Hepatocelular. Opções de Tratamento de Moeda Oncol 2021, 22(10): 87.
- Galati G, et al.: Current Treatment Options for HCC: From Pharmacokinetics to Efficacy and Adverse Events in Liver Cirrhosis. Curr Drug Metab 2020, 21(11): 866-884.
- Llovet JM, et al: Locoregional therapies in the era of molecular and immune treatments for hepatocellular carcinoma. Nat Rev Gastroenterol Hepatol 2021, 18(5): 293-313.
- Llovet JM, et al: Sorafenib em carcinoma hepatocelular avançado. N Engl J Med 2008, 359(4): 378-390.
- Bruix J, et al: Regorafenib para doentes com carcinoma hepatocelular que progrediram no tratamento com sorafenibe (RESORCE): um ensaio aleatório, duplo-cego, controlado por placebo, fase 3. Lancet 2017, 389(10064): 56-66.
- Casak SJ, et al: FDA Approval Summary: Atezolizumab Plus Bevacizumab for the Treatment of Patients with Advanced Unresectable or Metastatic Hepatocellular Carcinoma. Clin Cancer Res 2021. 27(7): 1836-1841.
- Finn RS, et al: Atezolizumab mais Bevacizumab em Carcinoma Hepatocelular Inesecável. N Engl J Med 2020, 382(20): 1894-1905.
- Finn R, QS, Ikeda M, et al.: IMbrave150: dados de sobrevivência global actualizados a partir de um estudo global, randomizado e aberto fase III de atezolizumab + bevacizumab vs sorafenib em doentes com carcinoma hepatocelular inconectável. Journal of Clinical Oncology 39, no. 3_suppl (20 de Janeiro de 2021) 267-267, 2021.
- Gordan JD, et al: Systemic Therapy for Advanced Hepatocellular Carcinoma: ASCO Guideline. J Clin Oncol 2020, 38(36): 4317-4345.
- Kelley RK, et al: VP10-2021: Cabozantinib (C) mais atezolizumab (A) versus sorafenib (S) como tratamento sistémico de primeira linha para o carcinoma hepatocelular avançado (aHCC): Resultados do ensaio aleatório da fase III COSMIC-312. Annals of Oncology 2021 ESMO VIRTUAL PLENARY ABSTRACT VOLUME 33, ISSUE 1, P114-116.
- Ren Z, et al: Sintilimab mais um bevacizumab biosimilar (IBI305) versus sorafenibe em carcinoma hepatocelular incontestável (ORIENT-32): um estudo aleatório, de rótulo aberto, fase 2-3. Lancet Oncol 2021, 22(7): 977-990.
InFo ONcOLOGIA & HaEMATOLOGIA 2022; 10(2): 6-8











