Les patients atteints de dermatite atopique modérée à sévère souffrent des effets physiques et psychologiques de la maladie et ne reçoivent pourtant pas, ou souvent avec retard, un traitement adéquat par des thérapies systémiques [1-3]. L’approche de l’activité minimale de la maladie vise à identifier de manière cohérente les patients susceptibles de bénéficier d’un traitement avancé, en combinant le concept de traitement à la cible et la prise de décision conjointe entre les patients et les médecins [4].
La dermatite atopique (DA) se caractérise par des lésions cutanées eczémateuses accompagnées de démangeaisons intenses et présente une grande hétérogénéité en termes de caractéristiques cliniques et de sévérité [5]. Au quotidien, la maladie représente souvent une charge physique et psychologique qui limite la qualité de vie (QOL) des personnes atteintes [1]. Pour les patients atteints de DA modérée à sévère réfractaire aux traitements topiques, il existe des thérapies systémiques ciblées qui peuvent réduire les poussées et atténuer les effets psychosociaux tels que l’anxiété, la dépression et l’absentéisme au travail [6-8]. Cependant, seule une minorité (7-8%) des patients atteints de DA modérée à sévère reçoivent un traitement systémique [2, 3]. Un retard dans le traitement peut avoir un impact négatif sur l’évolution de la maladie, tandis que le recours précoce à des options thérapeutiques systémiques efficaces permet de prévenir les effets à vie d’une maladie inflammatoire cutanée non contrôlée [9-12].
Consensus pour une approche Treat-to-Target de la MA
Avec la participation des dermatologues suisses, le professeur Peter Schmid-Grendelmeier de l’Hôpital universitaire de Zurich et le professeur Peter Häusermann du cabinet Dermatologie am Rhein de Bâle, dans un programme global, le concept de Activité minimale de la maladie (MDA) avec 100% d’approbation pour AD et maintenant pour la première fois au Congrès mondial de dermatologie 2023 à Singapour lors d’un symposium. La MDA est une nouvelle approche de traitement à la cible permettant d’identifier les patients atteints de MA modérée à sévère qui peuvent bénéficier d’un traitement systémique [4]. La MDA est définie comme un niveau d’activité de la maladie qui, compte tenu des options thérapeutiques disponibles, est considéré par les patients et les médecins traitants comme un objectif thérapeutique raisonnable [13]. Cela peut optimiser les résultats du traitement à long terme et aider les médecins à choisir les options thérapeutiques [14, 15].

Le concept MDA en pratique
Dans la pratique, les critères MDA impliquent une combinaison d’au moins un critère clinique et uncritère de patient. résultat rapportépar le patient (patient-reported) et les destinations sélectionnées sont listées par ordre de priorité (Fig. 1). Dans les deux catégories, il existe des objectifs modérés qui doivent être atteints dans les 3 mois et qui, s’ils ne sont pas atteints, conduisent à la modification ou à l’escalade du traitement. Les objectifs optimaux doivent être atteints à long terme (à partir de 6 mois) et sont considérés comme des MDA. L’approche MDA combine l’approche Treat-to-Target avec une prise de décision partagée entre les médecins et les patients [4].
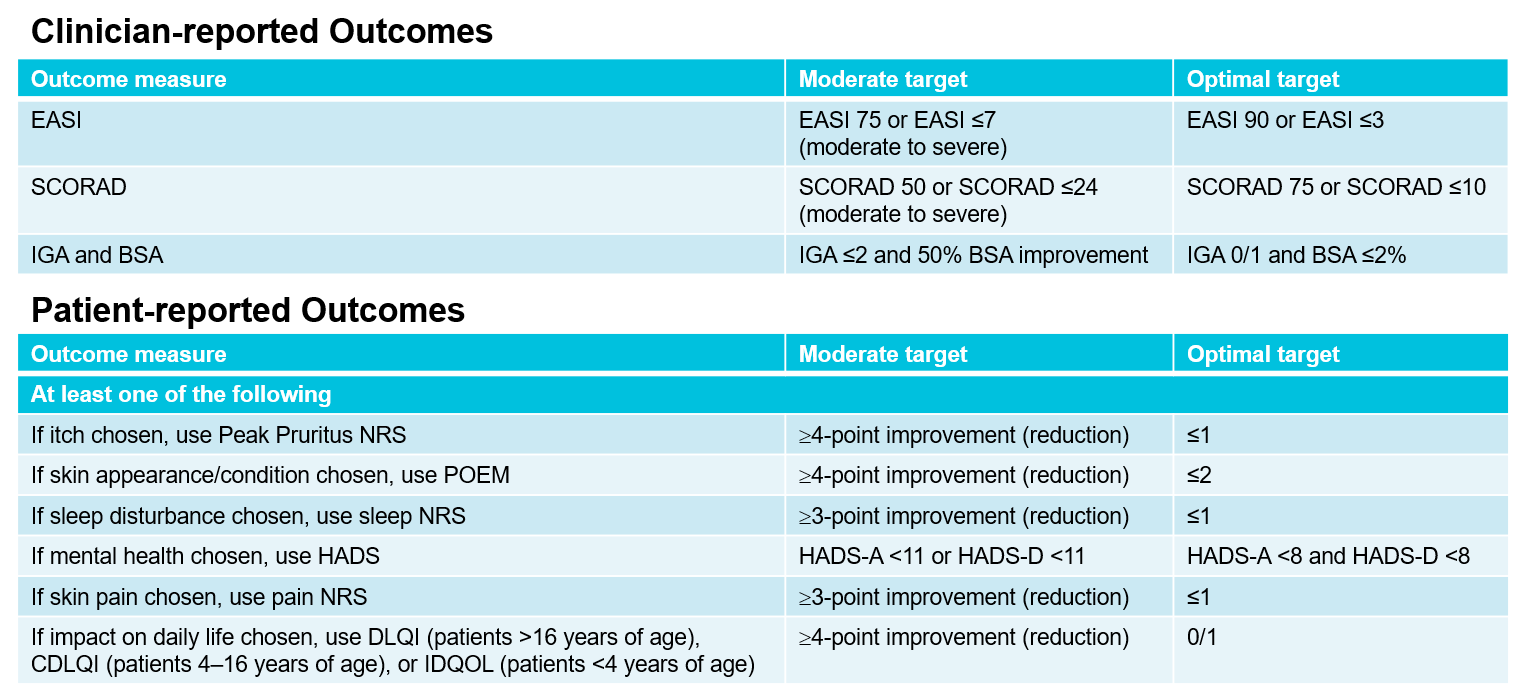
Fig. 1: Critères pour l’approche MDA qui combine les résultatscliniques et les résultats rapportés par les patients. EASI, Eczema Area and Severity Index ; SCORAD, SCORing Atopic Dermatitis ; IGA, Investigator Global Assessment ; BSA, Body Surface Area ; NRS, Numerical Rating Scale ; POEM, Patient Oriented Eczema Measure ; HADS, Hospital Anxiety and Depression Scale ; (C)DQOL, (Children’s) Dermatitis Quality of Life Index. Adapté de [4].
Atteindre les objectifs thérapeutiques
Pour les patients, les principaux objectifs thérapeutiques sont le soulagement des démangeaisons, l’amélioration des symptômes et la guérison complète de la peau. L’obtention de ces résultats rapportés par les patients est également directement liée à l’amélioration de la QVT [1]. Ces objectifs thérapeutiques sont désormais réalisables grâce aux options thérapeutiques avancées dans la MA. Par exemple, l’upadacitinib (RINVOQ®), un inhibiteur oral de JAK* qui inhibe sélectivement JAK-1, a permis d’obtenir une réponse EASI* 75 chez 82,0 % des patients et une réponse EASI 90 chez 62,7 % des patients dans les études pivots de phase III, randomisées, en double aveugle et contrôlées par placebo, MEASURE Up-1 et MEASURE Up-2, à la dose de 15 mg une fois par jour, après 52 semaines. [16]. En outre, une réponse rapide au RINVOQ® a été observée – après seulement deux jours, un nombre significativement plus élevé de patients ont signalé un soulagement significatif des démangeaisons par rapport aux patients sous placebo [17]. RINVOQ® est indiqué à la dose orale de 15 mg une fois par jour depuis novembre 2021 pour le traitement des adultes atteints de la MA modérée à sévère lorsqu’un traitement par des médicaments topiques conventionnels ne permet pas un contrôle adéquat de la maladie ou n’a pas pu être utilisé [18].
Conclusion
Pour atteindre des objectifs thérapeutiques élevés, il existe des thérapies systémiques appropriées pour la MA modérée à sévère [18-23]. Pour que les patients éligibles au traitement systémique puissent en bénéficier, la MDA peut être utilisée. Elle combine l’approche Treat-to-Target et la prise de décision partagée.
* JAK, Janus kinase ; EASI, Eczema Area and Severity Index
Information technique succincte RINVOQ
Littérature
1. Augustin, M., et al, Characterizing treatment-related patient needs in atopic eczema : insights for personalized goal orientation. J Eur Acad Dermatol Venereol, 2020. 34(1) : p. 142-152.
2 Pascal, C., et al, Prise en charge thérapeutique des adultes atteints de dermatite atopique : comparaison avec le psoriasis et l’urticaire chronique. J Eur Acad Dermatol Venereol, 2020. 34(10) : p. 2339-2345.
3. Egeberg, A. et J.P. Thyssen, Factors associated with patient-reported importance of skin clearance among adults with psoriasis and atopic dermatitis. J Am Acad Dermatol, 2019. 81(4) : p. 943-949.
4. Silverberg J, et al. Revolutionizing Atopic Dermatitis (RAD), Virtual Conference, 11 décembre 2022. Poster.
5. Langan, S.M., A.D. Irvine, and S. Weidinger, Atopic dermatitis. Lancet, 2020. 396(10247) : p. 345-360.
6. Song, A., S.E. Lee, and J.H. Kim, Immunopathology and Immunotherapy of Inflammatory Skin Diseases. Immune Netw, 2022. 22(1) : p. e7.
7. Silvestre JF et al. Real-World Burden in Patients With Atopic Dermatitis Who Are Candidates for Systemic Therapy and Currently Receiving No Systemic Therapy, No Treatment, Topical Therapy Alone, or Systemic Therapy : Results From a Real-World Multicountry Study. EADV, Milan, 7-11 septembre 2022. Session orale FC02.02.
8. Megna, M., et al, Systemic Treatment of Adult Atopic Dermatitis : A Review. Dermatol Ther (Heidelb), 2017. 7(1) : p. 1-23.
9. Marzano, A.V., et al., Evidence for a ‘window of opportunity’ in hidradenitis suppurativa treated with adalimumab : a retrospective, real-life multicentre cohort study. Br J Dermatol, 2021. 184(1) : p. 133-140.
10. Kimball, A.B., et al, Psoriasis : l’impact sur la vie d’un patient est-il cumulatif ? J Eur Acad Dermatol Venereol, 2010. 24(9) : p. 989-1004.
11. Linder, M.D., et al., Psoriasis – The Life Course Approach. Acta Derm Venereol, 2016. 96(217) : p. 102-8.
12. Ros, S., L. Puig, et J.M. Carrascosa, Impact cumulé sur le cours de la vie : l’empreinte du psoriasis sur la vie du patient. Actas Dermosifiliogr, 2014. 105(2) : p. 128-34.
13 Wells, G.A., et al, Activité pathologique minimale pour l’arthrite rhumatoïde : une définition préliminaire. J Rheumatol, 2005.32(10) : p. 2016-24.
14 De Bruin-Weller, M., et al, Treat-to-Target in Atopic Dermatitis : An International Consensus on a Set of Core Decision Points for Systemic Therapies. Acta Derm Venereol, 2021. 101(2) : p. adv00402.
15. Vestergaard, C., A. Wollenberg, et J.P. Thyssen, European Task Force on Atopic Dermatitis (ETFAD) Position Paper : treatment of parental atopic dermatitis during preconception, pregnancy and lactation period. J Eur Acad Dermatol Venereol, 2020. 34(2) : p. 426-427.
16. Simpson, E.L., et al, Efficacité et sécurité de l’upadacitinib chez les patients atteints de dermatite atopique modérée à sévère : analyse des données de suivi issues des essais cliniques randomisés Measure Up 1 et Measure Up 2. JAMA Dermatology, 2022. 158(4) : p. 404-413.
17. Guttman-Yassky, E., et al., Once-daily upadacitinib versus placebo in adolescents and adults with moderate-to-severe atopic dermatitis (Measure Up 1 and Measure Up 2) : results from two replicate double-blind, randomised controlled phase 3 trials. Lancet, 2021. 397(10290) : p. 2151-2168.
18. information professionnelle actuelle RINVOQ® (upadacitinib) sur www.swissmedicinfo.ch
19. information professionnelle actuelle Sandimmun Neoral® (cyclosporine A) sur www.swissmedicinfo.ch.
20. information professionnelle actuelle DUPIXENT® (dupilumab) sur www.swissmedicinfo.ch.
21. information professionnelle actuelle OLUMIANT® (baricitinib) sur www.swissmedicinfo.ch.
22. information professionnelle actuelle ADTRALZA® (tralokinumab) sur www.swissmedicinfo.ch.
23. information professionnelle actuelle CIBINQO® (abrocitinib) sur www.swissmedicinfo.ch.
Les références peuvent être demandées par les professionnels à medinfo.ch@abbvie.com.
Cet article a été rédigé avec le soutien financier de AbbVie AG, Alte Steinhauserstrasse 14, Cham.
CH-RNQD-230040_11/2023
Cet article a été publié en allemand.
Contribution en ligne depuis le 15/09/2023
Contribution mise à jour : 17/11/2023












