Fino a quando non sarà disponibile la terapia modificante la malattia (DMT) individualmente appropriata, esistono
In assenza di biomarcatori predittivi, spesso sono necessarie ottimizzazioni graduali, che possono comportare modifiche multiple della DMT. Per ridurre il rischio di effetti di rimbalzo, è necessario stabilire una strategia di follow-up del trattamento come misura precauzionale prima dell’interruzione.
L’eterogeneità della sclerosi multipla (SM) e la disponibilità di diverse terapie modificanti la malattia (DMT) rappresentano una sfida nella selezione della terapia. L’obiettivo è selezionare il trattamento che meglio risponde alle esigenze individuali del paziente, tenendo conto dell’efficacia e di un rapporto rischio-beneficio accettabile [1].

I cambiamenti di terapia sono comuni
I motivi per cambiare un DMT possono includere la mancanza di efficacia, gli eventi avversi e l’insufficiente aderenza al trattamento. Uno studio italiano multicentrico e retrospettivo ha analizzato i dati di 2954 pazienti con nuova diagnosi di sclerosi multipla recidivante-remittente (SMRR) tra il 2010 e il 2017 [2,3]. È stato riscontrato che il 48% dei pazienti ha cambiato terapia entro 3 anni [2,3]. Circa un decimo dei pazienti che interrompono il trattamento con fingolimod a causa di effetti collaterali o di un controllo inadeguato dell’attività della malattia, sperimenta un aumento dell’attività della malattia (il cosiddetto rebound) da due a quattro mesi dopo l’interruzione [4]. Pertanto, come misura precauzionale, è necessario determinare una strategia per il trattamento di follow-up prima dell’interruzione. Fingolimod è stato approvato in Svizzera dal 2011 per il trattamento dei pazienti con SMRR per ridurre la frequenza delle ricadute e ritardare la progressione della disabilità. Il modulatore del recettore della sfingosina-1-fosfato (S1PR) trattiene selettivamente e reversibilmente i linfociti nei linfonodi, consentendo di mantenere importanti funzioni immunitarie e di trattare i pazienti in modo flessibile.
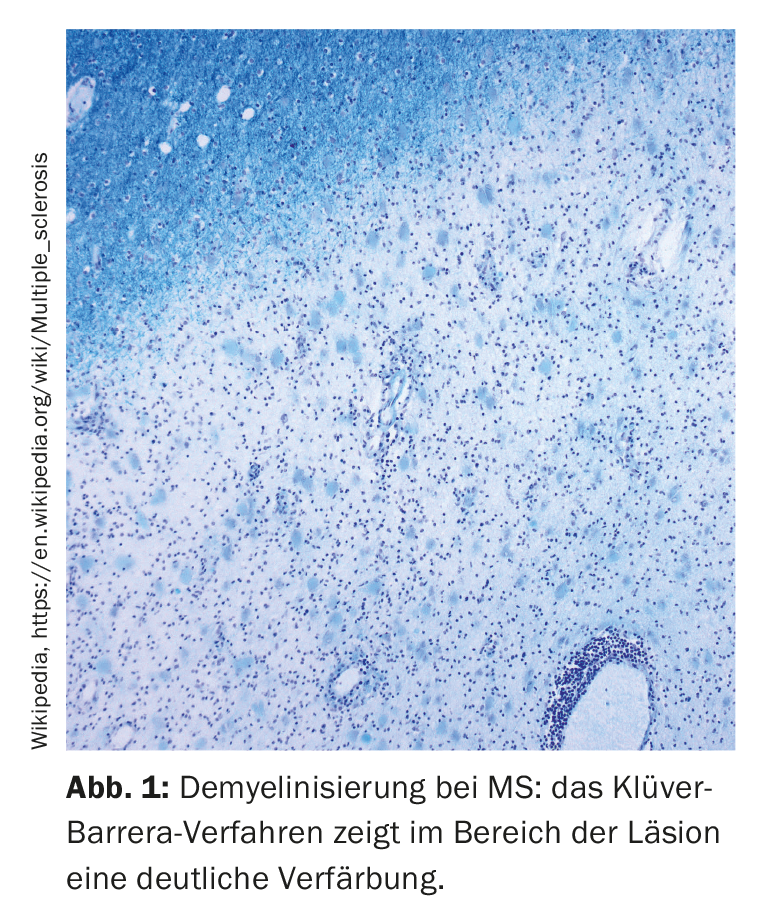
Studio sul passaggio da fingolimod a ocrelizumab o natalizumab
Uno studio recente nel Giornale di Neurologia, Neurochirurgia e Psichiatria Uno studio pubblicato, condotto dai ricercatori della Monash University, ha rilevato che il numero di ricadute nei pazienti con SMRR era ben controllato e la disabilità si stabilizzava o migliorava quando i pazienti che avevano interrotto il fingolimod passavano a ocrelizumab o natalizumab [5]. Il primo autore e biostatistico, il dottor Chao Zhu, ha utilizzato un approccio statistico sofisticato nell’analisi dei dati. In sintesi, ocrelizumab ha ottenuto la migliore performance nel ridurre il tasso annualizzato di ricadute, seguito da natalizumab e cladribina. Il natalizumab ha portato al maggior miglioramento della disabilità e i pazienti sono rimasti in terapia con ocrelizumab più a lungo. I risultati in sintesi:
- Un totale di 1.045 pazienti è passato da fingolimod a ocrelizumab (n=445), cladribina (n=76) o natalizumab (n=524).
- Il tasso di ricaduta annualizzato (ARR) per ocrelizumab è stato di 0,07, per natalizumab 0,11 e per cladribina 0,25.
- Rispetto a natalizumab, il rapporto ARR (intervallo di confidenza al 95% era [KI]) per ocrelizumab era 0,67 (0,47-0,96) e per cladribina era 2,31 (1,30-4,10); l’hazard ratio (95% CI) per il tempo alla prima ricaduta era 0,57 (0,40-0,83) per ocrelizumab e 1,18 (0,47-2,93) per cladribina.
- Gli utilizzatori di Ocrelizumab avevano un tasso di abbandono inferiore dell’89% (95% CI: 0,07-0,20) rispetto a natalizumab, ma anche una probabilità inferiore del 51% di miglioramento confermato della disabilità (95% CI: 0,32-0,73).
- Non c’è stata alcuna differenza nell’accumulo di perdite.
Il natalizumab è un anticorpo monoclonale IgG4 umanizzato che impedisce la migrazione dei leucociti nei tessuti infiammatori legandosi alla subunità α4 delle integrine umane [6]. Ocrelizumab è un anticorpo monoclonale ricombinante e umanizzato che elimina selettivamente le cellule B CD20-positive [7].
Letteratura:
- Grand’Maison F, et al: Sequenziamento delle terapie modificanti la malattia per la sclerosi multipla recidivante-remittente: un approccio teorico per ottimizzare il trattamento. Curr Med Res Opin 2018; 34(8): 1419-1430.
- Saccà F, et al: Determinanti del cambio di terapia nei pazienti della sclerosi multipla che non sono in trattamento: uno studio di vita reale. Mult Scler 2019; 25(9): 1263-1272.
- Wiendl H, et al; il Gruppo di consenso sulla terapia della sclerosi multipla (MSTKG): Position paper on course-modifying therapy for multiple sclerosis 2021 (libro bianco) Nervenarzt 2021; 92(8): 773-801.
- Rete di competenza sulla sclerosi multipla, Informazioni per i pazienti sul trattamento con Gilenya®, www.kompetenznetz-multiplesklerose.de, (ultimo accesso 12.12.2022)
- Zhu C, et al; Gruppo di studio MSBase: Confronto tra il passaggio a ocrelizumab, cladribina o natalizumab dopo la cessazione del trattamento con fingolimod nella sclerosi multipla. J Neurol Neurosurg Psychiatry 2022; 93(12): 1330-1337.
- Delbue S, Comar M, Ferrante P: Trattamento con Natalizumab della sclerosi multipla: nuove intuizioni. Immunoterapia 2017; 9: 157-171.
- Hoffmann O, Gold R: Terapia modificante la malattia nella sclerosi multipla secondaria progressiva. Neurologist 2021; 92(10): 1052-1060.
PRATICA GP 2023; 18(1): 38











