Le opzioni di trattamento per i pazienti con diabete e malattia renale cronica (CKD) sono migliorate in modo significativo grazie alle nuove opzioni terapeutiche delle classi di farmaci SGLT-2-i, GLP-1-RA e MRA. Le nuove linee guida pubblicate lo scorso anno dalla KDIGO (Kidney Disease: Improving Global Outcomes) mirano a fornire una guida pratica da utilizzare nella pratica clinica quotidiana. Come superare gli ostacoli all’attuazione di queste raccomandazioni è stato discusso al congresso di quest’anno dell’Associazione Renale Europea (ERA).
I diabetici di tipo 2 costituiscono una grande percentuale della popolazione di pazienti con CKD – fino al 40% ha una malattia renale cronica (CKD ) [3]. Questo non solo è prognosticamente sfavorevole per quanto riguarda le complicanze microvascolari, ma è anche associato a un aumento del rischio di eventi cardiovascolari**. Poiché gli studi randomizzati e controllati hanno dimostrato che l’assistenza multifattoriale migliora la prognosi, la linea guida KDIGO suggerisce una strategia su più fronti che affronta diversi livelli [1,4–7]. Nell’ultima versione delle linee guida KDIGO, sono state aggiunte le prove di efficacia sugli inibitori del cotrasportatore sodio-glucosio-2 (SGLT-2-i) e sugli agonisti del recettore del peptide glucagone-1 (GLP-1-RA) rispetto alla versione precedente, ed è stata aggiunta una nuova sezione sugli antagonisti dei mineralocorticoidi (MRA) (riquadro) [1]. Se questi farmaci, oggi disponibili, vengono utilizzati in tempo, si può ottenere un rallentamento significativo della perdita della funzione renale e migliorare la prognosi complessiva, ha spiegato il Dr. Frederik Persson, MD, Senior Research presso lo Steno Diabetes Center di Copenhagen (Danimarca) [2]. Come nelle precedenti linee guida, le raccomandazioni non si limitano alle misure mediche, ma i fattori legati allo stile di vita e all’autogestione sono ancora una volta propagandati come componenti importanti della gestione multimodale della malattia.
** ad esempio infarto del miocardio, aritmia cardiaca o insufficienza cardiaca
| T2D e CKD: raccomandazioni chiave delle Linee Guida KDIGO 2022 |
| In quali condizioni un SGLT-2-i è consigliato come add-on? In termini di controllo glicemico, la metformina è ancora considerata una terapia di prima linea nel diabete di tipo 2 (T2D) quando la velocità di filtrazione glomerulare stimata (eGFR) è ≥30 ml/min per 1,73 m2 ma si raccomanda l’aggiunta precoce di un SGLT-2-i: con un’eGFR di ≥20 ml/min per 1,73 m2 Il SGLT-2-i può essere iniziato e, a seconda della tollerabilità, continuato fino all’inizio della dialisi o del trapianto. Nella versione precedente della linea guida, la soglia di eGFR era ancora di 30 ml/min per 1,73m2. |
| Qual è la situazione del GLP-1 RA? Quando SGLT2-i e metformina non sono sufficienti per raggiungere gli obiettivi di glucosio nel sangue, o quando SGLT2-i o metformina non possono essere utilizzati, GLP-1 RA è il farmaco preferito per abbassare la glicemia. |
| Quando dovrebbe essere prescritta una MRA? Un MRA non steroideo selettivo (finerenone) può essere aggiunto alla terapia di prima linea per la T2D e un elevato rischio residuo di progressione della malattia renale e di eventi cardiovascolari. In particolare, con un eGFR ≥25 ml/min per 1,73m2, concentrazione sierica di potassio normale e albuminuria (≥30 mg/g [≥3 mg/mmol]) nonostante il dosaggio massimo tollerato di un inibitore del RAS (l’inibizione del RAS è raccomandata per i pazienti con albuminuria e ipertensione). |
| Cosa dice la linea guida sulla terapia con statine? Si raccomanda di prendere in considerazione la prescrizione di una statina in tutti i pazienti con T2D e CKD. |
| a [1,2] |
Eseguire lo screening dei pazienti con T2D per la CKD
A differenza del cancro, non esistono programmi di screening strutturati per le malattie metaboliche croniche come il diabete, ha sottolineato il dottor Persson [2]. Tuttavia, considerando che il diabete è la causa più comune di malattia renale cronica (CKD), è consigliabile valutare regolarmente i fattori di rischio per lo sviluppo della nefropatia nei diabetici di tipo 2 che ricevono assistenza primaria, ha detto il relatore [2]. La linea guida KDIGO consiglia di determinare l’eGFR e il rapporto albumina-creatinina (ACR) a intervalli regolari, come prerequisito per l’attuazione delle raccomandazioni terapeutiche [8]. L’albuminuria è un parametro molto sensibile per la diagnosi di insufficienza renale cronica [9].
Il relatore ha riferito che un approccio olistico alla cura del diabete e l’importanza dello screening dei pazienti a rischio di CKD, propagandato nelle linee guida, sta dando i suoi frutti, come dimostra l’esempio di uno studio condotto in Danimarca, dove gli sforzi corrispondenti sono stati intensificati negli ultimi anni [2]. I ricercatori hanno analizzato un’ampia serie di dati provenienti da tre studi trasversali su diabetici di tipo 2 (n=5592) condotti tra il 2009 e il 2017. Questo ha rilevato che il tasso di misurazione annuale ACR nel contesto dell’assistenza medica generale è aumentato dal 57,2% all’82,8% nel periodo 2012-2020 [10]. Poiché la CKD spesso non è quasi accompagnata da sintomi nelle fasi iniziali, questi screening sono un elemento estremamente importante nella gestione della malattia.
Assistenza multidisciplinare integrata
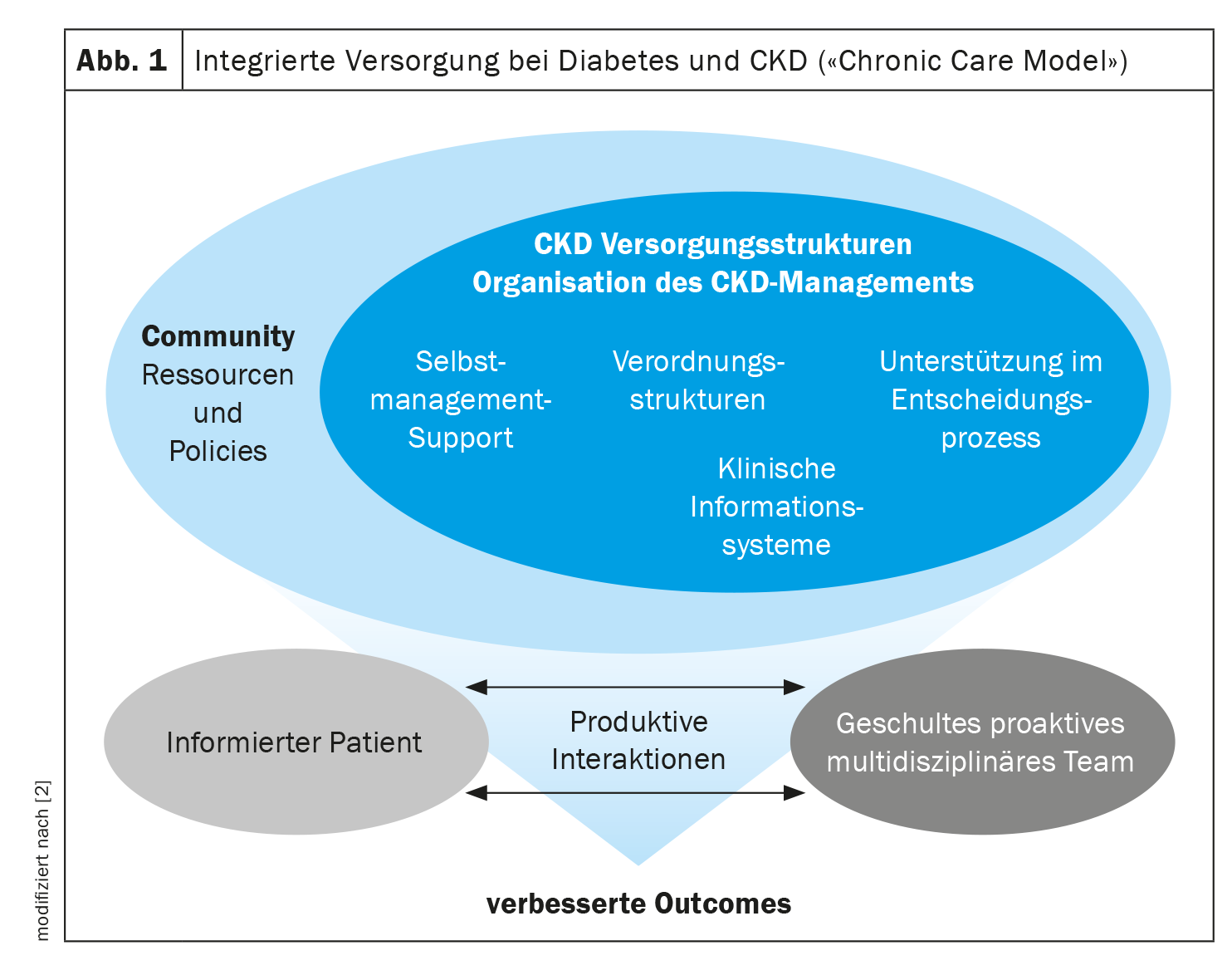
Per identificare la CKD in una fase precoce e per attuare le raccomandazioni delle linee guida KDIGO, è necessaria la collaborazione tra diversi attori del sistema sanitario, ha sottolineato il dottor Persson [2]. Gli ostacoli al successo dell’implementazione delle raccomandazioni della linea guida possono essere collocati a diversi livelli. Il relatore ha sottolineato che è importante riflettere su modi di pensare superati e creare prove che le nuove opzioni terapeutiche siano significative e sostenibili. Questo può anche togliere il vento alle vele dell’argomento dei costi elevati dei farmaci. Perché da un punto di vista economico-sanitario, il ritardo delle procedure di sostituzione renale ad alto costo attraverso l’avvio tempestivo delle moderne farmacoterapie è un investimento sostenibile, secondo una dichiarazione delle attuali linee guida KDIGO [1]. Tuttavia, l’implementazione della strategia terapeutica ottimale può anche incontrare ostacoli a livello del singolo paziente. Qui entrano in campo soprattutto i fattori motivazionali. Per esempio, ci sono pazienti che non capiscono perché devono assumere un altro farmaco [2]. In questo caso è necessario educare, mostrando i benefici basati sull’evidenza del rispettivo regime terapeutico. Inoltre, il dottor Persson ha sottolineato l’importanza della cooperazione interdisciplinare e ha fornito esempi di sistemi di assistenza integrata implementati con successo (Fig. 1) in Danimarca, Svezia e Regno Unito [2]. In ogni caso, si è trattato di un approccio incentrato sul paziente che ha portato a un’elevata soddisfazione dei pazienti. Un team multidisciplinare proattivo è un prerequisito importante, ha detto il relatore e ha fornito un esempio dalla routine clinica del Centro diabetico di Steno: lì, sono state fatte buone esperienze con il fatto che ad ogni secondo appuntamento con il paziente, la visita del medico di base era alternativamente abbinata ad una consultazione con il nefrologo o l’endocrinologo. Questo non solo facilita la migliore assistenza al paziente, ma promuove anche lo scambio interdisciplinare di conoscenze.
Congresso: Congresso ERA
Letteratura:
- Rossing P, et al.: Executive summary of the KDIGO 2022 Clinical Practice Guideline for Diabetes Management in Chronic Kidney Disease: an update based on rapidly emerging new evidence. Kidney Int 2022; 102(5): 990–999.
- «Implementation of the KDIGO Diabetes Guideline for the European context», Dr. Frederik Persson, MD, Annual Congress of the European Renal Association Congress (ERA), 18.06.2023.
- Seidu S, et al.: 2022 update to the position statement by Primary Care Diabetes Europe: a disease state approach to the pharmacological management of type 2 diabetes in primary care. Prim Care Diabetes 2022; 16(2): 223–244.
- Chan JC, et al.: Effects of structured versus usual care on renal endpoint in type 2 diabetes: the SURE study: a randomized multicenter translational study. Diabetes Care 2009; 32: 977–982.
- Chan JCN, et al.: Effect of a web-based management guide on risk factors in patients with type 2 diabetes and diabetic kidney disease: a JADE randomized clinical trial. JAMA Netw Open 2022; 5: e223862.
- Gaede P, et al.: Intensified multifactorial intervention in patients with type 2 diabetes mellitus and microalbuminuria: the Steno type 2 randomised study. Lancet 1999; 353: 617–622.
- Ueki K, et al.: Effect of an intensified multifactorial intervention on cardiovascular outcomes and mortality in type 2 diabetes (J-DOIT3): an open-label, randomised controlled trial. Lancet Diabetes Endocrinol 2017; 5: 951–964.
- de Boer IH, et al.: Diabetes management in chronic kidney disease: a consensus report by the American Diabetes Association (ADA) and Kidney Disease: Improving Global Outcomes (KDIGO). Diabetes Care. Published online October 3, 2022. https://doi.org/10.2337/dci22-0027, (ultimo accesso 31.08.2023).
- Medix, www.medix.ch/wissen/guidelines/chronische-niereninsuffizienz,(ultimo accesso 31.08.2023)
- Persson F, et al.: Improving frequency of urinary albumin testing in type 2 diabetes in primary care – An analysis of cross-sectional studies in Denmark. Prim Care Diabetes 2021; 15(6): 1007–1011.
HAUSARZT PRAXIS 2023; 18(9): 43–44