- Il trattamento a lungo termine con upadacitinib (UPA, RINVOQ®) fino a 5,5 anni non mostra nuovi segnali di sicurezza [1].
- L’UPA ha un profilo di sicurezza coerente nel trattamento della dermatite atopica (AD), dell’artrite reumatoide (AR), dell’artrite psoriasica (PsA) e della spondiloartrite assiale (AS), anche se l’incidenza degli eventi avversi varia a causa delle differenze nella popolazione di pazienti e delle comorbidità correlate alla malattia[1].
UPA nella dermatite atopica
La dermatite atopica (AD) è la malattia infiammatoria cronica della pelle più comune in tutto il mondo e rappresenta un onere considerevole per la vita dei pazienti e delle loro famiglie [2]. Inoltre, l’AD è associato a varie comorbidità allergiche, autoimmuni e cardiovascolari [3]. Per i pazienti con MA da moderata a grave che sono refrattari al trattamento topico, esistono terapie sistemiche mirate che riducono le ricadute e attenuano anche gli effetti psicologici della malattia [1, 4-6]. L’UPA è un inibitore orale e reversibile della Janus chinasi (JAK) che agisce specificamente sulla JAK1 e, in misura minore, anche sulla JAK2, JAK3 o TYK2. L’UPA è utilizzato al dosaggio di 15 mg una volta al giorno per il trattamento di AD, RA, PsA e AS [7].
L’UPA ha dimostrato una forte efficacia in tutti i 12 studi condotti su AD, RA, PsA e AS. Tuttavia, l’uso sicuro è altrettanto fondamentale per il trattamento [7]. I dati dello studio di sorveglianza ORAL, che ha confrontato l’inibitore JAK tofacitinib con un inibitore del fattore di necrosi tumorale (TNF) in pazienti anziani con RA e fattori di rischio cardiovascolare, sottolineano la necessità di caratterizzare meglio il profilo di sicurezza degli inibitori JAK – anche perché la sicurezza dei singoli inibitori JAK differisce nei vari gruppi di pazienti con malattie infiammatorie immuno-mediate (IMID) [1]. Una nuova pubblicazione di Burmester et al. ora mostra il profilo di sicurezza a lungo termine di UPA per un periodo fino a 5,5 anni in varie malattie reumatiche e fino a 2,75 anni nell’AD. Durante questo periodo non sono emersi nuovi segnali di sicurezza [1].
Trattamento a lungo termine con UPA
In totale, la sicurezza dell’UPA è stata studiata in 6000 pazienti con AD, RA, PsA e AS con oltre 15.000 anni-paziente (PY). I dati sulla sicurezza di 12 studi di Fase IIb/III per ciascuna malattia sono stati messi in comune tra tutti gli studi. Tre di questi studi, con un totale di 2693 partecipanti, sono stati condotti in AD. Questo corrisponde a 2035,8 PY.
Tabella 1: Dati demografici di base e caratteristiche della malattia dell’UPA nei pazienti con AD
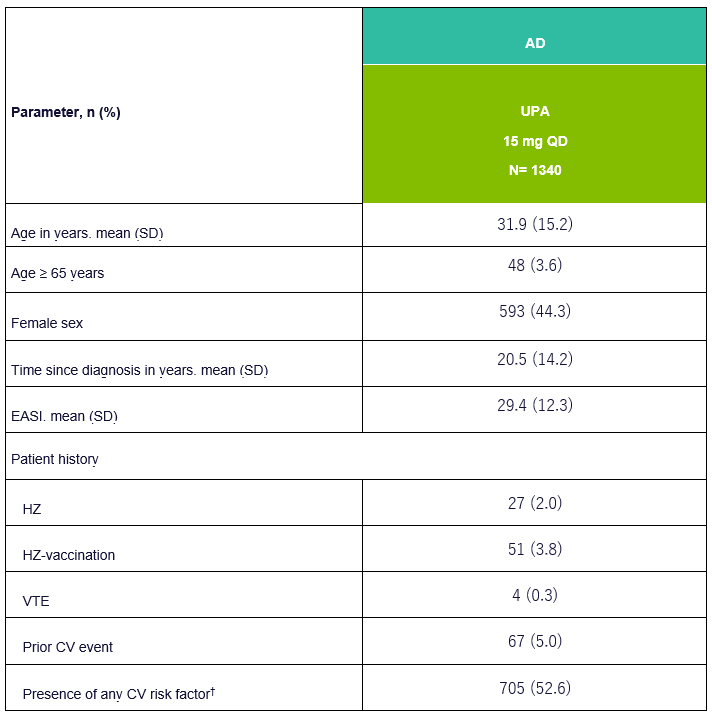
EASI, Eczema Area and Severity Index; VTE, Tromboembolismo Venoso; CV, Cardiovascolare; HZ, Herpes Zoster; †I fattori di rischio CV includono eventi cardiovascolari nell’anamnesi, pressione alta, diabete mellito, consumo di tabacco/nicotina, aumento del valore di LDL-C e diminuzione del valore di HDL-C. Adattato da [1]
Nessun nuovo segnale di sicurezza sotto l’UPA nell’AD
Le infezioni gravi con UPA 15 mg si sono verificate in AD a un tasso di 2,5 eventi per 100 PY (2,5 E/100 PY) e raramente hanno portato all’interruzione del trattamento. L’infezione grave più comune in tutte le popolazioni analizzate è stata la COVID-19, seguita dall’herpes zoster nella popolazione AD. In genere si trattava di disturbi lievi o moderati, senza coinvolgimento del sistema nervoso centrale o degli organi interni, raramente portavano all’interruzione della terapia e di solito interessavano solo un singolo dermatomo. Inoltre, non è stato possibile stabilire una correlazione tra la durata del trattamento e l’insorgenza dell’herpes zoster [1]. È disponibile la vaccinazione contro l’herpes zoster. Il vaccino deve essere somministrato 4 settimane prima del trattamento con un agente immunomodulatore attivo come l’UPA [7]. Altre infezioni opportunistiche con UPA 15 mg sono state elencate come 1,8 eventi per 100 PY, di cui è stato riportato soprattutto l’eczema erpetico. La tubercolosi (TB) è stata registrata separatamente e la TB attiva è stata registrata a 0,03 E/100 PY nei pazienti AD sotto UPA. L’evento avverso più comune legato al trattamento (TEAE) associato all’UPA è stata un’infezione del tratto respiratorio superiore [1].
Gli eventicardiovascolari avversi maggiori (MACE) hanno incluso i seguenti. Morte, infarto miocardico non fatale e apoplessia non fatale. Tu sono stati riportati nei pazienti con AD a un tasso di 0,03/100 PY. Non è stata trovata alcuna correlazione tra la durata dell’assunzione di UPA e il verificarsi di MACE. Inoltre, la maggior parte dei pazienti che hanno subito un MACE aveva almeno un fattore di rischio cardiovascolare [1].
Le trombosi venose profonde e le embolie polmonari sono state registrate come tromboembolie venose (VTE ). Si sono verificati a un tasso di 0,04 E/100 PY, con la maggior parte dei pazienti che avevano almeno un fattore di rischio cardiovascolare e/o tromboembolico. Non è stata trovata alcuna correlazione tra la durata dell’esposizione all’UPA e l’insorgenza di TEV [1].
Le malattie maligne (escluso il cancro della pelle non melanoma, NMSC) sono state registrate sotto UPA 15 mg a 0,2 E/100 PY. Non c’è stato alcun cambiamento significativo in questo tasso durante l’intera durata dell’assunzione di UPA. Gli eventi NMSC non sono stati generalmente gravi e non hanno portato all’interruzione del trattamento. I NMSC sono stati riportati nella popolazione UPA 15 mg a 0,3 E/100 PY [1].
Anomalie di laboratorio
Nei pazienti affetti da AD che assumono UPA sono stati segnalati anche effetti collaterali dose-dipendenti come anemia, neutropenia, linfopenia, disfunzione epatica ed elevazione della creatina fosfochinasi (CPK). La maggior parte delle anomalie di laboratorio sono state classificate come complessivamente lievi e transitorie e solo alcune hanno portato all’interruzione del farmaco in studio [1].
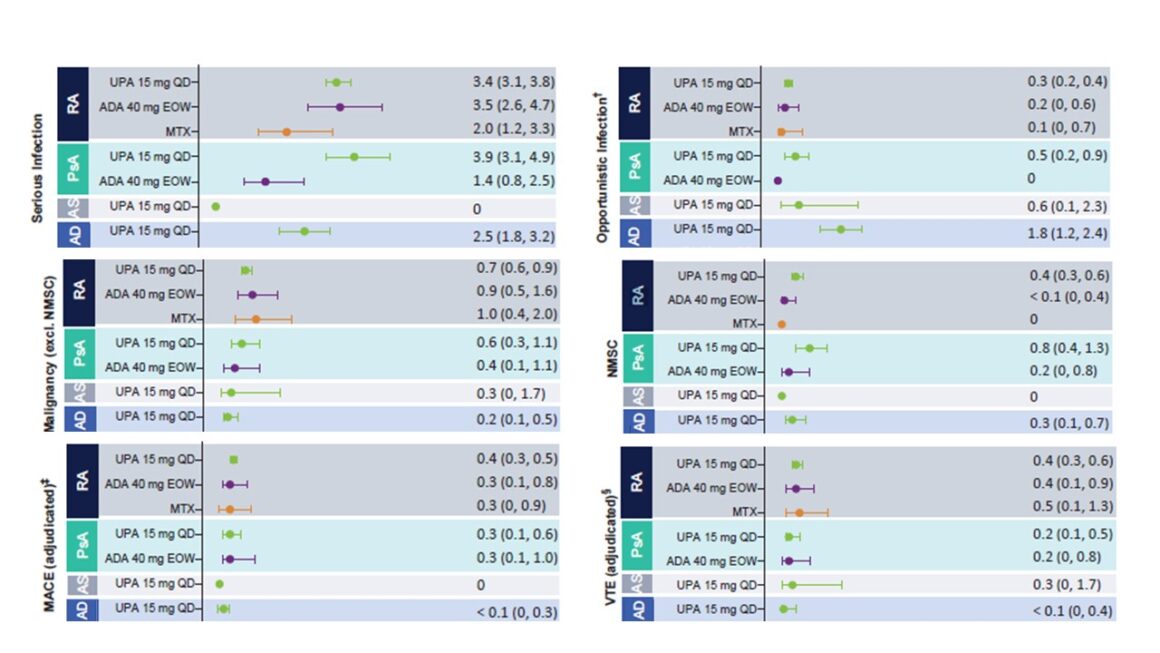
Figura 1: Tassi aggiustati per l’esposizione di eventi avversi al trattamento (TEAEs) di particolare interesse. Adattato da [1]
Questa analisi di sicurezza non mostra rischi di sicurezza nuovi o inaspettati con l’UPA rispetto ai rapporti precedenti. L’aumento del rischio di herpes zoster e l’aumento dei livelli di CPK sono associati all’inibizione di JAK e sono coerenti con il profilo di sicurezza generale degli inibitori di JAK. Le infezioni da Herpes zoster erano per lo più non gravi e limitate a un dermatomo, mentre i livelli elevati di CPK erano per lo più asintomatici e transitori. Sebbene siano stati segnalati eventi di TEV nei pazienti che ricevevano UPA, i tassi erano coerenti con i tassi di fondo per le singole condizioni. [1].
Conclusione
In sintesi, l’UPA è stato generalmente ben tollerato. Il profilo di sicurezza è paragonabile per AD, RA, PsA e AS, anche se l’incidenza degli eventi avversi varia a causa delle differenze nella popolazione di pazienti e delle comorbidità legate alla malattia. Anche con un trattamento a lungo termine con UPA fino a 5,5 anni o 2,75 anni nell’AD, non sono stati rilevati nuovi segnali di sicurezza.
La pubblicazione completa di Burmester et al. è disponibile qui.
JAK, Janus Chinasi; TYK, Tirosina Chinasi; IMIDs, Malattie Infiammatorie Immuno-Mediate; EASI, Indice di Area e Severità dell’Eczema; HZ, Herpes Zoster; MACE, Evento Cardiovascolare Avverso Maggiore; NMSC, Tumore Cutaneo Non-Melanoma; UPA, Upadacitinib; VTE, Tromboembolismo venoso; TEAE, Eventi avversi emergenti dal trattamento; LDL-C, Lipoproteina colesterolo a bassa densità; HDL-C, Lipoproteina colesterolo ad alta densità; CPK, Creatina fosfochinasi.
Riferimenti:
1. Burmester, G.R., et al, Profilo di sicurezza di upadacitinib su 15.000 anni-paziente tra artrite reumatoide, artrite psoriasica, spondilite anchilosante e dermatite atopica. RMD Open, 2023. 9(1).
2 Ali, F., J. Vyas e A.Y. Finlay, Contare il peso: Dermatite atopica e qualità della vita correlata alla salute. Acta Derm Venereol, 2020. 100(12): p. adv00161.
3 Langan, S.M., A.D. Irvine e S. Weidinger, Dermatite atopica. Lancet, 2020. 396(10247): p. 345-360.
4 Song, A., S.E. Lee e J.H. Kim, Immunopatologia e immunoterapia delle malattie infiammatorie della pelle.Immune Netw, 2022(1): p. e7.
5 Silvestre JF e altri. Carico nel mondo reale nei pazienti con dermatite atopica candidati alla terapia sistemica e che attualmente non ricevono alcuna terapia sistemica, nessun trattamento, terapia topica da sola o terapia sistemica: risultati di uno studio multinazionale sul mondo reale. EADV, Milano, 7-11 settembre 2022. Sessione orale FC02.02.
6 Megna, M., et al, Trattamento sistemico della dermatite atopica dell’adulto: una revisione. Dermatol Ther (Heidelb), 2017. 7(1): p. 1-23.
7. informazioni attuali per gli operatori sanitari RINVOQ® (upadacitinib) su www.swissmedicinfo.ch
Le referenze possono essere richieste dai professionisti all’indirizzo medinfo.ch@abbvie.com.
Autore: Dr Corinne Peter
Brevi informazioni tecniche RINVOQ®
Questo articolo è stato realizzato con il sostegno finanziario di AbbVie AG, Alte Steinhauserstrasse 14, Cham.
CH-RNQD230038_11/2023
Contributo online dal 23.10.2023
Questo articolo è stato pubblicato in tedesco
Messaggio aggiornato: 17.11.2023












