Con la continua espansione del panorama terapeutico, sta cambiando anche la gestione della terapia per le malattie reumatiche infiammatorie croniche come l’artrite reumatoide (RA), l’artrite psoriasica (PsA) e la spondilite anchilosante (AS). Le malattie sono spesso associate a limitazioni fisiche e psicologiche e la remissione è l’obiettivo primario del trattamento, al fine di migliorare la qualità di vita del paziente.1-5 Le decisioni terapeutiche individuali giocano un ruolo importante in questo caso.6 Al congresso annuale della Società Svizzera di Reumatologia (SGR), i trattamenti per RA, PsA e AS sono stati discussi in un simposio interattivo.
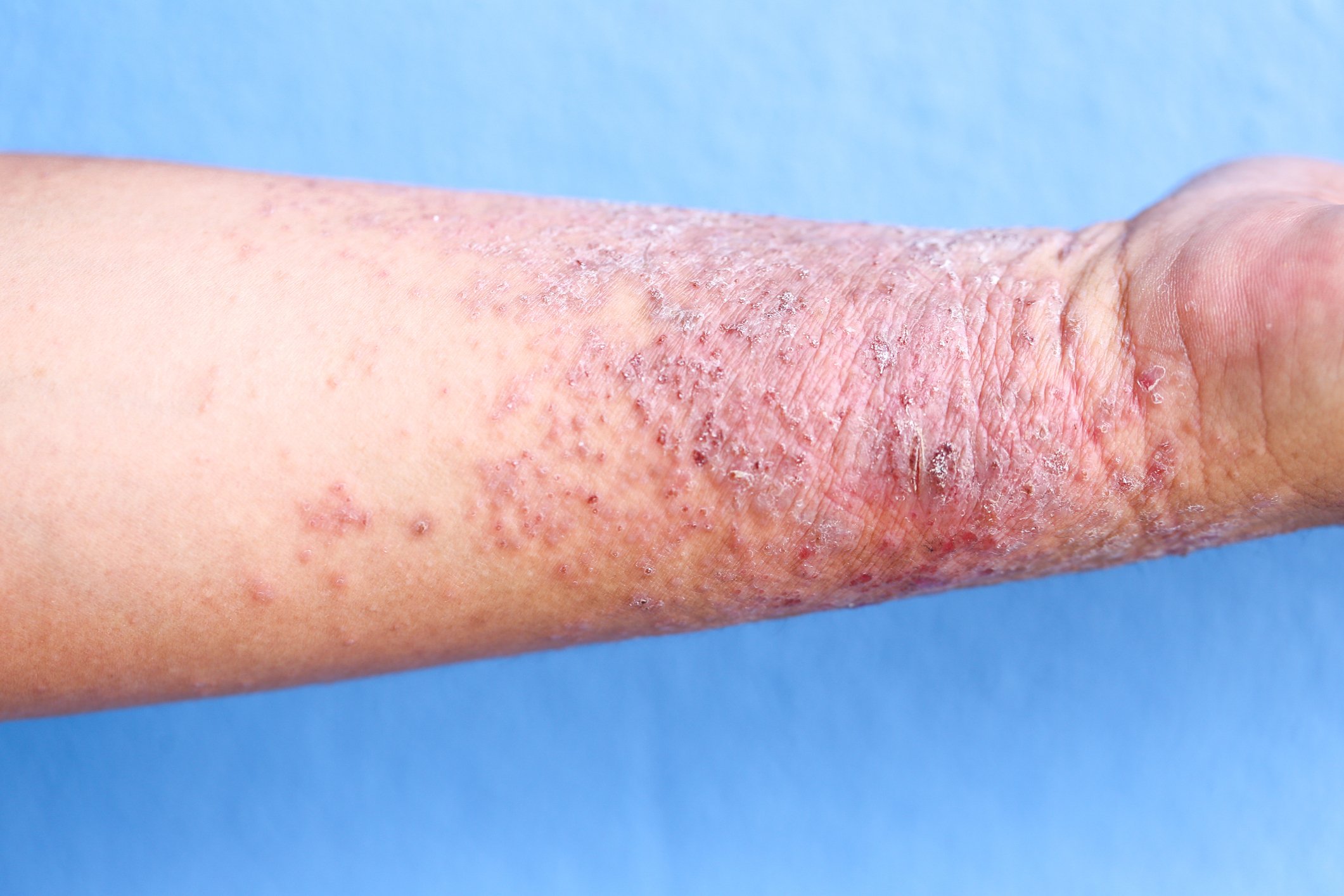
Le malattie reumatiche possono essere associate a manifestazioni extra-articolari e a comorbidità che aumentano il rischio di mortalità.1-3 I pazienti con RA mostrano un rischio maggiore di eventi cardiovascolari, che sono anche più spesso fatali rispetto alla popolazione generale.7 Fino al 30% del rischio di malattie cardiovascolari negli uomini e nelle donne è associato alle caratteristiche della malattia di RA. Il raggiungimento della remissione, quindi, non solo migliora la qualità di vita (QoL) dei pazienti con RA, ma riduce anche il rischio di eventi cardiovascolari, infezioni gravi e tumori.8-12 Nella PsA, una malattia eterogenea caratterizzata da manifestazioni muscolo-scheletriche nelle articolazioni periferiche, nella colonna vertebrale e sulla pelle, anche la QoL delle persone colpite è fortemente limitata. Circa due terzi dei pazienti hanno più di un dominio attivo; queste manifestazioni multiple aumentano ulteriormente il carico della malattia.13, 14 Le decisioni individuali sul trattamento sono di grande importanza in questo caso.6 La SA è anche una malattia muscoloscheletrica cronica, progressiva ed eterogenea, caratterizzata da dolore infiammatorio alla schiena e rigidità della colonna vertebrale, che colpisce principalmente lo scheletro assiale ed è associata a un grave onere fisico, psicologico e socioeconomico per le persone colpite.15, 16 A differenza di altre malattie reumatiche, esiste solo una gamma limitata di opzioni terapeutiche per la SA, che mostrano un’efficacia clinica limitata e comprendono il fattore di necrosi tumorale (TNF), l’interleuchina (IL)-17 e gli inibitori della Janus chinasi (JAK).17
Profilo beneficio-rischio di upadacitinib nell’AR
Nei pazienti con RA che avevano mostrato una risposta inadeguata ai farmaci antireumatici sintetici modificanti la malattia (csDMARDs) convenzionali, l’inibitore JAK (JAKi) upadacitinib (UPA, RINVOQ®) è stato più efficace nel raggiungere la remissione rispetto al principio attivo adalimumab (ADA) negli studi pivotal.18 Nei pazienti più refrattari che avevano già risposto in modo inadeguato a un farmaco biologico (bDMARDs), l’UPA era anche superiore al trattamento con abatacept.19 Un’analisi del rischio-beneficio basata su un’ipotetica coorte di 100 pazienti RA refrattari al metotrexato (MTX) ha dimostrato che il trattamento con UPA + MTX ha portato a tassi di remissione migliori nel punteggio DAS28-CRP* rispetto al trattamento con ADA + MTX. I tassi di eventi cardiovascolari avversi maggiori (MACE), di tumori maligni e di tromboembolismo venoso (VTE) erano comparabili tra i trattamenti.20
Un’analisi recentemente pubblicata di pazienti con RA di età ≥50 anni e con almeno un fattore di rischio cardiovascolare ha esaminato una popolazione simile a quella dello Studio di Sorveglianza ORAL.21 Questa analisi ha mostrato che l’incidenza di MACE, tumori maligni (ad eccezione del tumore della pelle non melanoma (NMSC)) e TEV era generalmente più alta nelle popolazioni con un maggiore rischio cardiovascolare. Tuttavia, l’incidenza di questi eventi avversi era anche paragonabile tra le rispettive terapie con UPA, ADA e MTX(Fig. 1).22 Nel complesso, l’UPA ha mostrato un profilo rischio-beneficio favorevole negli studi condotti.20, 22

Fig. 1: Analisi rischio-beneficio della JAKi nell’AR. A) Efficacia di UPA negli studi clinici testa a testa di fase 3. B) Sicurezza dell’UPA nei pazienti con RA ≥50 anni e con ≥1 fattore di rischio cardiovascolare.
ABA, abatacept; ADA, adalimumab; CV, cardiovascolare; DAS28, punteggio di attività della malattia basato su 28 articolazioni; EAIR, tasso di incidenza aggiustato per l’esposizione; EOW, ogni due settimane; EXCL, escluso; IV, endovenoso; IR, risposta inadeguata; MACE, eventi avversi cardiovascolari maggiori; MTX, metotrexato; NMSC, tumore cutaneo non melanocitico; PBO, placebo; QD, una volta al giorno; PY, anni-paziente; RA, artrite reumatoide; UPA, upadacitinib.
Adattato da 18, 19, 23
Risankizumab migliora la QoL in diversi gruppi di pazienti24
Risankizumab (RZB, SKYRIZI®) è un inibitore selettivo della subunità p19 dell’interleuchina-23, che ha dimostrato un’efficacia solida e duratura in tutte le manifestazioni della PsA(Fig. 2).24, 25 La RZB ha ottenuto una buona efficacia nei pazienti con un coinvolgimento articolare sia limitato che intenso.26 Inoltre, il trattamento con RCB ha portato a un miglioramento significativo della QoL in diversi gruppi di pazienti.24 Data l’eterogeneità della PsA, le decisioni terapeutiche devono essere individualizzate e si deve tenere conto dell’efficacia dei farmaci utilizzati sulle manifestazioni muscoloscheletriche ed extra-muscoloscheletriche. Anche la preferenza del paziente per il dosaggio orale rispetto alle iniezioni sottocutanee a intervalli più lunghi deve essere presa in considerazione nella decisione di trattamento.6 Con il regime di dosaggio di 12 settimane, l’RZB può apportare miglioramenti duraturi nelle manifestazioni muscoloscheletriche e nell’aspetto della pelle dei pazienti con PsA e mostra un profilo di sicurezza favorevole.27
Dal settembre 2023, RZB è stato approvato anche per il trattamento di pazienti adulti con malattia di Crohn attiva da moderata a grave che hanno risposto in modo inadeguato alla terapia convenzionale o a un biologico.28

Fig. 2: RZB mostra efficacia in tutte le manifestazioni della PsA.
aPazienticon BSA ≥ 3% al basale; bPazienticon LEI > 0 al basale; cPazienticon LDI > 0 al basale; dPazienticon spondilite al basale.
ACR50, American College of Rheumatology 50% di miglioramento; BASDAI, Bath Ankylosing Spondylitis Disease Activity Index; BSA: superficie corporea; HAQ-DI, Health Assessment Questionnaire-Disability Index; LDI, Leeds Dactylitis Index; LEI, Leeds Enthesitis Index; MCID, differenza minima clinicamente importante; MDA, attività minima di malattia; PASI 90, Psoriasis Area Severity Index 90% di miglioramento; PsA, artrite psoriasica; PsA-mTSS, psoriatic arthritis modified total Sharp score; Q12W, ogni 12 settimane.
Adattato da 24, 25
Upadacitinib nella SA
Una recente meta-analisi di rete indica un’efficacia comparabile di tutti i trattamenti precedentemente approvati per la SA(Fig. 3).17 Al contrario, l’UPA ha mostrato costantemente tassi di risposta numericamente più elevati, come il raggiungimento dell’ASAS40*, e un minor numero necessario da trattare (NNT) nei pazienti con AS biologici-naïve, così come nei pazienti con AS che avevano risposto in modo inadeguato ai biologici o agli inibitori del TNF.17 Con il suo nuovo meccanismo d’azione, l’UPA offre una risposta rapida, tassi di remissione migliorati (o bassa attività della malattia) e un profilo di sicurezza coerente con la somministrazione orale una volta al giorno nel trattamento della SA.29

Conclusione
Il panorama dei trattamenti per le malattie reumatiche è in crescita e offre un potenziale sempre maggiore di decisioni terapeutiche personalizzate. Questi dovrebbero prendere in considerazione l’eterogeneità delle malattie e i desideri del paziente, al fine di ottenere la remissione e migliorare la QoL delle persone colpite in modo sostenibile e a lungo termine.6
* DAS28-CRP, punteggio per l’attività della malattia basato su 28 articolazioni; BASDAI, Bath Ankylosing Spondylitis Disease Activity Index; ASAS40, Assessment of Spondyloarthritis International Society Improvement ≥40%.
Testo: Dr. sc. nat. Katja Becker
Breve informazione tecnica RINVOQ® e SKYRIZI®.
Questo articolo è stato realizzato con il sostegno finanziario di AbbVie AG, Alte Steinhauserstrasse 14, Cham.
CH-SKZ-230006_10/2023
Questo articolo è stato pubblicato in tedesco.
Articolo online dal 21.11.2023
Letteratura
1 Smolen JS e altri. Trattare la spondiloartrite, compresa la spondilite anchilosante e l’artrite psoriasica, in modo mirato: raccomandazioni di una task force internazionale. Ann Rheum Dis, 2014. 73(1): p. 6-16.
2 Gibofsky A. Epidemiologia, fisiopatologia e diagnosi dell’artrite reumatoide: una sinossi. Am J Manag Care, 2014. 20(7 Suppl): p. S128-35.
3 Gossec L e altri. Raccomandazioni EULAR per la gestione dell’artrite psoriasica con terapie farmacologiche: aggiornamento 2019. Ann Rheum Dis, 2020. 79(6): p. 700-712.
4 Smolen JS e altri. Raccomandazioni EULAR per la gestione dell’artrite reumatoide con farmaci antireumatici sintetici e biologici modificanti la malattia: aggiornamento 2019. Ann Rheum Dis, 2020. 79(6): p. 685-699.
5 Fraenkel L e altri. Linea guida 2021 dell’American College of Rheumatology per il trattamento dell’artrite reumatoide. Arthritis Care Res (Hoboken), 2021. 73(7): p. 924-939.
6 Coates LC e altri. Gruppo per la Ricerca e la Valutazione della Psoriasi e dell’Artrite Psoriasica (GRAPPA): raccomandazioni di trattamento aggiornate per l’artrite psoriasica 2021 Nat Rev Rheumatol, 2022. 18(8): p. 465-479.
7 Schieir O e altri. Infarto miocardico incidente associato ai principali tipi di artrite nella popolazione generale: una revisione sistematica e una meta-analisi. Ann Rheum Dis, 2017. 76(8): p. 1396-1404.
8 Crowson CS e altri. Impatto dei fattori di rischio associati agli esiti cardiovascolari nei pazienti con artrite reumatoide. Ann Rheum Dis, 2018. 77(1): p. 48-54.
9 McInnes IB e altri. La patogenesi dell’artrite reumatoide. N Engl J Med, 2011. 365(23): p. 2205-19.
10 Solomon DH e altri. Attività della malattia nell’artrite reumatoide e rischio di eventi cardiovascolari. Arthritis Rheumatol, 2015. 67(6): p. 1449-55.
11 Accortt NA et al. Impatto della remissione sostenuta sul rischio di infezioni gravi nei pazienti con artrite reumatoide.Arthritis Care Res (Hoboken), 2018. 70(5): p. 679-684.
12 Baecklund E e altri. Associazione dell’infiammazione cronica, non del suo trattamento, con un aumento del rischio di linfoma nell’artrite reumatoide. Arthritis Rheum, 2006. 54(3): p. 692-701.
13 Ritchlin CT e altri. Artrite psoriasica. N Engl J Med, 2017. 376(21): p. 2095-6.
14 Ogdie A e altri. Effetto delle presentazioni multidimensionali della malattia sui pazienti con artrite psoriasica nel registro Corrona Psoriatic Arthritis/Spondyloarthritis. J Rheumatol, 2021. 48(5): p. 698-706.
15. van der Heijde D et al. Efficacia e sicurezza di upadacitinib per la spondilite anchilosante attiva refrattaria alla terapia biologica: studio di fase 3 in doppio cieco, randomizzato e controllato con placebo. Ann Rheum Dis, 2022. 81(11): p. 1515-1523.
16 Navarro-Compán V et al. Spondiloartrite assiale. Ann Rheum Dis, 2021. 80(12): p. 1511-1521.
17 Walsh JA et al. Benefici clinici ed economici delle terapie avanzate per il trattamento della spondilite anchilosante attiva.Rheumatol Ther, 2023. 10(5): p. 1385-1398.
18 Fleischmann R et al. Upadacitinib rispetto a placebo o adalimumab nei pazienti con artrite reumatoide e risposta inadeguata al metotrexato: risultati di uno studio di fase III, in doppio cieco, randomizzato e controllato. Arthritis Rheumatol, 2019. 71(11): p. 1788-1800.
19 Rubbert-Roth A et al. Studio di Upadacitinib o Abatacept nell’artrite reumatoide. N Engl J Med, 2020. 383(16): p. 1511-1521.
20 Conaghan P et al. Analisi del rapporto beneficio/rischio di Upadacitinib rispetto ad Adalimumab nel trattamento di pazienti con artrite reumatoide da moderata a grave. Rheumatol Ther, 2022. 9(1): p. 191-206.
21 Ytterberg SR et al. Rischio cardiovascolare e di cancro con Tofacitinib nell’artrite reumatoide. N Engl J Med, 2022. 386(4): p. 316-326.
22 Fleischmann R et al. Profilo di sicurezza di upadacitinib nei pazienti a rischio di malattie cardiovascolari: analisi integrata post hoc del programma clinico di fase III SELECT per l’artrite reumatoide. Ann Rheum Dis, 2023. 82(9): p. 1130-1141.
23 Fleischmann R e altri. Profilo di sicurezza di upadacitinib nei pazienti a rischio di malattie cardiovascolari: analisi integrata post hoc del programma clinico SELECT di fase III sull’artrite reumatoide. Ann Rheum Dis, 2023.
24 Kristensen LE e altri. Pos1524: Miglioramenti duraturi e clinicamente significativi della qualità della vita, della fatica, del dolore e della produttività lavorativa dei pazienti con artrite psoriasica attiva trattati con risankizumab alla settimana 100. Ann Rheum Dis, 2023. 82: p. 1123.
25 Kristensen LE e altri. Efficacia e sicurezza di risankizumab per l’artrite psoriasica attiva: risultati a 52 settimane dallo studio KEEPsAKE 1. Rheumatology (Oxford), 2023. 62(6): p. 2113-2121.
26 Ogdie A e altri. Pos 1504 Efficacia di Risankizumab nel trattamento di pazienti affetti da PsA con coinvolgimento articolare limitato ed esteso. Presentato all’American College of Rheumatology (ACR) Convergence, 10-14 novembre 2022, Philadelphia, Pennsylvania.
27 Informazioni tecniche aggiornate su SKYRIZI® (rizankizumab) su www.swissmedicinfo.ch.
28. Riassunto attuale delle caratteristiche del prodotto di SKYRIZI® (risankizumab) Malattia di Crohn su www.swissmedicinfo.ch.
29 Riassunto attuale delle caratteristiche del prodotto di RINVOQ® (upadacitinib) su www.swissmedicinfo.ch.
Le referenze possono essere richieste dai professionisti all’indirizzo medinfo.ch@abbvie.com.