Um documento de revisão resumiu os resultados de quatro estudos aleatorizados em dupla ocultação, controlados por placebo ou por referência, de uma preparação combinada de Sabal-Urtica em homens com mais de 50 anos de idade com LUTS associados à HBP. A fitopreparação provou ser uma alternativa válida aos medicamentos sintéticos. O perfil favorável de efeitos secundários é um ponto positivo, especialmente para a terapia a longo prazo.
Em cerca de metade dos homens com mais de 50 anos, ocorrem alterações benignas nos tecidos da próstata, sob a forma de um aumento do tecido conjuntivo, do músculo e/ou das células epiteliais (hiperplasia benigna da próstata, HBP). Devido à hiperplasia do órgão, a compressão da uretra pode levar a um aumento da resistência da saída da bexiga – obstrução benigna da próstata (BPO). A HBP é a principal causa dos sintomas do trato urinário inferior ( LUTS), que incluem retenção vesical, sintomas miccionais e miccionais [1]. Em particular, os antagonistas dos receptores α1-adrenérgicos, os inibidores da 5α-redutase e os fitoterápicos são utilizados como terapia de primeira linha para os sintomas LUTS associados à HBP [2].
Há um interesse crescente nas opções de tratamento fitoterapêutico, sobretudo porque alguns doentes estão insatisfeitos com os efeitos adversos dos medicamentos sintéticos [3]. A terapia com antagonistas dos receptores α1-adrenérgicos e inibidores da 5α-redutase, por exemplo, pode estar associada a efeitos secundários sexuais, tais como disfunção erétil e perturbações da ejaculação [4]. Além disso, a maioria dos antagonistas dos receptores α-adrenérgicos apresenta um risco relativamente elevado de efeitos secundários relacionados com os vasos sanguíneos [5]. Os efeitos secundários cardiovasculares, como a hipotensão, acompanhada de tonturas ou síncope, afectam principalmente os homens mais velhos – ou seja, o principal grupo de doentes com LUTS/BPH que necessitam de terapia medicamentosa [6–8].
O medicamento PRO 160/120 (Prostaplant®-F) é uma alternativa fitoterapêutica promissora para o tratamento dos LUTS. A preparação combinada contém 160 mg de extrato de fruto de palmeira anã (Serenoa repens ou Sabal serrulata) e 120 mg de extrato seco de raiz de urtiga (Urtica dioica) como principais ingredientes farmacológicos activos (caixa ) [9].
| Mecanismos de ação do PRO 160/120 A preparação fitofarmacológica combinada de extractos de Sabal (extrato de palmeira anã) e de Urtica (raiz de urtiga) apresenta efeitos sinérgicos. Entre outras coisas, é induzida a conversão da testosterona em dihidrotestosterona e a atividade da aromatase [18]. O relaxamento do tecido prostático inchado resulta numa redução da pressão sobre a uretra. Devido ao seu efeito anti-inflamatório, PRO 160/120 reduz a irritação da próstata [19]. Foi demonstrado que o extrato de Saw palmetto inibe a 5α-redutase sem apresentar atividade de ligação aos androgénios [20,21] e provoca uma inibição não competitiva dos α1-adrenoceptores humanos in vitro [22]. Também inibe seletivamente os receptores muscarínicos no trato urinário inferior [23,24]. O extrato de raiz de urtiga inibe a atividade da Na+, K+-ATPase da membrana da próstata, o que pode limitar o metabolismo e o crescimento das células da próstata [25]. Além disso, foram relatados efeitos antiproliferativos, antiflogísticos e antiedematosos para ambos os agentes [27,28]. |
Escala Internacional de Sintomas da Próstata (I-PSS)
Nos estudos incluídos na revisão, a melhoria dos sintomas foi avaliada utilizando o International Prostate Symptom Score (I-PSS) [10–13]. Trata-se de um instrumento de medição fiável e válido, comummente utilizado para avaliar os LUTS associados à HBP, com sete perguntas sobre a micção, cada uma pontuada de 0 a 5 [2,14]. As perguntas referem-se geralmente ao mês anterior. Nos quatro estudos [10–13], foi alcançada uma melhoria de mais de três pontos na pontuação total do I-PSS, o que é classificado como uma alteração clinicamente significativa [16]. Os seguintes parâmetros foram recolhidos como outros parâmetros finais: Volume do tempo de urina ou volume do tempo de urina, tempo de fluxo de urina, fluxo médio de urina, fluxo máximo de urina, volume de micção, duração da micção (tempo de esvaziamento da bexiga), volume residual de urina, volume da próstata, qualidade de vida. Além disso, foram registados eventos adversos e sinais de segurança de diagnóstico laboratorial.
Resultados importantes do estudo num relance
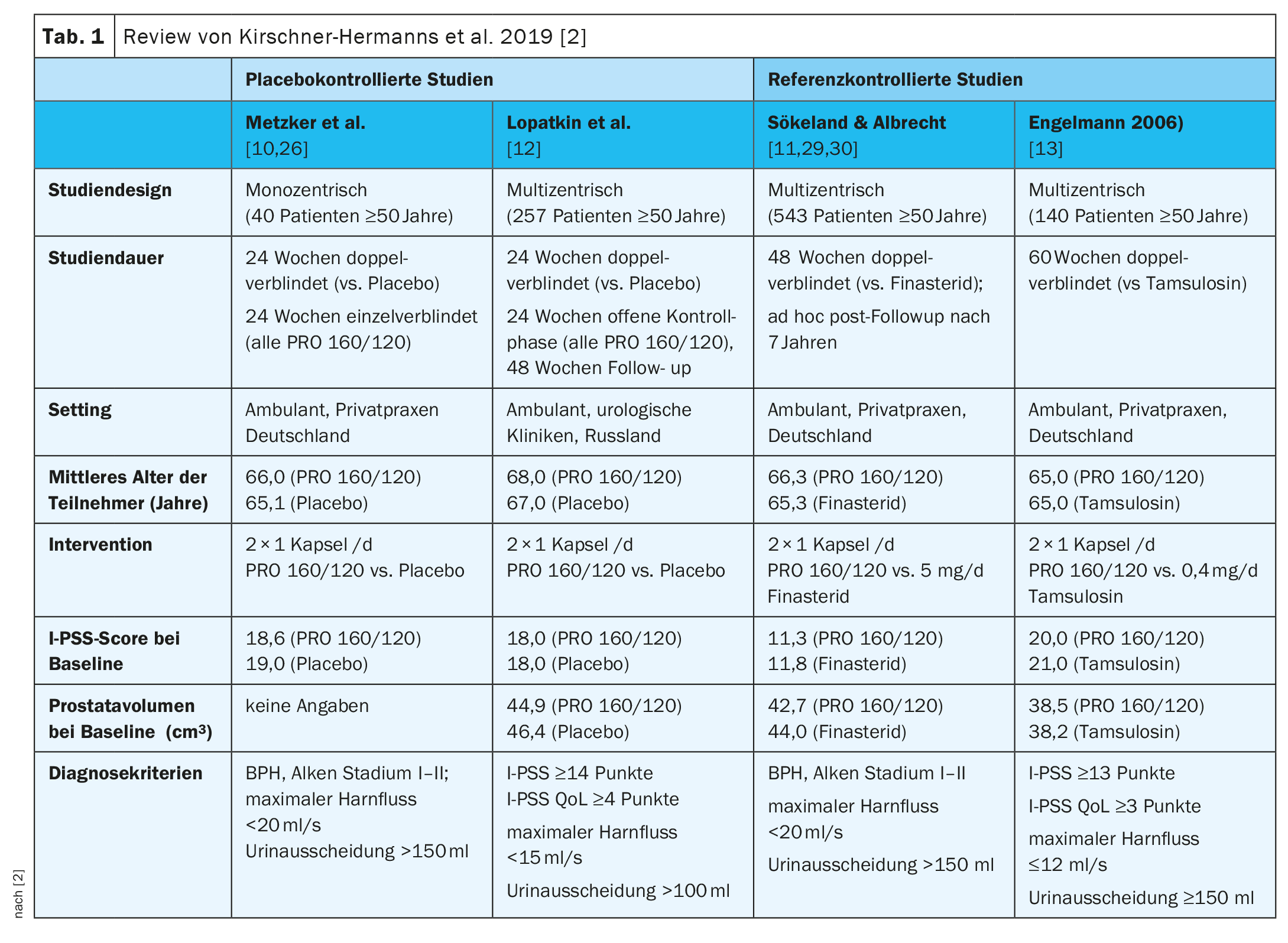
Os principais dados dos quatro estudos podem ser consultados no Quadro 1 [2,10–13]. No processo Metzker et al. e Lopatkin et al. foram controlados por placebo e em Engelmann et al. e Sökeland & Albrecht para estudos controlados de referência [2,10–13].
Metzker et al (n=40) [10]: Na fase de tratamento em dupla ocultação, o I-PSS médio diminuiu de valores basais de 18,6 pontos no grupo PRO 160/120 e 19,0 pontos no grupo placebo para 11,1 e 17,6 pontos na semana 24, respetivamente (p=0,002; teste U bilateral). Numa avaliação post-hoc destes resultados, que se centrou nos itens do I-PSS que avaliam os chamados sintomas irritativos, foi demonstrado que houve uma melhoria estatisticamente significativa da urgência urinária e da frequência miccional no PRO 160/120 durante esta fase de tratamento [26]. Na fase de tratamento simples-cego subsequente, o I-PSS também diminuiu nos doentes que passaram do placebo para o tratamento com PRO 160/120. No entanto, à semana 48, continuava a haver uma vantagem a favor do grupo que estava no braço de tratamento ativo (PRO 160/120) em ambas as fases do estudo (p=0,009; teste U bilateral).
Lopatkin et al. (n=257) [12]: Após a fase de tratamento em dupla ocultação, foi observada uma diferença de grupo estatisticamente significativa no declínio do I-PSS a favor do PRO 160/120; -6 pontos no braço do tratamento e -4 pontos no braço do placebo (p<0,01, teste U unilateral estratificado). No final da fase de controlo, o I-PSS foi reduzido em mais 2 pontos nos antigos doentes tratados com placebo (que agora também eram tratados com PRO 160/120) e em mais 1 ponto nos doentes que tinham sido tratados com PRO 160/120 desde o início do estudo. Esta diferença entre os dois grupos de tratamento também foi estatisticamente significativa (p=0,01, teste U estratificado unilateral). No final da fase de controlo, a redução do I-PSS médio em ambos os grupos de tratamento foi de sete pontos em comparação com a linha de base, indicando que os antigos doentes com placebo beneficiaram do tratamento com PRO 160/120 na mesma medida que os doentes que já tinham sido tratados com PRO 160/120 desde o início do tratamento em dupla ocultação [15]. Após a fase de controlo, 213 pacientes (PRO 160/120: 106; placebo: 107) participaram na extensão aberta subsequente do estudo (semanas 49-96) [17]. Nos doentes sem pontuações I-PSS em falta na linha de base (PRO 160/120: 106; placebo: 103), foi observada uma redução mediana adicional de 1 ponto em cada grupo, resultando numa redução mediana global de 9 pontos em ambos os grupos em comparação com a linha de base. Isto corresponde a uma redução de 52,9% na pontuação total do I-PSS em comparação com a linha de base.
Sökeland & Albrecht (n=543) [11]No final do estudo, os sintomas dos doentes tratados com PRO 160/120 tinham melhorado de forma semelhante aos dos doentes tratados com finasterida, com o I-PSS a aumentar de 11,3 ± 6,5 pontos (PRO 160/120) e 11,8 ± 6,6 pontos (finasterida) no início do estudo para 8,2 ± 5,8 pontos (PRO 160/120) e 8,0 ± 5,7 pontos (finasterida) na semana 24. 11,8 ± 6,6 pontos (finasterida) na linha de base para 8,2 ± 5,8 pontos (PRO 160/120) e 8,0 ± 5,7 pontos (finasterida) na semana 24 e 6,5 ± 5,8 pontos (PRO 160/120) e 6,2 ± 5,2 pontos (finasterida) na semana 48 (médias ± DP). A melhoria da qualidade de vida de acordo com a pontuação C da AUA também foi semelhante à da finasterida. O aumento do fluxo máximo de urina com PRO 160/120 (+1,9 ml/s) e finasterida (+2,4 ml/s) revelou-se terapeuticamente comparável num intervalo de equivalência de ±1,5 ml/s (p=0,037; teste t modificado para hipóteses deslocadas).
Engelmann et al. (n=140) [13]: A pontuação total do IPSS melhorou numa média de 9 pontos no final do tratamento em ambos os grupos, a partir de uma pontuação inicial de cerca de 20 pontos. Um total de 32,4% dos doentes tratados com PRO 160/120 e 27,9% dos doentes tratados com tansulosina foram respondedores (ou seja, pontuação total IPSS ≤7 no final do tratamento; p=0,034, teste de não inferioridade Farrington-Manning; limiar de não inferioridade 10%). Numa análise de subgrupo por pontuação I-PSS basal, o PRO 160/120 e a tansulosina foram comparativamente eficazes tanto em doentes com sintomas moderados (I-PSS basal ≤19 pontos) como em doentes com sintomas graves (I-PSS basal ≥20 pontos). A qualidade de vida dos doentes melhorou numa mediana de 2 pontos no grupo PRO 160/120 e de 1 ponto no grupo da tansulosina (valores de base: 3 pontos e 4 pontos, respetivamente; medianas).
Literatura:
- S2e-Leitlinie Diagnostik und Therapie des Benignen Prostatasyndroms (BPS), Registernummer: 043-034, Langversion 5.0 – Stand Februar 2023.
- Kirschner-Hermanns R, Funk P, Leistner N: WS PRO 160 I 120 mg (uma combinação de sabal e extracto de urtica) em doentes com LUTS relacionados com BPH. Ther Adv Urol 2019 Oct 11;11:1756287219879533.
- Geavlete P, Multescu R, Geavlete B: Extrato de Serenoa repens no tratamento da hiperplasia benigna da próstata. Ther Adv Urol 2011; 3: 193-198.
- Mirone V, et al: Tratamento atual da hiperplasia benigna da próstata: impacto na função sexual e gestão de eventos adversos sexuais relacionados. Int J Clin Pract 2011; 65: 1005-1013.
- Nickel JC, Sander S, Moon TD: A meta-analysis of the vascular-related safety profile and efficacy of alpha-adrenergic blockers for symptoms related to benign prostatic hyperplasia. Int J Clin Pract 2008; 62: 1547-1559.
- Logan IC, Witham MD: Efficacy of treatments for orthostatic hypotension: a systematic review (Eficácia dos tratamentos para a hipotensão ortostática: uma revisão sistemática). Ageing 2012; 41: 587-594.
- Man in’t Veld AJ: HBP sintomática e hipertensão: a comorbilidade afecta a qualidade de vida? Eur Urol 1998; 34(Suppl. 2): 29-36.
- Schimke L, Schimke J: Implicações urológicas das quedas nos idosos: sintomas do trato urinário inferior e medicamentos alfa-bloqueadores. Urol Nurs 2014; 34: 223-229.
- Informações sobre medicamentos, www.swissmedicinfo.ch,(último acesso em 15.09.2023)
- Metzker H, Kieser M, Hölscher U: Eficácia de uma preparação combinada de Sabal-Urtica no tratamento da hiperplasia benigna da próstata (BPH). Urologist B 1996; 36: 292-300.
- Sökeland J, Albrecht J: Combinação de extrato de sabal e urtica vs. finasterida na HBP (stad. I a II de acordo com Alken). Comparação da eficácia terapêutica num estudo duplamente cego de um ano. Urologist A 1997; 36: 327-333.
- Lopatkin N, et al: Eficácia e segurança a longo prazo de uma combinação de extrato de sabal e urtica para sintomas do trato urinário inferior – um ensaio multicêntrico, duplamente cego e controlado por placebo. World J Urol 2005; 23: 139-146.
- Engelmann U, et al.: Eficácia e segurança de uma combinação de extrato de sabal e urtica nos sintomas do trato urinário inferior. Um estudo aleatório e em dupla ocultação versus tamsulosina. Arzneimittelforschung 2006; 56: 222-229.
- McConnell J, et al. (Eds): Disfunção do trato urinário inferior masculino. Avaliação e gestão. In: Proceedings of the6th International Consultation on New Developments in Prostate Cancer and Prostate Diseases, Paris, França, 24-27 de junho de 2005. Publicações de Saúde, 2006.
- Sivkov A, et al: Longterm efficacy and safety of a combination of sabal and urtica extracts in LUTS – a placebo-controlled, double-blind, multicenter trial. Urologist A 2001; 40(Suppl. 1): S19.
- Barry MJ, et al: Medidas do estado de saúde específicas da hiperplasia prostática benigna na investigação clínica: qual o grau de alteração do índice de sintomas da Associação Americana de Urologia e do índice de impacto da hiperplasia prostática benigna que é percetível para os doentes? J Urol 1995; 154: 1770-1774.
- Lopatkin et al: Eficácia e segurança de uma combinação de extrato de Sabal e Urtica nos sintomas do trato urinário inferior – acompanhamento a longo prazo de um ensaio multicêntrico, duplamente cego e controlado por placebo. Int Urol Nephrol 2007; 39: 1137-1146.
- Madersbacher S, et al.: Associação entre as prescrições de PRO 160/120 e a incidência de complicações da hiperplasia benigna da próstata na Alemanha: um estudo de coorte retrospetivo. Postgrad Med 2023; 135(2): 149-154.
- Koch E: Extractos de frutos de palmeira serrada (Sabal serrulata) e raízes de urtiga picante (Urtica dioica): alternativas viáveis no tratamento médico da hiperplasia benigna da próstata e sintomas associados das vias urinárias inferiores. Planta Med 2001; 67(6): 489-500.
- Casarosa C, et al.: Ausência de efeitos de um extrato lioposterólico de Serenoa repens nos níveis plasmáticos de testos-terona, hormona folículo-estimulante e hormona luteinizante. Clin Ther 1988; 10: 585-588.
- Düker EM, Kopanski L, Schweikert HU: Inibição da atividade da 5α-reductase por extractos de Sabal serrulata. Planta Med 1989; 55: 587.
- Goepel M, et al.: Os extractos de Saw palmetto inibem potentemente e de forma não competitiva os 1-adrenoceptores humanos in vitro. Prostate 1999; 38: 208-215.
- 23 Abe M, et al: Características de ligação aos receptores farmacologicamente relevantes e atividade inibidora da 5α-redutase dos ácidos gordos livres contidos no extrato de palmeira anã. Biol Pharm Bull 2009; 32: 646-650.
- Suzuki M, et al.: Características de ligação dos receptores muscarínicos e alfa 1-adrenérgicos do extrato de saw palmetto no trato urinário inferior do rato. Urology 2007; 69: 1216-1220.
- Hirano T, Homma M, Oka K: Efeitos dos extractos de raiz de urtiga e dos seus componentes esteroidais na Na+, K+-ATPase da hiperplasia benigna da próstata. Planta Med 1994; 60: 30-33.
- Popa G, Hägele-Kaddour H, Walther C: Eficácia sintomática de uma preparação combinada de Sabal-Urtica na terapia da síndrome prostática benigna. Resultados de um estudo em dupla ocultação controlado por placebo. MMW Fortschr Med 2005; 147(Originalien III): 103-108.
- Koch E, Biber A: Efeitos farmacológicos dos extractos de sabal e urtica como base para uma terapia medicamentosa racional da hiperplasia benigna da próstata. Urologist B 1994; 34: 90-95.
- Lichius JJ, et al.: Efeito antiproliferativo de uma fração polissacárida de um extrato metanólico a 20% de raízes de urtiga em células epiteliais da próstata humana (LNCaP). Pharmacy 1999; 54: 768-771.
- Sökeland J: Extrato combinado de sabal e urtica comparado com finasterida em homens com hiperplasia benigna da próstata: análise do volume da próstata e do resultado terapêutico. BJU Int 2000; 86: 439-442.
- Sökeland J, Schläfke S: Efeitos a longo prazo do PRO 160/120 em doentes com HBP. Uro-News Therapie Report aktuell 2007; 164: 2-3.