El trasplante de pulmón (Lutx) es también una opción terapéutica establecida en la infancia y la adolescencia cuando, a pesar de haberse agotado todas las medidas terapéuticas disponibles, una enfermedad grave progresa, la calidad de vida se ve significativamente deteriorada como consecuencia de ello y el fallo terminal del órgano parece probable en un futuro próximo. No obstante, el lutx es una intervención importante en la integridad física del niño con muchos riesgos.
El trasplante de pulmón (Lutx) es también una opción terapéutica establecida en la infancia y la adolescencia cuando, a pesar de haberse agotado todas las medidas terapéuticas disponibles, una enfermedad grave progresa, la calidad de vida se ve significativamente deteriorada como consecuencia de ello y el fallo terminal del órgano parece probable en un futuro próximo.

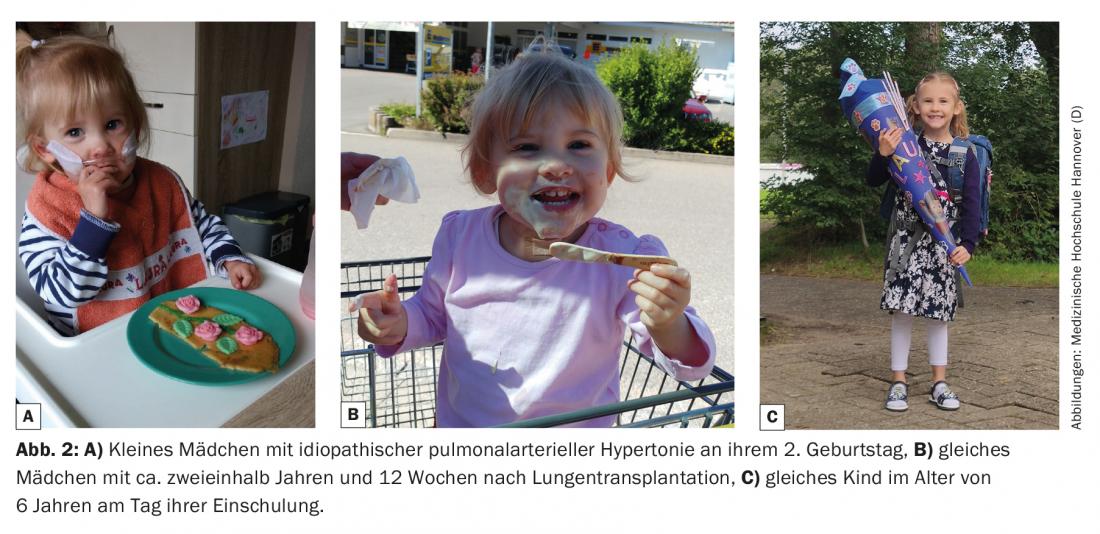
El objetivo principal de prolongar la vida de los afectados y mejorar su calidad de vida se consigue en la mayoría de los casos [1,2] (Fig. 1 y 2). No obstante, la lutx representa una intervención significativa en la integridad física del niño con muchos riesgos, complicaciones potencialmente graves y la necesidad de una terapia farmacológica de por vida con múltiples efectos secundarios potenciales. Esto a su vez tiene considerables efectos sociales y psicológicos en el niño o adolescente en crecimiento, pero también en el entorno familiar. El tipo y el alcance son variables y dependen de muchos factores como la enfermedad subyacente, las comorbilidades adicionales, la edad, el entorno social, así como la estabilidad psicológica de los afectados. Por esta razón, un lutx es, en mi opinión, una posible opción de tratamiento, pero no una conclusión terapéutica obligatoria para los niños con enfermedades potencialmente mortales. La decisión consciente de no someterse a un trasplante no significa renunciar al niño, ni es un signo de debilidad o falta de cuidados, sino que incluso puede ser una decisión mejor para algunos y posiblemente evitarles un sufrimiento innecesario.
Para poder tomar esta grave decisión, a favor o en contra de un trasplante, es indispensable una explicación detallada y honesta tanto del paciente como de los tutores legales, teniendo en cuenta las circunstancias médicas y sociales individuales. En particular, es importante no sólo aceptar el deseo del niño (que no siempre se corresponde con el de los padres), siempre que el niño esté en edad de tomar decisiones, sino también apoyarlo activamente.
Me resulta difícil escribir sobre el crecimiento tras un trasplante de pulmón en la infancia y la adolescencia en general. Por este motivo, he decidido ofrecer en primer lugar una visión general de los aspectos médicos importantes del lutx en la infancia y la adolescencia, para abordar a continuación determinadas características especiales y retos en función de la fase de la vida.
Trasplante de pulmón en niños y adolescentes
Cada año se realizan trasplantes de pulmón a entre 120 y 140 niños en unos 40 centros de todo el mundo. La mayoría de los centros realizan menos de 5 trasplantes al año y menos de 5 centros comunican 10 o más trasplantes al año al Registro Internacional de Trasplantes de Órganos Torácicos de la Sociedad Internacional de Trasplante de Corazón y Pulmón (ISHLT) [3]. El número de trasplantes combinados de corazón y pulmón ha disminuido constantemente en los últimos 20 años y ahora sólo se indica en casos excepcionales. La edad media en el momento del trasplante se sitúa entre los 12 y los 15 años y la fibrosis quística (FQ) sigue siendo la indicación más frecuente, con cerca del 60%, seguida de la hipertensión arterial pulmonar (HAP) [4]. Sin embargo, cabe suponer que la proporción de pacientes pediátricos con fibrosis quística con enfermedad pulmonar terminal disminuirá continuamente en los próximos años debido a la detección más precoz y a la terapia específica mediante el cribado exhaustivo de los recién nacidos, así como a la disponibilidad de moduladores de la fibrosis quística altamente eficaces. Por otro lado, es probable que aumente el número de niños más pequeños con enfermedades pulmonares difusas graves, como las disfunciones del surfactante, sobre todo debido a las cada vez mejores opciones de tratamiento médico intensivo.
La determinación del momento de inclusión en la lista depende en gran medida de la gravedad y la progresión de la enfermedad subyacente. Los criterios de decisión importantes para la inclusión en la lista en pacientes con FQ son un FEV1 inferior a <30% del objetivo, un rápido deterioro imparable de la función pulmonar, exacerbaciones repetidas de la infección que pongan en peligro la vida, hemoptisis grave recurrente o insuficiencia pulmonar crónica hipercápnica [5,6]. En el caso de otras afecciones, se carece de criterios de decisión validados para los niños y, especialmente en el caso de los pacientes con hipertensión arterial pulmonar (HAP) hereditaria o idiopática, la evaluación del pronóstico es muy difícil debido a las cada vez mejores opciones de tratamiento. A menudo, los pacientes se presentan en un centro de trasplantes demasiado tarde, por lo que ya no es posible realizar una evaluación y una formación suficientes, o ni siquiera se les puede incluir en la lista debido a su estado crítico (por ejemplo, ventilados y/o con ECMO). Por lo tanto, todo paciente con enfermedad pulmonar grave, crónica y progresiva debe ser evaluado precozmente en un centro [5]. Un largo periodo de espera también debe tenerse en cuenta a la hora de decidirse a cotizar. El tiempo medio de espera para pacientes pediátricos en Hannover es de unos 3,5 meses. Los procedimientos de trasplante varían en función del centro. En Hannover se favorece el trasplante pulmonar doble bilateral secuencial mediante una técnica mínimamente invasiva por toracotomía anterolateral, a ser posible sin procedimientos de sustitución pulmonar extracorpórea como ECMO o circulación extracorpórea. Los pacientes con HAP constituyen aquí una excepción. En este caso, el ventrículo derecho siempre se alivia intraoperatoriamente mediante ECMO venoarterial o (por ejemplo, en lactantes) con una máquina de circulación extracorpórea. Dado que la hipotrofia ventricular izquierda muscular se desarrolla en todos los pacientes con HAP grave, la descompensación ventricular izquierda debida a la carga de volumen con la correspondiente contrapresión venosa pulmonar y el edema pulmonar resultante es muy común tras el trasplante. Esto, a su vez, se asocia a un largo tiempo de ventilación y a muchas complicaciones como barotrauma, sedación prolongada, inmovilización e infecciones [7]. Por este motivo, en algunos centros se sigue favoreciendo el trasplante combinado de corazón y pulmón para los pacientes con HAP grave. En Hannover, sólo se realizan trasplantes pulmonares aislados en este grupo de pacientes. Sin embargo, tras el trasplante, siempre se deja la va-ECMO para descargar el ventrículo izquierdo y evitar la carga de volumen. Por lo general, los pacientes pueden ser extubados con este procedimiento al cabo de poco tiempo y el ventrículo izquierdo puede ser “entrenado” durante los días siguientes reduciendo progresivamente el flujo de ECMO bajo control ecocardiográfico y medición de la presión auricular izquierda hasta que el ECMO pueda ser explantado al cabo de una media de 7 días. En nuestro centro, este procedimiento ha supuesto una reducción significativa de los tiempos de ventilación, una reducción de la disfunción primaria del injerto y una reducción significativa de la mortalidad [1,8]. Aunque todavía no se ha demostrado en ensayos controlados aleatorizados una ventaja de supervivencia mediante la terapia de inducción, por ejemplo con globulina antitimocítica policlonal o antagonistas monoclonales de los receptores de IL-2, en la actualidad se lleva a cabo en la mayoría de los centros [3].
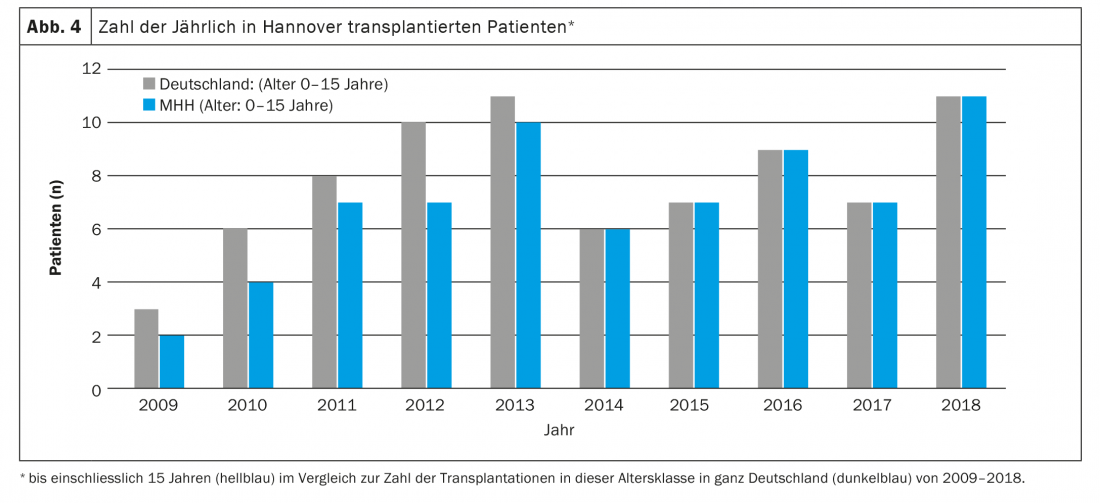
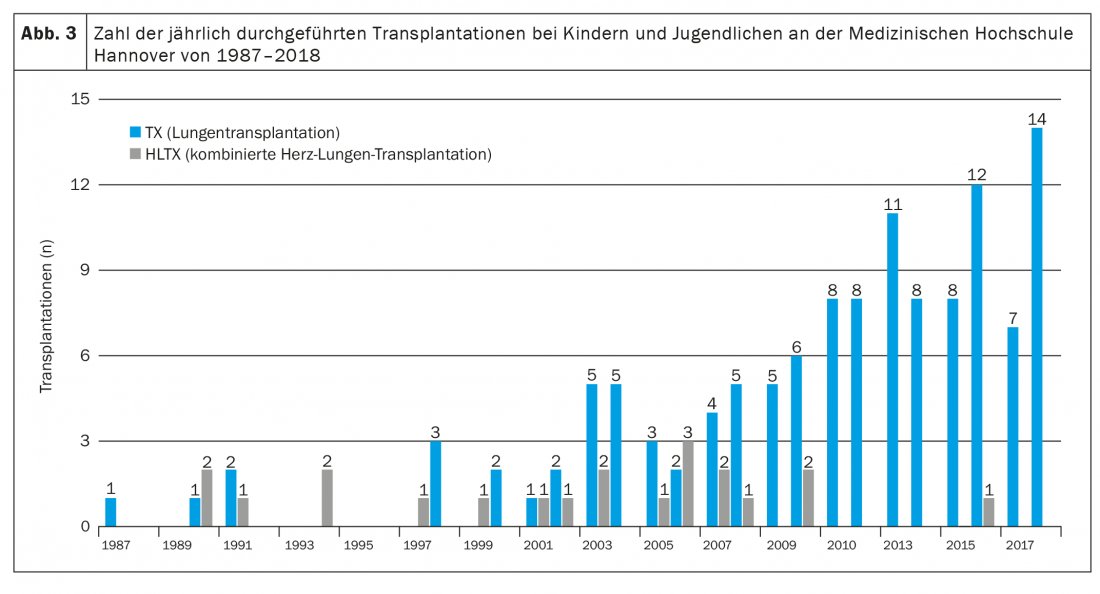
La terapia inmunosupresora a largo plazo consiste en un inhibidor de la calcineurina, un inhibidor del ciclo celular y un glucocorticosteroide, normalmente en forma de tacrolimus, micofenolato mofetil y prednisolona [3,4,9]. Además, todos los pacientes (en Hannover) reciben ganciclovir o valganciclovir para prevenir la infección por CMV, itraconazol o voriconazol para prevenir la infección fúngica y cotrimoxazol para prevenir la infección por Pneumocystis jiroveccii, al menos en los primeros meses tras el trasplante. Además, los efectos secundarios debidos a la terapia inmunosupresora, como la hipertensión arterial, la hipercolesterolemia, la diabetes mellitus (especialmente en pacientes con FQ) y la insuficiencia renal, suelen aparecer muy pronto y deben tratarse con medicación [4]. Debido a la inmunosupresión intensiva necesaria en los primeros 12 meses tras el trasplante, las infecciones son la causa más común de muerte en el primer año postoperatorio [9]. Entre las consecuencias graves a largo plazo (en los primeros 5 años tras la Lutx) de la terapia inmunosupresora se incluyen, en particular, la insuficiencia renal grave (en aproximadamente un 6%), la diabetes mellitus (en aproximadamente un 30%) y los tumores malignos (en aproximadamente un 10%) [3,4,9]. Mientras que los tumores cutáneos son la entidad maligna más común en adultos, los pacientes pediátricos desarrollan predominantemente linfomas asociados al VEB. La causa más común de muerte más allá del primer año tras el trasplante, incluso en niños, es la disfunción crónica del aloinjerto, normalmente en forma de síndrome de bronquiolitis obliterante (BOS) [10]. 5 años después del trasplante, alrededor del 50% de los pacientes están afectados [4]. En comparación con otros trasplantes de órganos sólidos, los pacientes tras Lutx siguen teniendo el peor pronóstico. La mediana de supervivencia tras el Lutx de todos los pacientes pediátricos notificados en el registro ISHLT entre 1992 y 2017 fue de 5,7 años y ha aumentado a 6,4 años en los años más recientes (2002-2009) [4]. Esto se debe principalmente a la mejora de las opciones de tratamiento perioperatorio con una reducción de la mortalidad precoz. Sin embargo, el pronóstico varía considerablemente entre los distintos centros y parece depender en particular del tamaño y, por tanto, de la experiencia de un programa de trasplantes [11]. Con 8-14 trasplantes al año, el Hospital Infantil de la Facultad de Medicina de Hannover es uno de los mayores centros pediátricos de trasplante de pulmón del mundo (Fig. 3) . En este caso, la supervivencia a los 5 años ha aumentado en los últimos años, con un incremento anual del número de pacientes, del 41% (periodo de trasplante 1987-2008) a más del 80% (periodo de trasplante 2014-2018) [1,12].
Una de las principales razones del mal pronóstico en comparación con otros trasplantes de órganos sólidos es probablemente la exposición significativamente mayor del pulmón al medio ambiente, con la consiguiente estimulación constante del sistema inmunológico. Por ejemplo, las infecciones agudas o crónicas de las vías respiratorias inferiores son un factor de riesgo de rechazo crónico del injerto tras un trasplante de pulmón.
Los hechos anteriores ponen de manifiesto la complejidad, las dificultades y el extraordinario estrés que supone un lutx para los niños, los adolescentes y sus familiares y sugieren el impacto que tiene en la vida de un niño en crecimiento.
Aspectos específicos para lactantes y niños pequeños
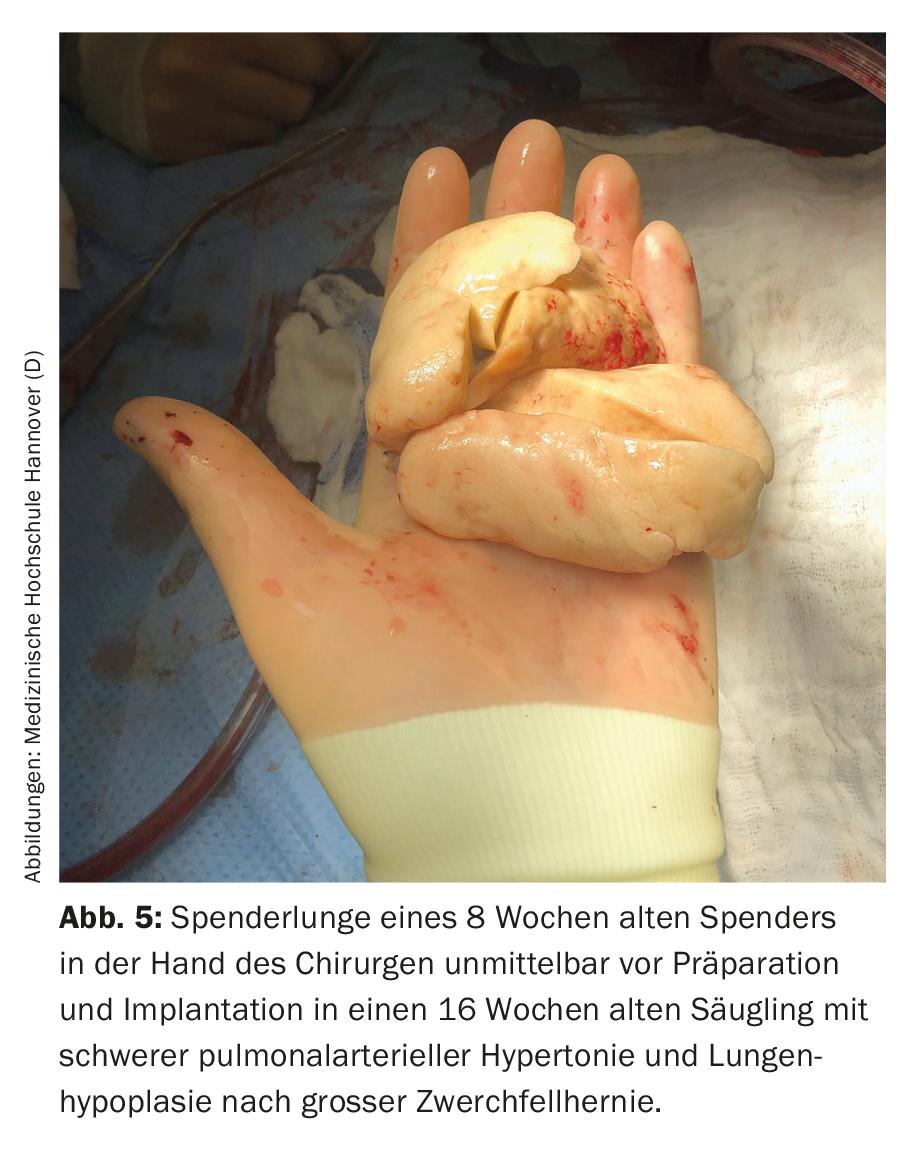
Las principales indicaciones para el trasplante de pulmón en este grupo de edad son la enfermedad pulmonar parenquimatosa difusa y la HAP. Los padres y el personal médico se enfrentan a grandes retos incluso antes del trasplante. En la mayoría de los casos, los niños se encuentran en una situación aguda que pone en peligro su vida, a menudo tienen que ser ventilados, no pocas veces están completamente inmovilizados y tienen que esperar largos tiempos de espera (hospitalizados) debido a la escasez de órganos disponibles. Además de la tensión psicológica que supone para los padres, el largo tiempo de espera se asocia también a evidentes problemas de organización y resulta muy estresante para los hermanos sanos que puedan estar presentes. A menudo uno de los progenitores, en la mayoría de los casos la madre, no puede estar en casa durante semanas o meses, porque una de las personas tiene que cuidar del niño enfermo en la clínica, que casi nunca se encuentra en la ciudad natal de la familia. En Alemania, por ejemplo, casi todos los niños menores de 16 años han sido trasplantados en la Facultad de Medicina de Hannover en los últimos años y sólo unos pocos de ellos viven en Baja Sajonia o incluso en Hannover (Fig. 4) . Las consecuencias resultantes son probablemente difícilmente imaginables para nosotros como personal médico. Debido al mal estado antes del trasplante, la falta de reservas físicas, la corta edad y los difíciles procedimientos quirúrgicos (Fig. 5) y de cuidados intensivos asociados, el riesgo de complicaciones pre y postoperatorias es alto. Debido a su edad, los niños suelen ser incapaces de expresar sus deseos y temores, incluso cuando están conscientes. Los padres se debaten entre el temor por la vida de su hijo y la preocupación de que ni siquiera se consiga el trasplante o de que el niño muera después del trasplante y tenga que soportar un duro calvario hasta entonces. Debido al reducido número total de pacientes trasplantados a esta edad, no es posible obtener información concreta y fiable sobre el pronóstico. El trato con los niños y sus padres, así como la dirección de las conversaciones, requieren por tanto un alto grado de empatía, honestidad, conocimiento de la naturaleza humana y, sobre todo, tiempo.
Los médicos no estamos preparados para tales escenarios durante nuestros estudios y por ello dependemos imperativamente del apoyo de psicólogos, psicoterapeutas y personal de enfermería, entre otros. Otro problema es la constante disminución de los recursos de tiempo debido a la creciente presión pecuniaria para rendir, la flagrante escasez de personal y el continuo aumento de las tareas burocráticas del personal médico. Además, al menos en Alemania, cada vez se recortan más puestos no médicos. Al mismo tiempo, las profesiones que simplemente no “compensan” en la sociedad hospitalaria orientada al rendimiento, como los arteterapeutas, los musicoterapeutas, los psicoterapeutas, los fisioterapeutas o los payasos de clínica, son en muchos aspectos mucho más importantes para los niños y sus padres que los médicos y contribuyen significativamente al bienestar de los pacientes y, por tanto, al éxito de un trasplante. Aquí, un replanteamiento por parte de las instituciones no sólo sería deseable, sino en mi opinión también imperativo. Desgraciadamente, la eficacia del trabajo de los grupos profesionales mencionados apenas puede demostrarse a partir de estudios controlados. El cálculo de las necesidades de personal a partir de datos sólidos es, por tanto, un problema importante de la “medicina basada en pruebas” y no tiene sentido en ámbitos tan marginales como la medicina pediátrica de trasplantes. A menudo, a los padres les resultan muy útiles las conversaciones con otras familias cuyo hijo fue trasplantado a una edad similar con la misma o parecida indicación. Por ello, siempre ofrecemos referencias a dichas familias en el proceso de toma de decisiones. Pero el tiempo posterior al trasplante es también un reto especial en este grupo de edad. Por un lado, debido al estrecho margen terapéutico y a los numerosos efectos secundarios de los inmunosupresores, es necesario realizar análisis de sangre muy seguidos, que resultan estresantes para el niño. Inicialmente a diario, luego semanalmente y más tarde a intervalos de 4 semanas. El examen más importante para la detección precoz de una disfunción orgánica es la función pulmonar medida diariamente (en casa). Sin embargo, esto aún no es posible con bebés y niños pequeños. Otras pruebas de control como la frecuencia respiratoria y la saturación de oxígeno son aquí las únicas alternativas (pobres). Debido al alto riesgo de infección, los niños no pueden asistir a la guardería. Esto, a su vez, tiene importantes consecuencias psicosociales para el niño y supone una carga para la familia, especialmente si el niño está siendo criado por un solo progenitor.
A menudo no existe una protección vacunal completa en el momento del trasplante y la respuesta vacunal bajo inmunosupresión es significativamente limitada. Además, las vacunas vivas están contraindicadas en niños después de la Lutx. Esto, a su vez, aumenta el riesgo de infección y requiere medidas preventivas especiales. Lo que tenemos que sufrir dolorosamente en términos de restricciones en el contexto de la pandemia de SRAS-CoV-2 ha sido siempre y sigue siendo la normalidad vivida, especialmente para los niños pequeños, según Lutx. A menudo, debido a las circunstancias mencionadas, las familias se ven en dificultades financieras y por ello necesitan ayuda adicional. Afortunadamente, hemos podido demostrar que la supervivencia de los niños trasplantados en nuestro centro no es, sin embargo, peor que la de los adolescentes, sino que tiende a ser incluso mejor [1]. Además de una posible mayor plasticidad del sistema inmunitario con una tasa menor asociada de rechazos agudos y crónicos (a pesar de una menor inmunosupresión), esto se explica, en mi opinión, principalmente por un cumplimiento terapéutico significativamente mejor (los padres siguen administrando ellos mismos la medicación a esta edad) en comparación con los adolescentes. Sin embargo, el pronóstico gratificantemente bueno con un porcentaje de supervivencia a 5 años superior al 80% [1] también conlleva nuevos retos y obligaciones, a saber, prevenir los daños iatrogénicos a largo plazo siempre que sea posible. Por lo tanto, siempre debe cuestionarse críticamente la necesidad de cada medicamento, cada examen invasivo y cada diagnóstico por imagen con exposición a la radiación o que requiera sedación/anestesia. Además, los estudios controlados sobre la eficacia y la seguridad de los fármacos utilizados en los niños trasplantados de pulmón serían extremadamente importantes, pero desgraciadamente no están disponibles debido al reducido número de pacientes, así como a la falta de interés por parte de la industria farmacéutica y a la falta de financiación pública.
Aspectos específicos para niños en edad preescolar y escolar
Gran parte de lo que se ha mencionado antes sobre los bebés y los niños pequeños también se aplica a los niños en edad preescolar y escolar, por lo que no se vuelve a explicar. Sin embargo, la fibrosis quística es la indicación más común en este grupo de edad. A diferencia de los lactantes y los niños pequeños, los niños mayores rara vez se encuentran en una situación aguda que ponga en peligro su vida en el momento de la inclusión en la lista, lo que permite más tiempo para la discusión y una evaluación adecuada. Además, los niños casi siempre pueden esperar un órgano donado en casa si están en la lista. Sin embargo, a esta edad es importante implicar activamente a los niños en los debates educativos, responder a sus preguntas de forma suficiente y comprensible y, sobre todo, tomar muy en serio sus deseos y temores. Por mi propia experiencia, sé que incluso los niños más pequeños pueden afrontar mucho mejor las complicaciones y los exámenes o tratamientos desagradables tras un trasplante de pulmón si se les ha preparado adecuadamente para ellos antes del trasplante. Muy a menudo tengo la sensación durante las charlas educativas de que los niños no pueden o no quieren verbalizar sus miedos y preocupaciones y que, al igual que los adolescentes, quieren ser “fuertes” para sus padres. Esto hace que el acompañamiento psicológico y la terapia artística sean aún más importantes para estos niños, además de las charlas educativas. Con colores, formas e imágenes, a menudo expresan pensamientos, miedos, expectativas y esperanzas mucho mejor de lo que podrían hacerlo con palabras (Fig. 6) . Además, la terapia con pintura tiene claramente un efecto terapéutico relevante. Por regla general, los niños pueden ir al colegio 6 meses después del trasplante y, aparte de la medicación regular y los controles de seguimiento, apenas hay otras restricciones en su vida cotidiana.

Aspectos específicos con los adolescentes
Los pacientes adolescentes ya están bien situados para comprender la importancia del trasplante de pulmón, con todas las ventajas y desventajas potenciales, y por lo tanto deberían ser los principales interlocutores en las discusiones educativas. Su decisión, ya sea a favor o en contra de un trasplante, es ante todo autorizada y, por lo tanto, debe ser aceptada. A menudo, los adolescentes ya tienen a sus espaldas un largo camino de sufrimiento y no pudieron vivir una infancia despreocupada como la de sus compañeros sanos. Por este motivo, sus expectativas ante un trasplante de pulmón son muy altas. Sin embargo, a menudo no pueden cumplirse en su totalidad. Por lo tanto, es importante transmitir que aunque el trasplante es una oportunidad real de tener una vida más larga y mejor, uno no está sano después y que tomar la medicación con regularidad, someterse a revisiones diarias y evitar comportamientos potencialmente perjudiciales como el consumo excesivo de alcohol o tabaco son extremadamente importantes y, por lo tanto, un requisito básico para la inclusión en la lista de espera. Debe informarse a las niñas de que no deben tener hijos más adelante debido a los efectos secundarios teratogénicos potencialmente graves de los inmunosupresores, y debe garantizarse un asesoramiento ginecológico detallado sobre anticoncepción.
En mi opinión, el cuidado de los adolescentes tras un trasplante de pulmón suele ser mucho más difícil que el de los niños más pequeños. El principal problema, y en mi opinión la causa más común de muerte en este grupo de edad, es la falta de adherencia al tratamiento. A veces los adolescentes invierten más tiempo en “encubrir” las medidas terapéuticas y/o las revisiones que no se han llevado a cabo que en realizarlas de forma coherente. Intuitivamente, esto suele desencadenar en mí ira y frustración (Fig. 7) . Pero estas reacciones no ayudan a las personas afectadas y les facilitan inadecuadamente las cosas al transferirles la responsabilidad. Todos los que tenemos hijos de esta edad sabemos lo difícil, pero también importante, que es la fase de la adolescencia. Se caracteriza por los conflictos de identificación, el deseo de autonomía y autodeterminación y el rechazo interior a los consejos u órdenes de los adultos. Las prohibiciones, las amenazas y los mandamientos tienden a incitar a la gente a hacer lo contrario. Al menos ese fue mi caso durante este tiempo. Además, también está la presión social del grupo de iguales y el deseo de “pertenecer”, incluso cuando se trata de poner a prueba los límites y las cosas prohibidas. La forma en que los jóvenes se enfrentan a esto, por supuesto, también depende en gran medida del apoyo y la integridad del entorno social. Por lo tanto, nuestra tarea consiste en comunicar bien estos temas en el contexto de la educación, establecer una relación de confianza y, con la ayuda de los padres, psicólogos y trabajadores sociales, identificar los puntos conflictivos lo antes posible y encontrar soluciones individualizadas a la altura de los pacientes adolescentes.

Por último, me gustaría abordar la importante cuestión de la transición. Los jóvenes deben ser preparados intensivamente para el tiempo como paciente “adulto” a partir de los 16 años como muy tarde. En mi opinión, la bienintencionada atención orientadora y la reducción de tareas y responsabilidades son errores que los pediatras seguimos cometiendo con demasiada frecuencia, sobre todo con los pacientes crónicos. Tenemos que ser conscientes de que no estamos fomentando la independencia de los pacientes. Por esta razón, un programa de transición estructurado es importante para el curso a largo plazo más allá de los 18 años.
Resumen
El trasplante de pulmón ofrece a niños y jóvenes, independientemente de su edad, la oportunidad de una vida más larga y mejor. Sin embargo, también se asocia a complicaciones y compromisos de por vida que son muy diferentes de una vida normal y exigen mucho de los pacientes y sus familias. Por lo tanto, una evaluación detallada, una educación exhaustiva, la consiguiente identificación selectiva de los candidatos adecuados y una atención multidisciplinar antes y después del trasplante son siempre indispensables. La atención individualizada al paciente que se requiere para ello requiere mucho tiempo y personal. Esto no se tiene suficientemente en cuenta en el sistema sanitario actual. Para mejorar la supervivencia a largo plazo, así como la calidad de vida de los niños que se nos confían, no debemos cansarnos de luchar contra ello.
Mensajes para llevarse a casa
- La edad media en el momento del trasplante oscila entre los 12 y los 15 años, la fibrosis quística (FQ) es la indicación más común con cerca del 60%, seguida de la hipertensión arterial pulmonar (HAP).
- Cada fase de la vida antes y después del trasplante de pulmón conlleva unos retos médicos y psicosociales particulares que pueden diferir de forma interindividual, pero que es esencial tener en cuenta.
- Una atención psicosocial cercana e individualizada para los niños trasplantados y sus familiares es extremadamente importante.
- La falta de adherencia al tratamiento en adolescentes tras un trasplante de pulmón es un factor de riesgo importante para el rechazo crónico del órgano.
- Entre las consecuencias graves a largo plazo del tratamiento inmunosupresor se encuentran la insuficiencia renal grave (aprox. 6%), la diabetes mellitus (aprox. 30%) y los tumores malignos (aprox. 10%). Los pacientes pediátricos contraen predominantemente linfomas asociados al VEB.
- Una de las principales razones del mal pronóstico en comparación con otros trasplantes de órganos sólidos es probablemente la exposición significativamente mayor del pulmón al medio ambiente, con la consiguiente estimulación constante del sistema inmunológico.
Literatura:
- Iablonskii P, Carlens J, Mueller C, et al: Indicaciones y resultados tras el trasplante de pulmón en niños menores de 12 años: Una experiencia de 16 años en un único centro. J Heart Lung Transplant 2021 Oct 28.
- Schmid FA, Inci I, Burgi U, et al: Resultados favorables de los niños y adolescentes sometidos a trasplante de pulmón en un centro europeo de adultos en la nueva era. Pediatr Pulmonol 2016; 5(11): 1222-1228.
- Khush KK, Cherikh WS, Chambers DC, et al: The International Thoracic Organ Transplant Registry of the International Society for Heart and Lung Transplantation: Thirty-sixth adult heart transplantation report – 2019; focus theme: Donor and recipient size match. J Heart Lung Transplant 2019; 38(10): 1056-1066.
- Hayes D Jr AD, The International Society for Heart and Lung Transplantation – International Thoracic Organ Transplant Registry, Dallas,Texas, Harhay MO, et al: The International Thoracic Organ Transplant Registry of the International Society for Heart and Lung Transplantation: Twenty-fourth pediatric lung transplantation report – 2021; Focus on recipient characteristics. J Heart Lung Transplant 2021; 40(10): 1023-1034.
- Leard LE, Holm AM, Valapour M, et al: Documento de consenso para la selección de candidatos a trasplante de pulmón: Una actualización de la Sociedad Internacional de Trasplante de Corazón y Pulmón. J Heart Lung Transplant 2021; 40(11): 1349-1379.
- Solomon M, Mallory GB.: Remisiones para trasplante de pulmón en individuos con fibrosis quística: Una perspectiva pediátrica sobre las directrices de consenso de la fundación de fibrosis quística. Pediatr Pulmonol 2021; 56(2): 465-471.
- Huddleston CB: Trasplante pulmonar para la hipertensión pulmonar en niños. Pediatr Crit Care Med 2010; 11(2 Suppl): S53-S56.
- Tudorache I, Sommer W, Kuhn C, et al: Trasplante pulmonar para la hipertensión pulmonar grave – oxigenación con membrana extracorpórea despierto para el remodelado ventricular izquierdo postoperatorio. Trasplantes 2015; 99(2): 451-458.
- Goldfarb SB, Hayes DJ, Levvey BJ, et al: The International Thoracic Organ Transplant Registry of the International Society for Heart and Lung Transplantation: Twenty-first Pediatric Lung and HeartLung Transplantation Report-2018; Focus Theme: Multiorgan Transplantation. J Heart Lung Transplant 2018; 37(10): 1196-1206.
- Verleden GM, Raghu G, Meyer KC, et al: Un nuevo sistema de clasificación para la disfunción crónica del aloinjerto pulmonar. J Heart Lung Transplant 2014; 33(2): 127-133.
- Khan MS, Zhang W, Taylor RA, et al: Supervivencia en el trasplante pediátrico de pulmón: El efecto del volumen y la experiencia del centro. J Heart Lung Transplant 2015; 34(8): 1073-1081.
- Gorler H, Struber M, Ballmann M, et al: Trasplante pulmonar y cardiopulmonar en niños y adolescentes: una experiencia unicéntrica a largo plazo. J Heart Lung Transplant 2009; 28(3): 243-248.
InFo NEUMOLOGÍA Y ALERGOLOGÍA 2022; 4(1): 12-18