En la reunión anual de la ASCO de este año se presentaron algunos estudios apasionantes sobre el carcinoma de células renales. Especialmente en el caso de los tumores localizados, la práctica clínica podría cambiar en un futuro próximo. Por primera vez, los inhibidores de los puntos de control parecen ser una opción eficaz para la terapia adyuvante. Y también hay nuevos hallazgos en el tratamiento de primera y segunda línea del carcinoma avanzado de células renales.
Durante años, la investigación ha buscado posibles terapias adyuvantes para el carcinoma de células renales, hasta ahora sin éxito. Desgraciadamente, no se pudo lograr ningún avance mediante el uso de inhibidores de la tirosina quinasa. Por ejemplo, hay una serie de estudios que no mostraron ningún beneficio o sólo un beneficio mínimo en la supervivencia del tratamiento adyuvante con sunitinib, sorafenib, pazopanib y axitinib – con una toxicidad considerable [1–5]. En la reunión anual de la ASCO, Keynote-564 fue el primer estudio en presentar un tratamiento adyuvante prometedor tras una nefrectomía. Esto podría cambiar pronto la práctica clínica para siempre. Actualmente, sólo se recomienda el seguimiento del tumor tras la nefrectomía, independientemente del tamaño y la graduación del tumor. Sin embargo, se sabe desde hace tiempo que estos factores tienen una influencia significativa en el pronóstico [6]. Por tanto, es lógico que especialmente los pacientes del grupo de alto riesgo -por ejemplo, los que presentan tumores sarcomatoides desdiferenciados o de gran tamaño- puedan beneficiarse de un tratamiento adyuvante tras la nefrectomía.
Terapia adyuvante: centrada en los inhibidores de puntos de control
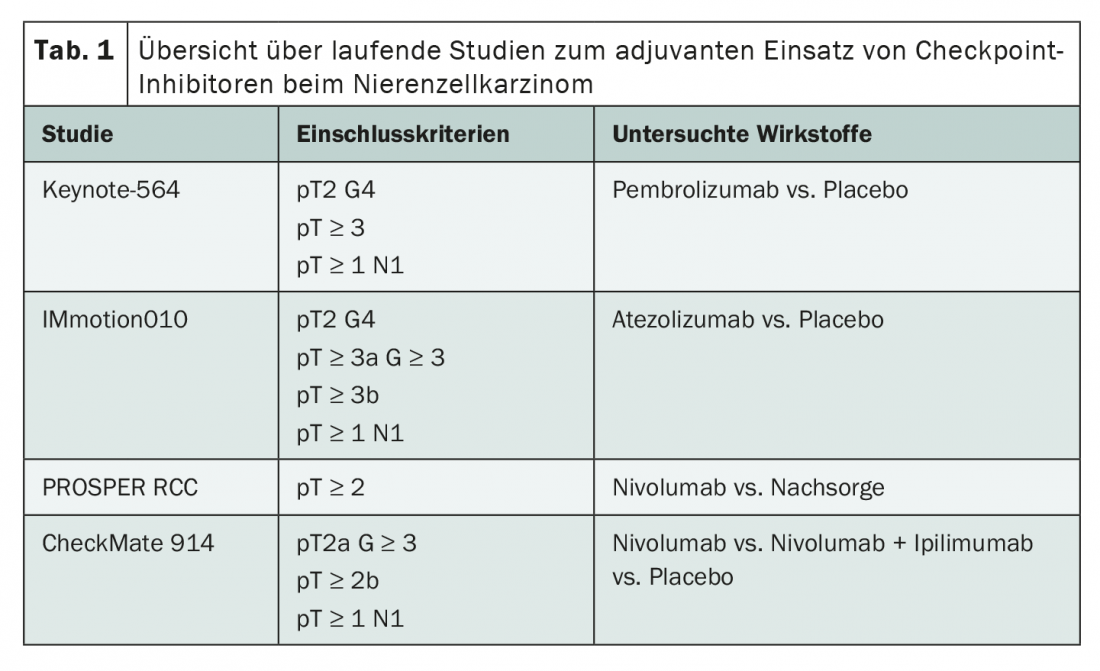
Mientras que en el transcurso de la última década se investigaron principalmente los inhibidores de la tirosina quinasa en el contexto adyuvante, la atención se centra ahora en la inmunoterapia mediante inhibidores de los puntos de control. Actualmente, hay cuatro ensayos en marcha que investigan el uso de pembrolizumab, atezolizumab y nivolumab como monoterapia o en combinación con ipilimumab (tab. 1). Aunque los criterios de inclusión fueron ligeramente diferentes en todos los estudios, siempre se centran en los pacientes de los grupos de riesgo intermedio y alto. Una característica especial tanto del estudio Keynote 564 como del estudio IMmotion010 es que también se pudo incluir a pacientes tras una cirugía metastásica con éxito dentro del primer año tras el diagnóstico primario.
Los resultados iniciales de Keynote-564 ya se han presentado en la reunión anual de la ASCO [7]. En el estudio de fase III, los pacientes incluidos recibieron pembrolizumab o placebo durante un año tras la nefrectomía. La mediana de seguimiento fue de 24,1 meses. Tanto la supervivencia libre de enfermedad (SLE) como la supervivencia global (SG) mostraron ventajas estadísticamente significativas del tratamiento adyuvante con pembrolizumab, a pesar del periodo de seguimiento aún relativamente corto. Así, la tasa de SSE a los 24 meses fue del 77,3%, frente al 68,1% en el brazo de control (cociente de riesgos 0,68; p=0,001). La tasa de SG a los 24 meses fue del 96,6% en el grupo de intervención y del 93,5% con placebo (cociente de riesgos 0,54, p=0,0164). Estos efectos estuvieron presentes y fueron similares en todos los subgrupos. Los pacientes que se habían sometido previamente a una metastasectomía con éxito parecían beneficiarse especialmente de la inmunoterapia adyuvante. No hubo sorpresas en cuanto a la compatibilidad. Como cabía esperar de los estudios en monoterapia, se produjeron efectos secundarios graves en aproximadamente el 20% de los pacientes, lo que se correspondía con el espectro conocido de efectos secundarios del pembrolizumab. Quedan por ver datos más maduros del ensayo Keynote 564, así como los resultados iniciales de los demás ensayos de inmunoterapia, para evaluar los efectos reales del tratamiento. Sin embargo, tras muchos años sin éxito, ahora podría surgir una opción para la terapia adyuvante del carcinoma de células renales, especialmente para los pacientes de alto riesgo.
Carcinoma avanzado de células renales: terapia de primera línea en transición
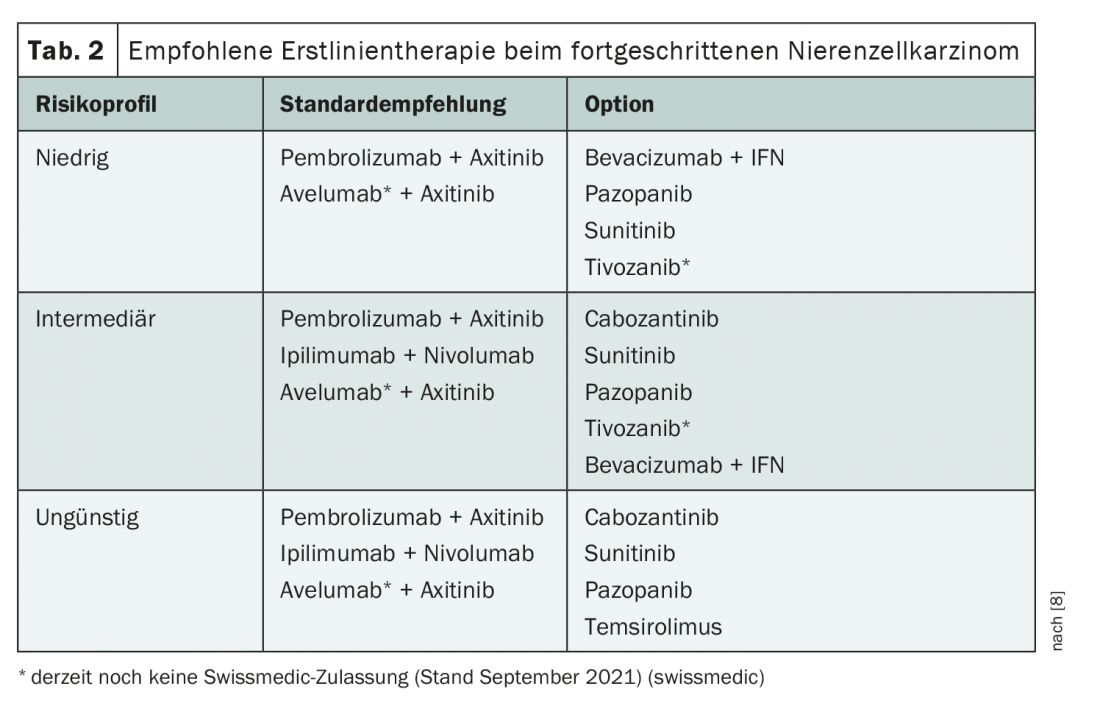
En la reunión anual de la ASCO también se presentaron varios hallazgos en el campo de la terapia de primera línea para el carcinoma avanzado de células renales. Con la introducción de varias terapias combinadas de inmunoterapéuticos e inhibidores de la tirosina quinasa, el tratamiento está en pleno cambio. Actualmente, se recomiendan diferentes terapias en función del perfil de riesgo (Tab. 2) [8]. Recientemente, también se aprobó el cabozantinib, un inhibidor de la tirosina quinasa (ITC) de tercera generación, en combinación con nivolumab para el tratamiento de primera línea; esta opción aún no se contempla en las directrices. También existe una buena base de datos para el tratamiento con lenvatinib + pembrolizumab, aunque la aprobación aún está pendiente [9,10]. Actualmente, el lenvatinib sólo está aprobado en Suiza para la terapia de segunda línea tras los inhibidores del VEGF [11].
Entre las diferentes opciones, la atención se centra actualmente en la cuestión de si las combinaciones TKI-inmunoterapéuticas (IO) también pueden mantenerse a largo plazo con la combinación IO-IO nivolumab/ipilimumab, para la que ya existe un periodo de seguimiento más largo. Hasta ahora, los datos de las combinaciones nivolumab/ipilimumab, axitinib/pembrolizumab, cabozantinib/nivolumab y también de la combinación aún no aprobada lenvatinib/pembrolizumab muestran resultados similares en cuanto a la supervivencia con un cociente de riesgos instantáneos de aproximadamente 0,66 en comparación con la monoterapia con sunitinib [9,12–16]. Sin embargo, falta un seguimiento a más largo plazo para las combinaciones IO-TKI. Se presentó uno para axitinib/pembrolizumab en la reunión anual de la ASCO de este año [15]. Las tasas de SG y SLP en los distintos puntos temporales fueron similares a las de los ensayos de la combinación IO-IO nivolumab/ipilimumab. Después de 36 meses, la tasa de SLP con ambas terapias era de alrededor del 30% [14,15]. Se trata sin duda de una buena noticia, pero aún quedan por ver más datos sobre la duración de la respuesta. La conclusión es que el seguimiento de la combinación TKI-IO axitinib/pembrolizumab muestra datos consistentes hasta el momento sin nuevas preocupaciones de seguridad.
Además, en la reunión anual de la ASCO se presentaron datos sobre las nuevas combinaciones TKI-IO lanvatinib/pembrolizumab y cabozantinib/nivolumab. Mientras que éstos son claramente superiores al tratamiento con sunitinib solo en pacientes de riesgo intermedio y alto, los pacientes con perfiles de riesgo favorables han mostrado hasta ahora una prolongación significativa de la SLP pero sin efecto sobre la SG [10,17]. Esto podría deberse al periodo de seguimiento relativamente corto, pero indica que el beneficio de la estrategia dual es potencialmente mayor en los grupos de riesgo intermedio y alto que en la población de bajo riesgo. Si las combinaciones con TKIs de tercera generación sustituirán a otras combinaciones TKI-IO en el futuro -por ejemplo, las realizadas con axitinib- sigue siendo una cuestión abierta en la actualidad.
Noticias de la segunda línea
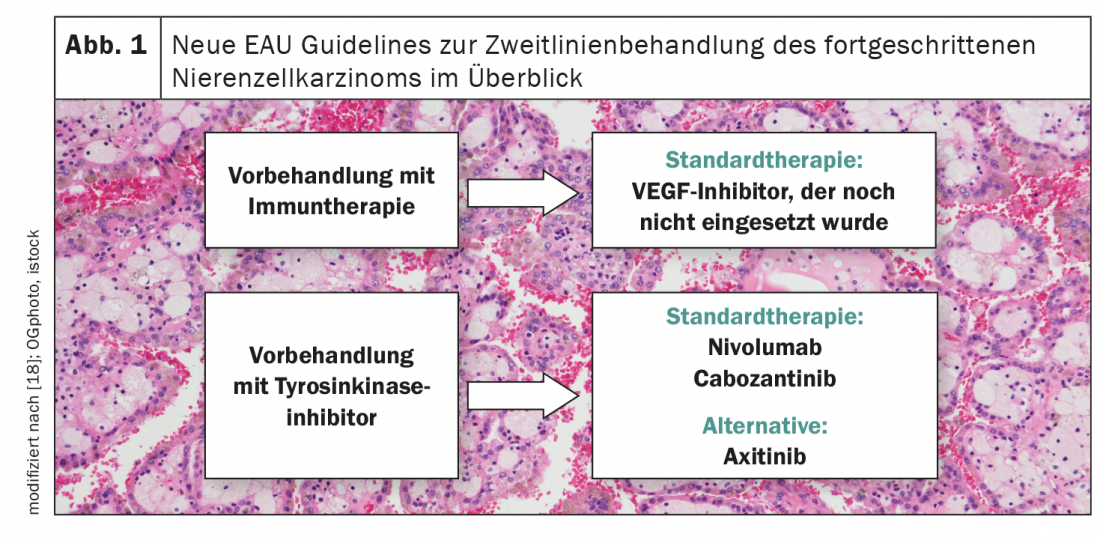
Tras el fracaso de la terapia de primera línea, siguen faltando recomendaciones sólidas en el carcinoma de células renales, especialmente si se utilizaron inmunoterapéuticos en la primera línea de tratamiento (Fig. 1) [18]. Hasta ahora, existen tres estudios prospectivos en este ámbito, todos de un solo brazo. Mientras que se observó una mediana de SLP de 8,8 meses con el tratamiento con axitinib, ésta fue de 7,4 meses con la terapia con pazopanib y de 6,8 meses con la administración de sunitinib [19-21]. El estudio CANTATA presentado en la Reunión Anual de la ASCO investigó la eficacia de cabozantinib/telaglenastat en el contexto de segunda línea y comparó esta terapia combinada con cabozantinib/placebo [22]. Aunque no se observó ningún beneficio al añadir telaglenastat, el cabozantinib demostró ser un candidato prometedor para la terapia de segunda línea del carcinoma avanzado de células renales. Así, la mediana de la SLP en el brazo de control fue de 9,3 meses con una tasa de respuesta objetiva de alrededor del 30%.
Congreso: Reunión anual de la ASCO
Literatura:
- Ravaud A, et al: Sunitinib adyuvante en el carcinoma de células renales de alto riesgo tras nefrectomía. N Engl J Med. 2016; 375(23): 2246-2254.
- Eisen TQG, et al: Resultados del análisis de eficacia primaria del ensayo SORCE (RE05): Sorafenib adyuvante para el carcinoma de células renales con riesgo intermedio o alto de recaída: un ensayo internacional aleatorizado doble ciego de fase III dirigido por la UAT del MRC en la UCL. Congreso ESMO 2019, Proffered Paper 2 – Tumores genitourinarios, no prostáticos, Abstract #2483.
- Motzer RJ, et al: Ensayo aleatorizado de fase III de pazopanib adyuvante frente a placebo tras nefrectomía en pacientes con carcinoma de células renales localizado o localmente avanzado. J Clin Oncol. 2017; 35(35): 3916-3923.
- Haas NB, et al: Adjuvant sunitinib or sorafenib for high-risk, non-metastatic renal-cell carcinoma (ECOG-ACRIN E2805): a double-blind, placebo-controlled, randomised, phase 3 trial. Lancet. 2016; 387(10032): 2008-2016.
- Gross-Goupil M, et al: Axitinib frente a placebo en pacientes con alto riesgo de carcinoma de células renales (CCR) recurrente: Resultados del ensayo ATLAS. Congreso ESMO 2018, Proffered paper session – Tumores genitourinarios, no prostáticos, Abstract #1286.
- Gettman MT, et al: Estadificación patológica del carcinoma de células renales: importancia de la clasificación del tumor con el sistema de estadificación TNM de 1997. Cáncer. 2001; 91(2): 354-361.
- Choueiri TK, et al: Pembrolizumab frente a placebo como tratamiento adyuvante tras nefrectomía en pacientes con carcinoma de células renales: Estudio KEYNOTE-564 aleatorizado, doble ciego y de fase III. Reunión anual de la ASCO 2021, Resumen #LBA5.
- AWMF: S3-Leitlinie Diagnostik, Therapie und Nachsorge des Nierenzellkarzinoms, Langversion 2.0, Stand August 2020.
- Motzer R, et al: Lenvatinib más pembrolizumab o everolimus para el carcinoma avanzado de células renales. N Engl J Med. 2021; 384(14): 1289-1300.
- Grünwald V, et al.: Análisis del estudio CLEAR en pacientes (pts) con carcinoma avanzado de células renales (CCR): Profundidad de la respuesta y eficacia para subgrupos seleccionados en los brazos de tratamiento con lenvatinib (LEN) + pembrolizumab (PEMBRO) y sunitinib (SUN). Reunión anual de la ASCO 2021, resumen nº 4560.
- www.swissmedicinfo.ch (última consulta: 15.09.2021)
- Albiges L, et al.: Nivolumab más ipilimumab frente a sunitinib para el tratamiento de primera línea del carcinoma avanzado de células renales: seguimiento ampliado a 4 años del ensayo de fase III CheckMate 214. ESMO Open. 2020; 5(6): e001079.
- Choueiri TK, et al: Nivolumab + cabozantinib frente a sunitinib en el tratamiento de primera línea del carcinoma avanzado de células renales: Primeros resultados del ensayo aleatorizado de fase III CheckMate 9ER. Anales de Oncología. 2020; 31: S1142-1215.
- Motzer RJ, et al: Resultados de supervivencia y evaluación independiente de la respuesta con nivolumab más ipilimumab frente a sunitinib en pacientes con carcinoma avanzado de células renales: seguimiento durante 42 meses de un ensayo clínico aleatorizado de fase 3. J Immunother Cancer. 2020; 8(2).
- Rini BI, et al: Pembrolizumab (pembro) más axitinib (axi) frente a sunitinib como tratamiento de primera línea para el carcinoma avanzado de células renales claras (CCRc): Resultados del seguimiento de 42 meses de KEYNOTE-426. Reunión anual de la ASCO 2021, resumen nº 4500.
- Plimack ER, et al: Pembrolizumab más axitinib frente a sunitinib como tratamiento de primera línea para el carcinoma avanzado de células renales (CCR): Análisis actualizado de KEYNOTE-426. Journal of Clinical Oncology. 2020; 38(15_suppl).
- Apolo AB, et al: Nivolumab más cabozantinib (N+C) frente a sunitinib (S) para el carcinoma avanzado de células renales (aRCC): Resultados según las características basales de la enfermedad en el ensayo de fase 3 CheckMate 9ER. Reunión anual de la ASCO 2021, resumen nº 4553.
- Ljungberg B, et al.: Directrices de la EAU: Carcinoma de células renales 2021. https://uroweb.org/guideline/renal-cell-carcinoma/ (última consulta: 15.09.2021).
- Ornstein MC, et al: Régimen individualizado de axitinib para pacientes con carcinoma metastásico de células renales tras el tratamiento con inhibidores de puntos de control: un estudio multicéntrico, de un solo brazo, de fase 2. Lancet Oncol. 2019; 20(10): 1386-1394.
- Powles TB, et al: Estudio de fase II de pacientes con carcinoma de células renales (CCRm) avanzado o metastásico que reciben pazopanib tras un tratamiento previo con inhibidores de puntos de control. Anales de Oncología. 2020; 31: S564.
- Grande E, et al: Ensayo INMUNOSUN-SOGUG: Un estudio prospectivo de fase II para evaluar la eficacia y la seguridad del sunitinib como tratamiento de segunda línea (2L) en pacientes (pts) con cáncer de células renales (CCR) metastásico que recibieron una combinación basada en inmunoterapia por adelantado. Revista de Oncología Clínica. 2020; 38(15_suppl).
- Tannir NM, et al: CANTATA: Análisis primario de un ensayo global, aleatorizado, controlado con placebo (Pbo) y a doble ciego de telaglenastat (CB-839) + cabozantinib frente a Pbo + cabozantinib en pacientes (pts) con carcinoma de células renales avanzado/metastásico (CCRm) que progresaron con inhibidores de puntos de control inmunitarios (ICI) o terapias antiangiogénicas. Reunión anual de la ASCO 2021, resumen nº 4501.
InFo ONCOLOGÍA Y HEMATOLOGÍA 2021; 9(4): 33-34