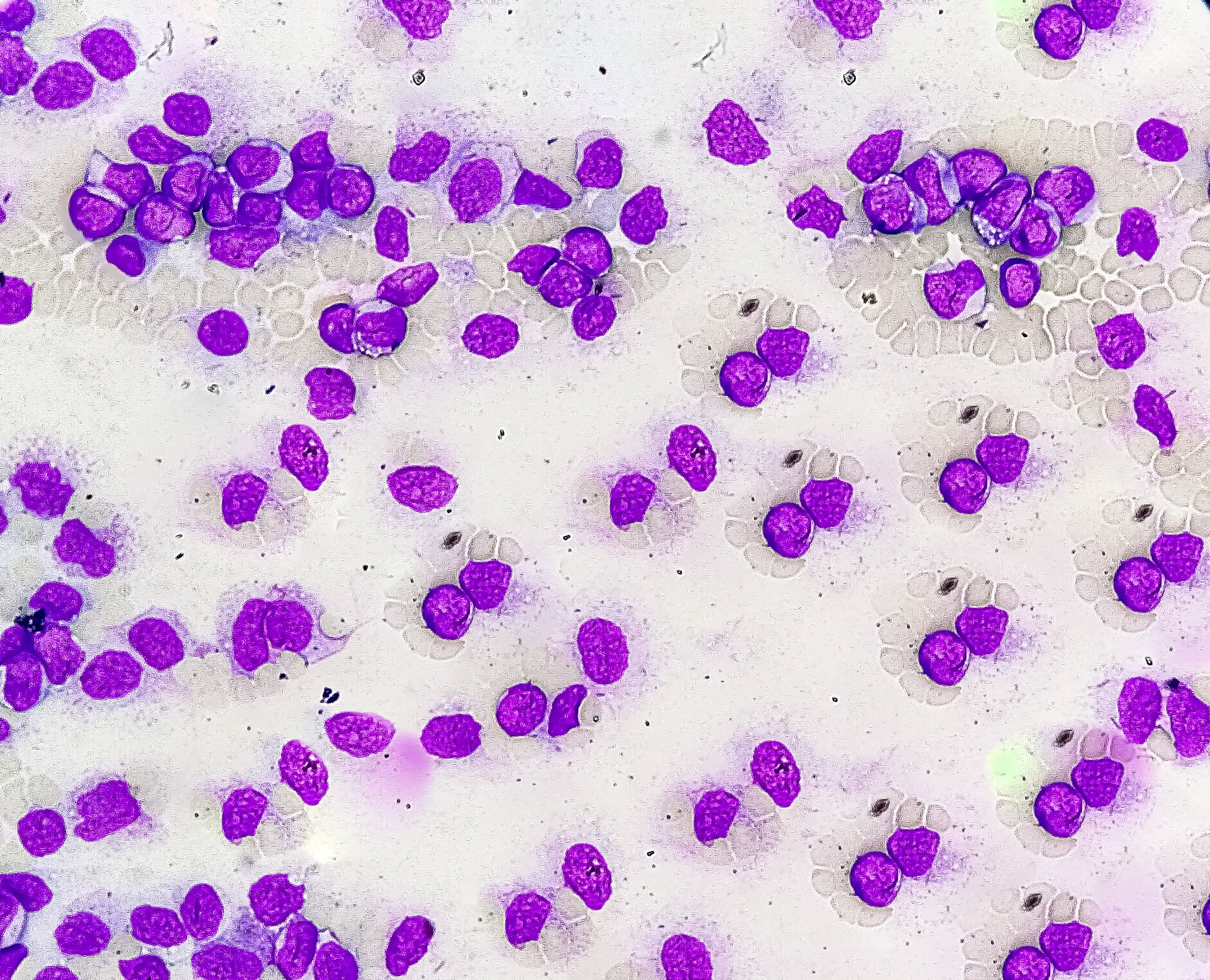
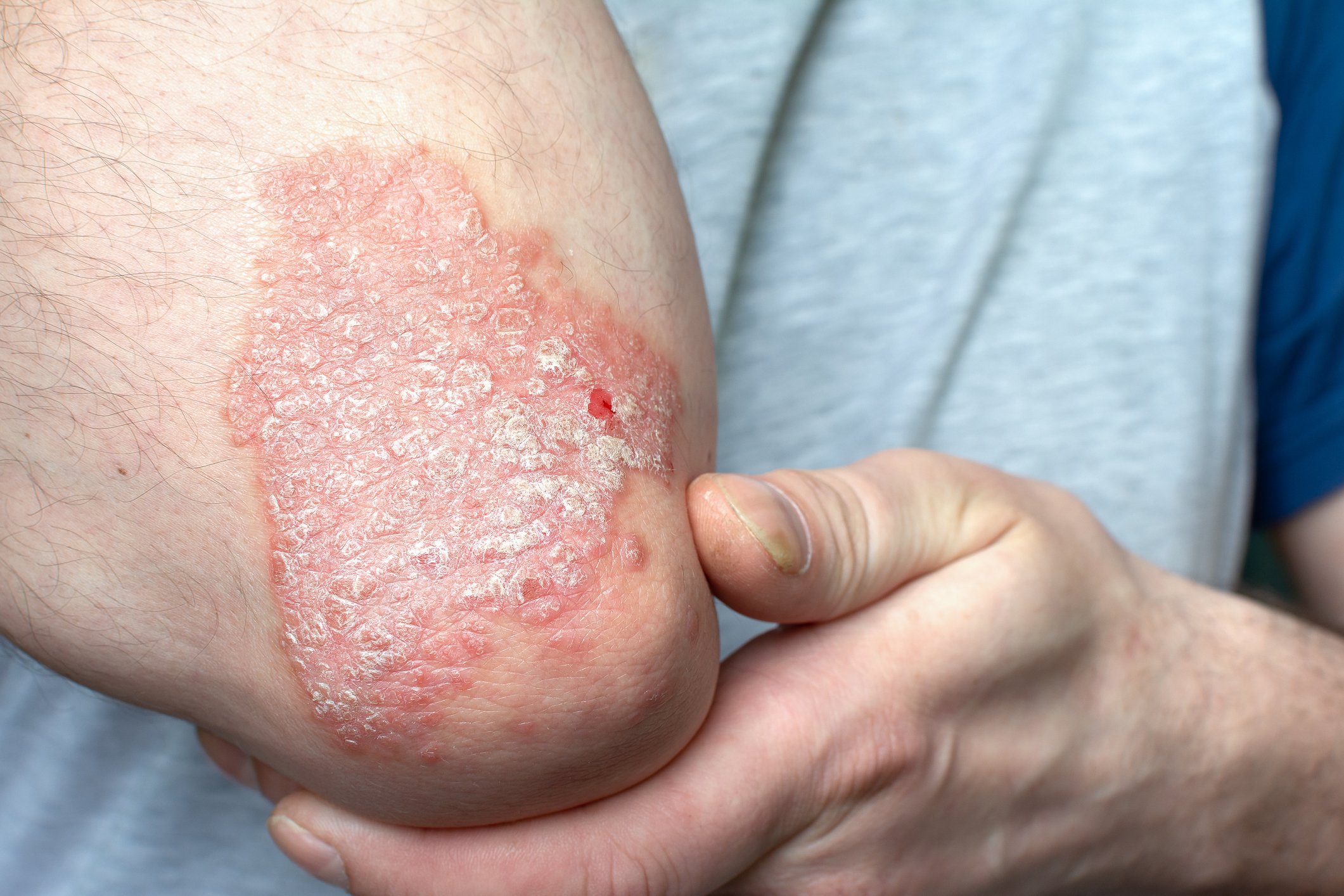
Es en gran parte desconocida: la cistitis intersticial. Sin embargo, la inflamación crónica no infecciosa de la pared vesical se asocia a síntomas dolorosos, enfermedades concomitantes y estrés psicológico.
La primera directriz sobre el diagnóstico y el tratamiento de la cistitis intersticial está en vigor desde otoño de 2018 [1]. Está dirigido a médicos generalistas, urólogos, ginecólogos, internistas, terapeutas del dolor y psicosomáticos y pretende contribuir a una mejor calidad de la atención a los afectados.
Alto número de casos no denunciados
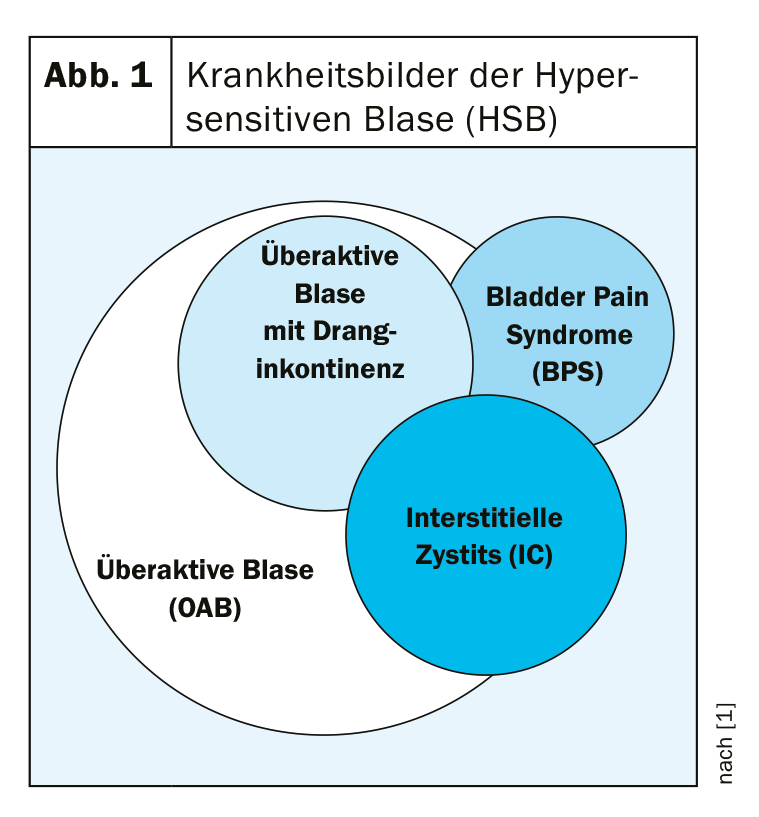
Aunque no existe una definición válida a nivel mundial, se entiende por cistitis intersticial (CI) una inflamación crónica no infecciosa de la vejiga urinaria, que se manifiesta sintomáticamente con dolor, polaquiuria y nicturia. Los síntomas se presentan en diversos grados y combinaciones. El diagnóstico de síndrome de dolor vesical (SDV) no es suficiente en este caso, ya que se centra demasiado en el dolor, lo que no hace justicia al cuadro clínico de la CI. Sin embargo, debido a la a veces estrecha superposición de diferentes cuadros clínicos, no es tan fácil distinguir la CI de otras enfermedades de la vejiga (Fig. 1).
En principio, la CI puede darse en cualquier grupo de edad, encontrándose la mayor prevalencia en personas de mediana edad. Las mujeres se ven afectadas unas nueve veces más que los hombres. Sin embargo, como faltan estudios epidemiológicos, no existen datos precisos. El número de casos no denunciados es elevado.
Tampoco está claro cómo se crea un CI en primer lugar. Se discuten diversos factores etiopatogénicos. La atención se centra en los posibles daños al urotelio: las infecciones frecuentes de la vejiga modifican la capa de glicosaminoglicanos, la permeabilidad de la vejiga urinaria y la homeostasis urotelial. Como resultado, las sustancias irritantes de la orina penetran en la submucosa y en las capas más profundas de la pared de la vejiga urinaria. Este proceso destructivo puede llevar incluso a la pérdida del urotelio. La mucosa vesical defectuosa provoca una mayor sensibilidad y dolor en la vejiga.
El maratón de médicos intensifica el sufrimiento
Los pacientes afectados pueden tardar hasta nueve años en ser diagnosticados de CI. Los diagnósticos erróneos no son infrecuentes, sobre todo en las primeras fases de la enfermedad. Este maratón de médicos es estresante y puede hacer que los afectados se sientan mal, se sientan solos e incluso desarrollen una depresión. Para empeorar las cosas, los pacientes con CI suelen padecer enfermedades concomitantes como fatiga, síndrome del intestino irritable, fibromialgia, trastornos psicológicos y otras dolencias neurológicas, somáticas funcionales o reumáticas.
Por ello es aún más importante que ahora exista un consenso sobre cómo diagnosticar y tratar la CI con la directriz S2k de la Sociedad Urológica Alemana.
¿Cómo diagnosticar?
Al igual que con otras enfermedades, la directriz S2k recomienda iniciar el diagnóstico con una anamnesis exhaustiva. Cuestionarios como el índice ICSI/ICPI (frecuencia miccional, molestias de la vejiga urinaria), el cuestionario PUF (dypareunia, dolor pélvico) y la puntuación de los síntomas de dolor de vejiga/IC (BPIC-SS) sirven de apoyo. También son útiles las hojas de documentación en forma de diario del dolor o de registro de micciones. El examen físico se centra en la zona genital. Además, debe tomarse una muestra de orina. Los exámenes adicionales incluyen la urosonografía, la cistoscopia y, en los hombres, la uroflujometría. Si es necesario, se puede considerar la hidrodistensión, un EMG de flujo o una prueba de cloruro potásico para provocar un aumento de la sensibilidad al dolor. Una biopsia de la pared de la vejiga no es decisiva para el diagnóstico, pero también debe considerarse. Sin embargo, como los mastocitos están implicados en diversos procesos inflamatorios, este método no es concluyente para determinar un CI. Otra opción de medicina complementaria es una muestra de heces, que proporciona información sobre la flora intestinal. Actualmente no se conocen biomarcadores, aunque se está investigando en este sentido.
El diagnóstico también incluye la exclusión de toda una serie de diagnósticos diferenciales. Entre ellas se incluyen:
- Enfermedades musculoesqueléticas (por ejemplo, disfunción del suelo pélvico, fibromialgia, hernias, dolor de espalda crónico, neoplasias malignas)
- Enfermedades gastrointestinales (por ejemplo, EII, síndrome del intestino irritable, estenosis del intestino delgado y grueso, neoplasias malignas)
- Enfermedades ginecológicas (por ejemplo, endometriosis/adenomiositis, varicosis pélvica, estenosis cervical)
- Enfermedades urológicas (por ejemplo, disfunción de la vejiga, inflamación crónica de las vías urinarias, prostatitis, neoplasias malignas)
- Causas neurogénicas (por ejemplo, herpes genital, neuralgia, varicela zoster)
- Trastornos mentales (por ejemplo, trastornos afectivos, esquizofrénicos, somatomorfos)
¡Tratamiento multimodal!
La CI no es curable. Sin embargo, se puede ralentizar la progresión de la enfermedad y aliviar los síntomas. La terapia adecuada debe ser interdisciplinar y multimodal, teniendo en cuenta los aspectos biopsicosociales (Fig. 2). El primer paso es un cambio en el estilo de vida. El vestuario, la sexualidad y los deportes deben organizarse de forma que no se produzca un empeoramiento de los síntomas. El estrés y el frío tienen un efecto negativo, mientras que se dice que el entrenamiento de la vejiga tiene cierta eficacia. Dado que las intolerancias alimentarias se asocian a menudo con los síntomas de IC/BPS, debe prestarse especial atención a la dieta. Por su bajo contenido en histamina, son preferibles los alimentos no fermentados, fermentados o madurados microbiológicamente. Al igual que en el caso del SII, una dieta baja en FODMAP puede resultar útil. Los síntomas psicosomáticos deben aliviarse mediante atención psicológica o psiquiátrica, en la que el entorno social del paciente también desempeña un papel importante. La disfunción del suelo pélvico, frecuente en la CI, puede tratarse con fisioterapia.
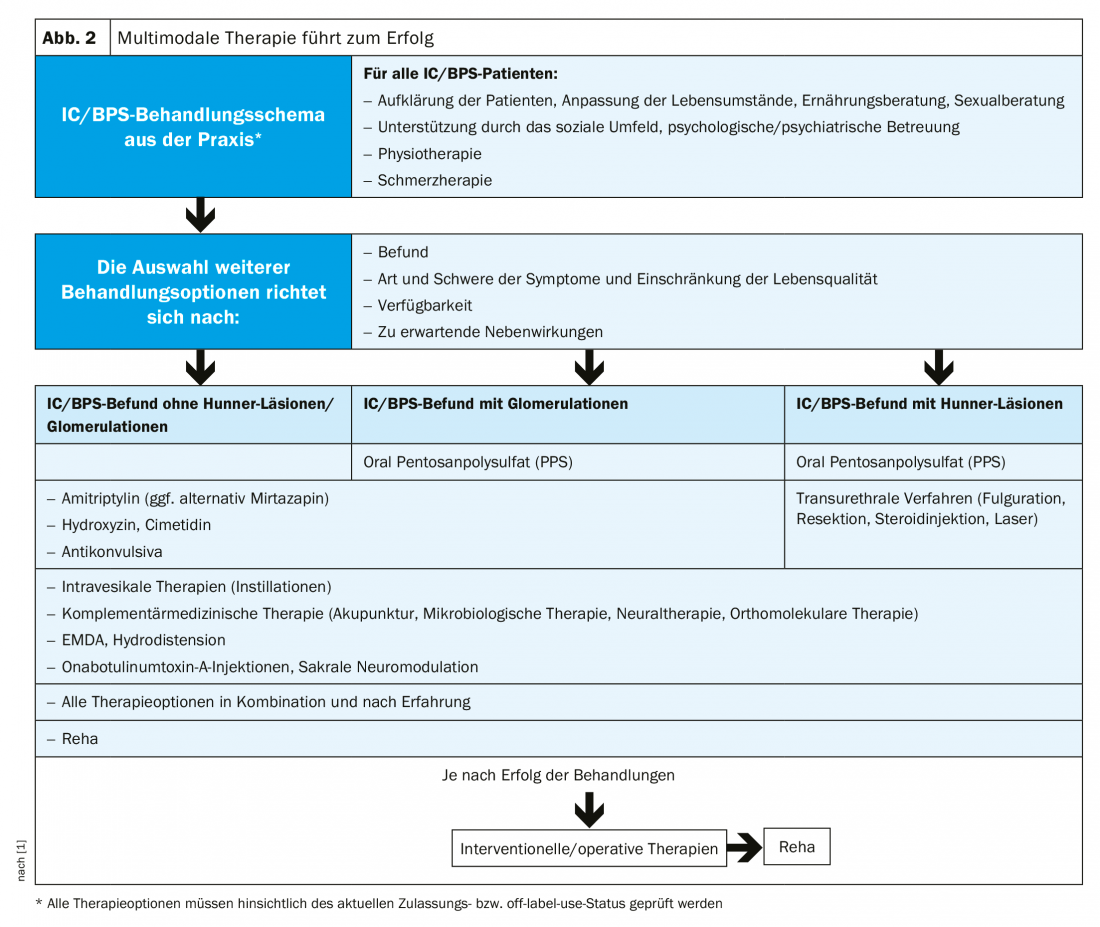
Actualmente, sólo el polisulfato de pentosán (PPS) está aprobado como tratamiento farmacológico oral para la CI en Europa. El principio activo repara la capa de glicosaminoglicanos del urotelio, impidiendo que penetren sustancias tóxicas o irritantes para la pared de la vejiga urinaria. El SPP también favorece el flujo sanguíneo a la vejiga urinaria. El efecto suele producirse al cabo de tres a seis meses, por lo que se aplica lo siguiente: ¡cuanto antes comience la terapia, mejor!
Fuera de indicación, pueden considerarse otros agentes. La amitriptilina, al inhibir la recaptación de serotonina/norepinefrina, modifica la transmisión del dolor en el SNC y reduce la activación de los mastocitos, lo que se traduce en una reducción de la micción y del dolor. Una alternativa a la amitriptilina es el antidepresivo tetracíclico mirtazapina, que – a diferencia de la amitriptilina – no tiene efectos secundarios anticolinérgicos. La hidroxizina también inhibe la activación de los mastocitos y tiene efectos anticolinérgicos, ansiolíticos y analgésicos. Los estudios mostraron una reducción del dolor y la nicturia en pacientes con CI tratados con el antagonista de los receptores de histamina-2 cimetidina. Este efecto puede explicarse por el hecho de que la cimetidina inhibe la sobreexpresión de los receptores H1 y H2, los receptores purinérgicos P2X y los receptores colinérgicos muscarínicos observados en el CI. El montelukast, que está aprobado para el asma, también mostró su efecto en el CI en un pequeño estudio al reducir la inflamación inducida por los mastocitos. Los inhibidores de la fosfodiesterasa-5 (PDE5) tienen un efecto relajante sobre las células musculares lisas de la vejiga urinaria, aunque la causa de su acción aún no está clara. El antagonista de los canales de calcio nifedipino también resultó eficaz en el tratamiento de la CI. Sin embargo, aún faltan estudios prospectivos aleatorios.
La directriz S2k también recomienda una terapia adecuada contra el dolor. Hay que aliviar el dolor de los pacientes y evitar el uso irreflexivo de analgésicos poco eficaces. En la actualidad, no existe un consenso sobre el tratamiento de la CI, pero los expertos se refieren a diferentes grupos de fármacos que también pueden utilizarse en combinación. Dependiendo de la gravedad y de la respuesta del paciente, pueden utilizarse AINE, anticonvulsivos, sulfona de novamina y opiáceos.
Además, es posible el uso de relajantes musculares (por ejemplo, tizanidina), alfabloqueantes (por ejemplo, tamsulosina) y anticonvulsivos (por ejemplo, pregabalina).
Los efectos secundarios sistémicos pueden eludirse mediante formas intravesicales de tratamiento. Sin embargo, las desventajas de esta terapia, en la que se introducen altas concentraciones de sustancias activas directamente en la vejiga urinaria, son el riesgo de infección, el carácter invasivo y los elevados costes.
Los procedimientos de medicina complementaria como la acupuntura, la terapia neural, las terapias microbiológicas o la sustitución de micronutrientes son otra opción. Si ninguna de las terapias tiene éxito, la cirugía es la única opción. Una medida de acompañamiento es siempre el tratamiento en centros especializados de rehabilitación urológica. En última instancia, el objetivo sigue siendo proteger al enfermo de CI de la amenaza de la incapacidad laboral y/o el aislamiento social.
Literatura:
- Sociedad Alemana de Urología, ed.: S2k-Leitlinie Diagnostik und Therapie der Interstitiellen Cystitis (IC/BPS), Langfassung, 1. Auflage, Version 1. 2018.
PRÁCTICA GP 2019; 14(5): 39-41