La diabetes es la causa más frecuente de enfermedad renal crónica (ERC).
La organización internacional Kidney Disease: Improving Global Outcomes (KDIGO) ha publicado recientemente nuevas directrices sobre el tratamiento de la diabetes tipo 2 en personas con ERC. Se propaga un enfoque de tratamiento basado en varios pilares. Uno de los mensajes clave: la progresión de la enfermedad renal puede ralentizarse con nuevos fármacos, de modo que muchas personas pueden ahorrarse la diálisis durante mucho tiempo.
Mientras que en el pasado sólo se disponía de unas pocas opciones de tratamiento que pudieran detener la progresión de la ERC asociada a la diabetes, en la actualidad existen varias clases modernas de fármacos que pueden ralentizar significativamente la pérdida de la función renal si se utilizan a tiempo. Por lo tanto, es importante que los afectados reciban la atención oportuna de un nefrólogo [1]. “Los criterios para presentar a la persona con diabetes mellitus al nefrólogo son, por ejemplo: descenso nuevo o significativo de la TFGe, TFGe ≤60 ml/min/1,73 m², eritrocituria o una albuminuria de grado 2 o 3”, explicó la Prof. Dra. Julia Weinmann-Menke, de Maguncia, responsable de prensa de la Sociedad Alemana de Nefrología [1,3].
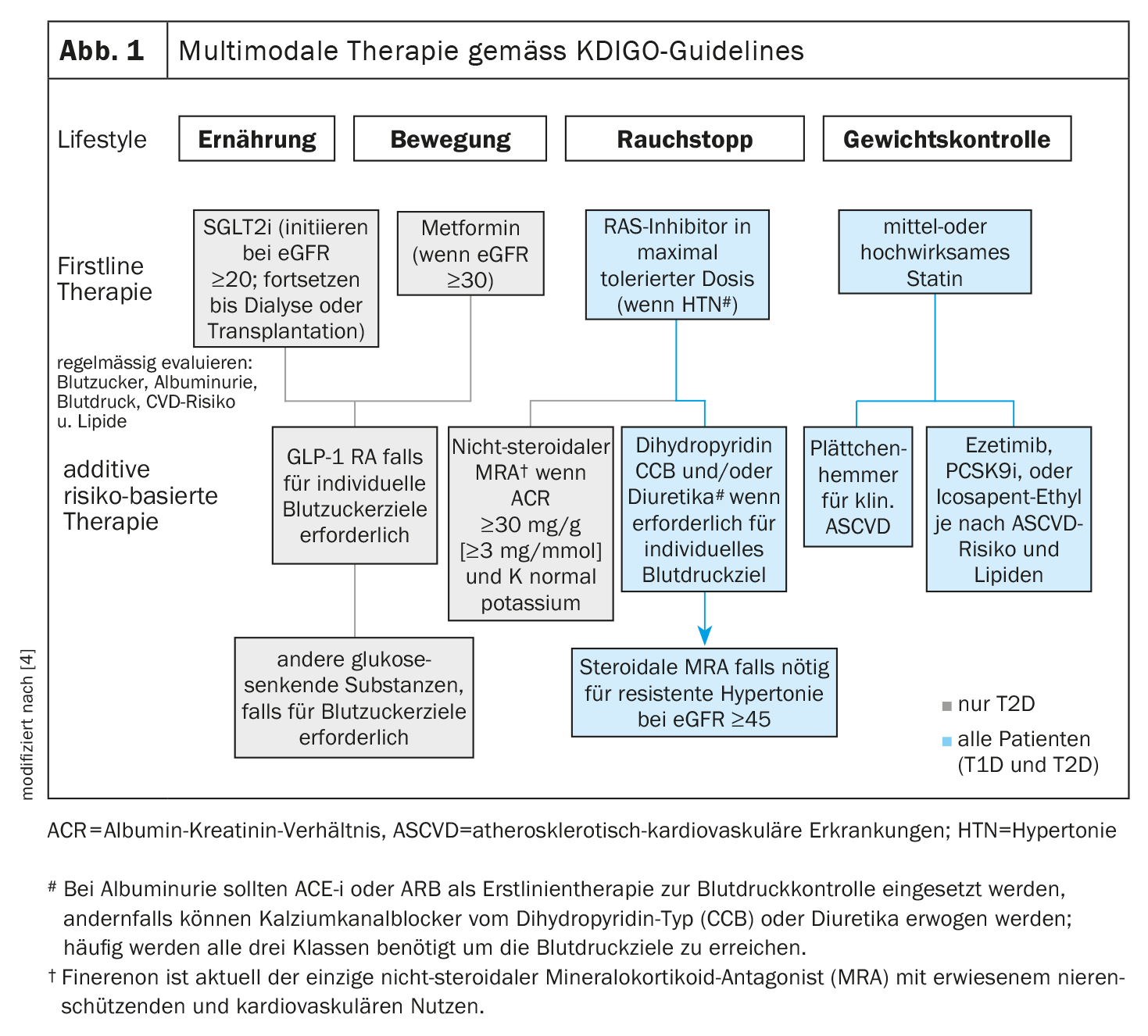
El hecho de que las directrices KDIGO publicadas en 2020 ya estén disponibles en una versión revisada en 2022 refleja el rápido progreso en el campo del tratamiento de la nefropatía asociada a la diabetes [4]. La KDIGO propugna un enfoque terapéutico multimodal (Fig. 1).
- Todos los pacientes deben prestar atención a los factores del estilo de vida como el ejercicio, la dieta y dejar de fumar. Los tratamientos farmacológicos de primera línea deben seleccionarse en función de las características clínicas individuales.
- El control de la glucemia en la diabetes de tipo 2 (T2D) se basa en una combinación de metformina e inhibidores del cotransportador 2 de sodio-glucosa (SGLT-2-i). Para los pacientes en los que el SGLT-2-i y la metformina no son eficaces para alcanzar los objetivos de glucemia, los agonistas del receptor del péptido-1 similar al glucagón (AR GLP-1) son la medicación preferida para reducir la glucosa.
- En pacientes con albuminuria e hipertensión (HTA), se aconseja la inhibición del sistema renina-angiotensina (SRA). Se recomienda una estatina para todos los pacientes con T1D o T2D y ERC.
- Puede añadirse un antagonista no esteroideo de los receptores de mineralocorticoides (ns-MRA) al tratamiento de primera línea en pacientes con T2D y un alto riesgo residual de progresión de la ERC y de episodios cardiovasculares**.
- La aspirina se utiliza generalmente para la prevención secundaria de por vida en pacientes con enfermedad cardiovascular establecida, a menos que existan contraindicaciones, y puede considerarse para la prevención primaria en pacientes con alto riesgo de enfermedad cardiovascular aterosclerótica (ECVA).
** Indicador de alto riesgo residual de progresión de la ERC y de eventos cardiovasculares: albuminuria persistente (>30 mg/g [>3 mg/mmol])

SGLT-2-i: se redujo el umbral de eGFR
Los pacientes con T2D, ERC y una TFGe ≥20 ml/min por 1,73 m² ya han sido ampliamente estudiados en ECA sobre SGLT-2-i. Basándose en estos estudios, se reitera la firme recomendación de tratar a los pacientes con T2D y ERC con un SGLT-2-i, independientemente de la albuminuria. Un cambio importante es el umbral más bajo de TFGe a partir del cual debe iniciarse el tratamiento con SGLT-2-i. La directriz de 2022 recomienda la introducción de un SGLT-2-i para los pacientes con T2D y ERC que tengan una TFGe ≥20 ml/min por 1,73 m², frente a ≥30 ml/min por 1,73 m² en la directriz de 2020 [4].

Los estudios Dapagliflozina y prevención de resultados adversos en la enfermedad renal crónica (DAPA-CKD) y Efecto de la sotagliflozina sobre los acontecimientos cardiovasculares y renales en pacientes con diabetes de tipo 2 y deterioro renal moderado con riesgo cardiovascular (SCORED) reclutó a pacientes con ERC con una TFGe de hasta 25 ml/min por 1,73 m2. [5,6].
El Estudio de Protección Cardiaca y Renal con Empagliflozina (EMPA-KIDNEY), realizado exclusivamente con poblaciones con ERC y detenido prematuramente debido a sus beneficios, también incluyó a participantes con una TFGe ≥20 ml/min por 1,73 m² [7]. Los análisis de subgrupos de estudios individuales y los metaanálisis han demostrado beneficios renales y cardiovasculares en todas las categorías de TFGe, incluidos los participantes con TFGe <30 ml/min por 1,73 m² y los que no presentan albuminuria [8,9].

Agonistas del receptor GLP-1: nuevos conocimientos
En 2021, se publicaron los resultados de un nuevo estudio a gran escala sobre la efpeglenatida, que se han incorporado a las nuevas directrices KDIGO. El estudio AMPLITUDE-O (Efecto de la efpeglenatida en los resultados cardiovasculares) respaldó las pruebas de los beneficios cardiovasculares del GLP-1 AR y reforzó la hipótesis de que el GLP-1 AR también puede mejorar los resultados renales [2]. En consecuencia, los AR GLP-1 siguen siendo la terapia de segunda línea recomendada para reducir los niveles de glucosa en sangre en la T2D y la ERC. El beneficio cardiovascular probado del GLP-1 AR se demostró para todas las categorías de TFGe y sirvió como justificación principal para recomendar el GLP-1 AR como fármaco de elección para reducir la glucemia en pacientes con T2D y ERC que no alcanzaban sus objetivos de glucemia a pesar del uso de SGLT-2-i y metformina (o en los que no se podía utilizar SGLT-2-i y/o metformina).
Finerenona – antagonista mineralocorticoide no esteroideo como último actor
También es eficaz para prevenir la progresión de la enfermedad renal diabética el nuevo antagonista selectivo de los receptores mineralocorticoides no esteroideos, la finerenona [1]. Así lo han demostrado los dos grandes ensayos clínicos FIDELIO-DKD ( Finerenone in Reducing Kidney Failure and Disease Progression in Diabetic Kidney Disease) [10] y FIGARO-DKD (Finerenone in Reducing Cardiovascular Mortality and Morbidity in Diabetic Kidney Disease) [11], así como el análisis combinado FIDELITY [12] basado en ellos. Los resultados más importantes de un vistazo:
En el ensayo FIDELIO-DKD, la finerenona redujo significativamente la incidencia tanto del resultado renal compuesto primario (insuficiencia renal, disminución sostenida de la TFGe en ≥40% o muerte por enfermedad renal; cociente de riesgo [HR]: 0,82; IC 95%: 0,73-0,93) y el resultado cardiovascular compuesto secundario (muerte por causas cardiovasculares, infarto de miocardio no mortal, ictus no mortal u hospitalización por insuficiencia cardiaca; HR: 0,86; IC 95%: 0,75-0,99). [10].
En el estudio FIGARO-DKD, la finerenona redujo significativamente el criterio de valoración cardiovascular combinado (HR: 0,87; IC 95%: 0,76-0,98) [11].
En el ensayo FIDELITY, los resultados cardiovasculares globales se redujeron en los pacientes tratados con finerenona (HR: 0,86; IC 95%: 0,78-0,95), sin heterogeneidad significativa en las características de los pacientes al inicio del estudio [12].
Los pacientes tratados con finerenona también tuvieron menos probabilidades de sufrir insuficiencia renal, una disminución de la TFGe superior al 57% o muerte renal (CRI: 0,77; IC 95%: 0,67-0,88), y menos probabilidades de sufrir insuficiencia renal definida como inicio de diálisis crónica o trasplante renal (CRI: 0,80; IC 95%: 0,64-0,99).
Literatura:
- “Día Mundial de la Diabetes: ¡La diálisis no es un destino inevitable para las personas con diabetes mellitus!”, Sociedad Alemana de Nefrología, 11.11.2022
- Gerstein HC, et al: N Engl J Med 2021; 385: 896-907.
- Documento de posición Cooperación Diabetología/Nefrología. Sociedad Alemana de Diabetes/Sociedad Alemana de Nefrología/Asociación de Nefrología Hospitalaria Senior 2018. www.ddg.info,(última consulta: 10.01.2023)
- Rossing P, et al: Resumen ejecutivo de la Guía de práctica clínica KDIGO 2022 para el tratamiento de la diabetes en la insuficiencia renal crónica: una actualización basada en las nuevas pruebas que surgen rápidamente. Kidney Int 2022; 102(5): 990-999.
- Bhatt DL, et al: N Engl J Med 2021; 384: 117-128.
- Heerspink HJL, et al: N Engl J Med 2020; 383: 1436-1446.
- Grupo de colaboración EMPA-riñón: Nephrol Dial Transplant 2022; 37; 1317-1329.
- Bakris G, et al: Clin J Am Soc Nephrol 2020; 15: 1705-1714.
- Chertow GM, et al: J Am Soc Nephrol 2021; 32: 2352-2361.
- Bakris GL, et al: N Engl J Med 2020; 383: 2219-2229.
- Pitt B, et al: N Engl J Med 2021; 385: 2252-2263.
- Rossing P, et al.: Investigadores de FIDELIO-DKD y FIGARO-DKD: Diabetes Care. Publicado en línea, 15 de agosto (2022), 10.2337/dc22-0294
- Seidu S, et al: Actualización 2022 de la declaración de posición de Primary Care Diabetes Europe: un enfoque del estado de la enfermedad para el tratamiento farmacológico de la diabetes tipo 2 en atención primaria. Prim Care Diabetes 2022; 16(2): 223-244.
- “Prurito asociado a la enfermedad renal crónica: de la epidemiología al tratamiento”, 25 nov 2021, www.emjreviews.com,(última consulta: 14 dic 2022).
- Sukul N, et al: Kidney Med 2020; 3(1): 42-53.e1
- Yan B, et al: J Am Heart Assoc 2021; 10(7): e016201.
- “CHMP Meeting Highlights February 2022”, 17/03/2022, www.basg.gv.at, (última consulta: 14/12/2022).
- Fishbane S; Investigadores del ensayo KALM-1: N Engl J Med 2020; 382(3): 222-232.
- Sociedad Americana de Nefrología: Resumen FR-OR24, www.asn-online.org (última consulta: 14 de diciembre de 2022).
PRÁCTICA GP 2023; 18(1): 20-21











