La Sociedad Europea de Nutrición Clínica y Metabolismo (ESPEN) es una organización paraguas confederativa de numerosas sociedades profesionales nacionales en el campo de la medicina nutricional. El año pasado se publicó una nueva directriz sobre micronutrientes en el contexto de la nutrición clínica. Entre otras cosas, contiene numerosas recomendaciones para la clarificación y suplementación de las vitaminas B.
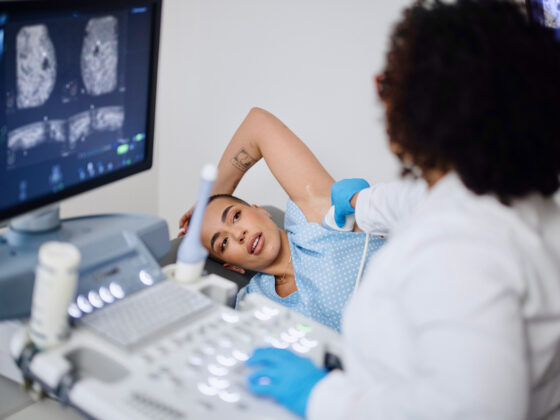
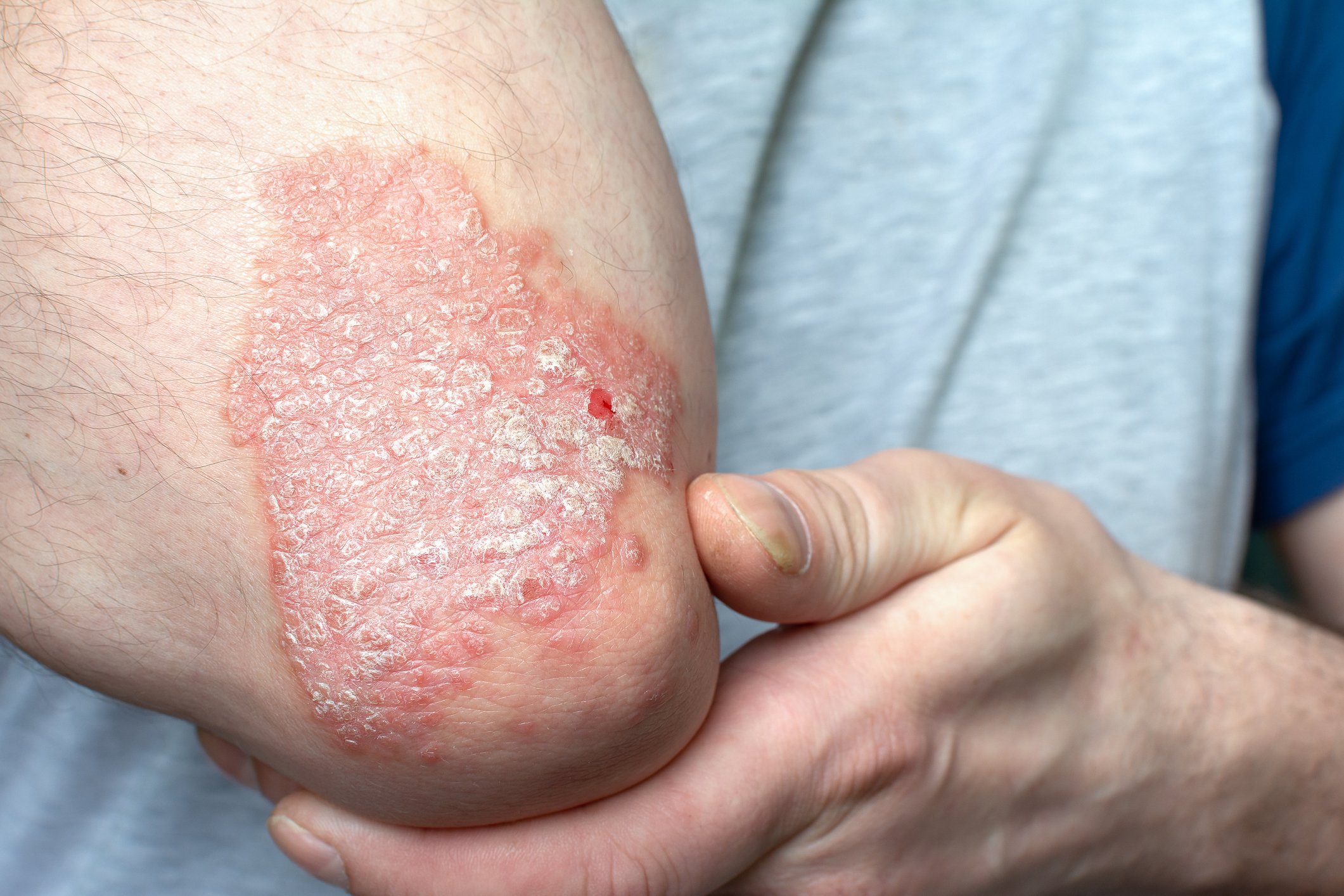
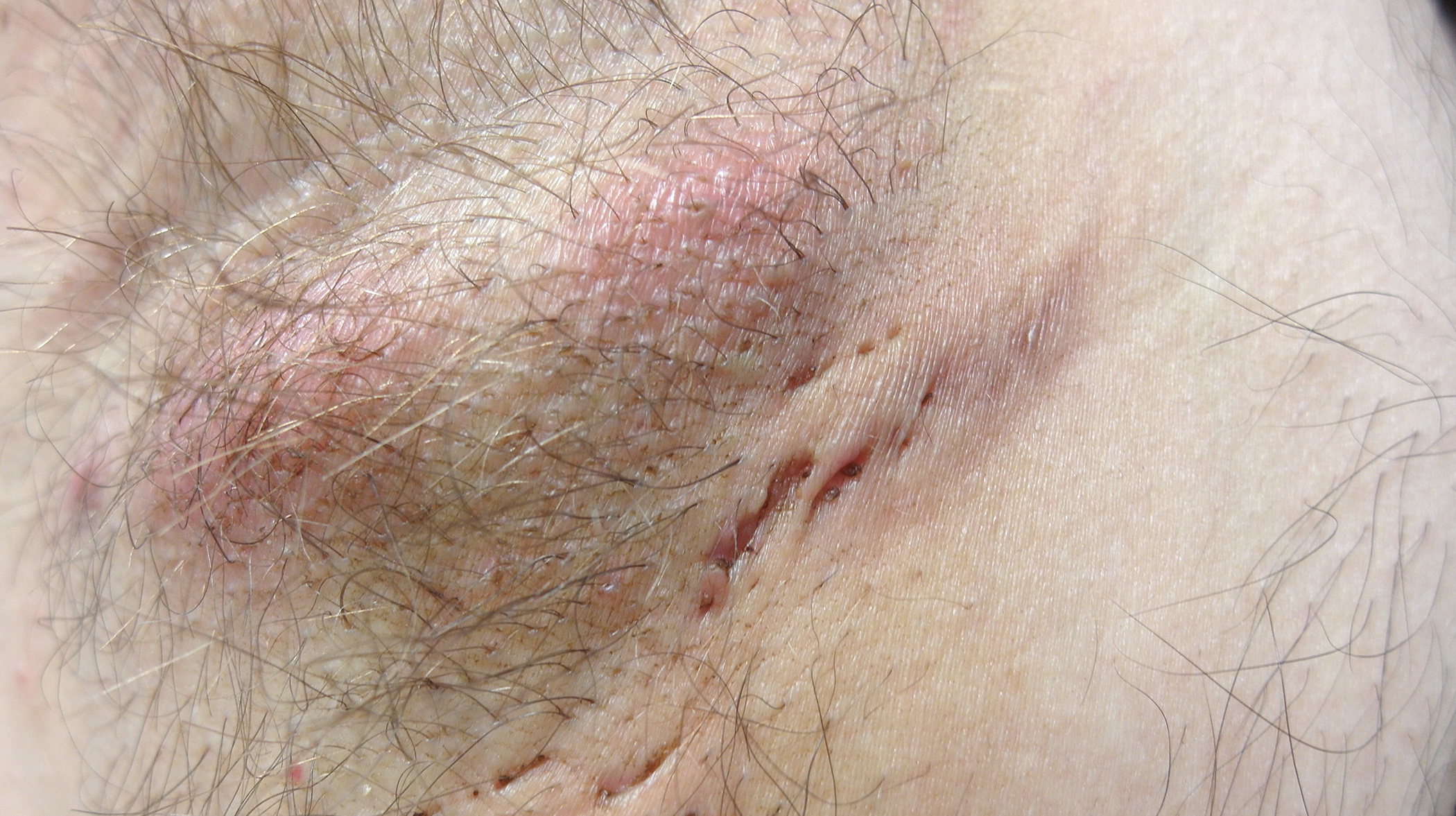
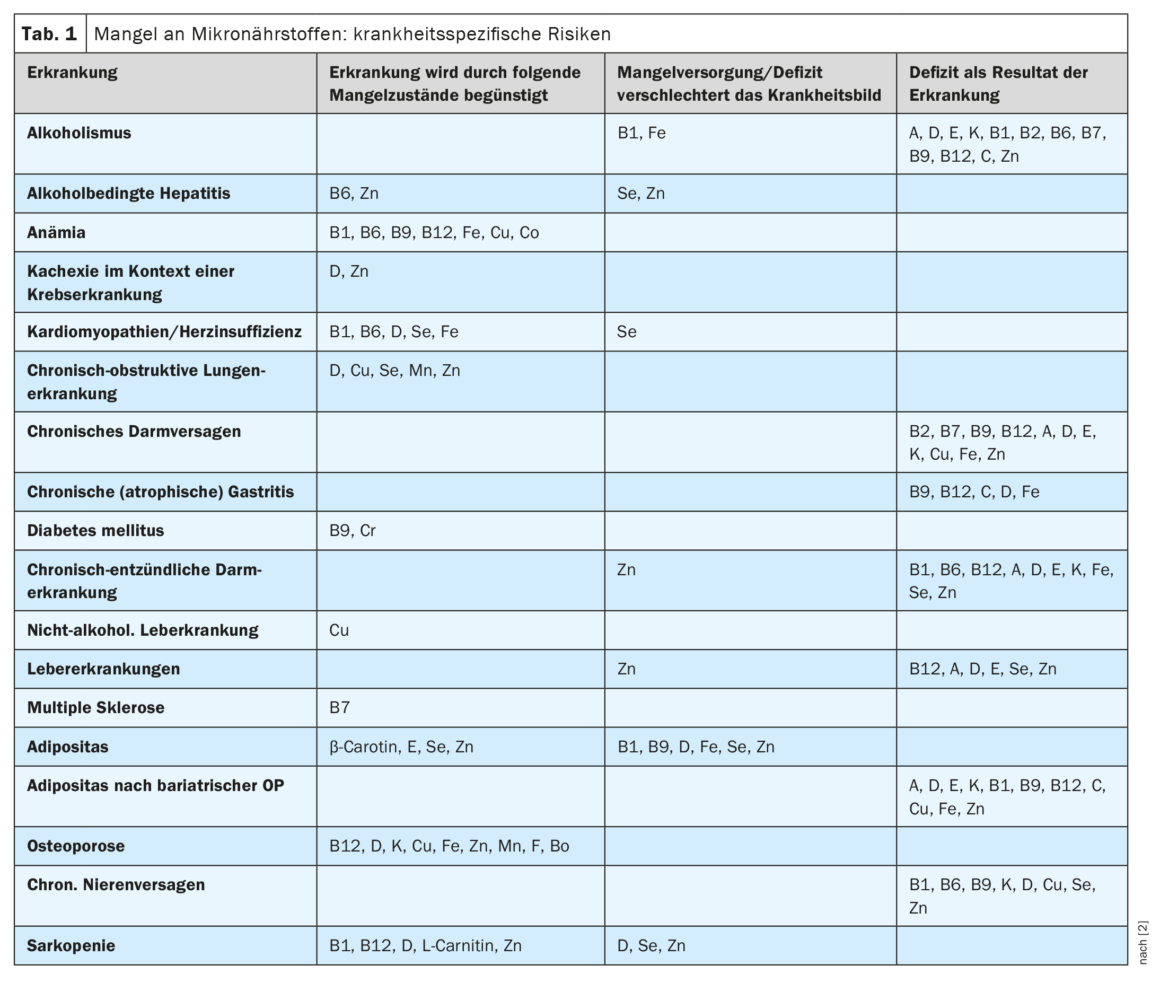
La malnutrición y la desnutrición pueden favorecer la progresión de enfermedades. Además del suministro de macronutrientes, también es importante garantizar un suministro suficiente de micronutrientes [1]. La directriz de la ESPEN, publicada el año pasado, ofrece recomendaciones prácticas para ayudar a los médicos a identificar a los pacientes con riesgo de deficiencias (tabla 1) y proporcionarles suplementos en el contexto de la nutrición enteral (alimentación oral o por sonda) o parenteral (infusión directa de soluciones nutritivas de moléculas pequeñas en el torrente sanguíneo). Además de consejos útiles sobre los factores de riesgo de la carencia de micronutrientes y las medidas de detección, también se ofrecen recomendaciones específicas sobre la dosificación de los suplementos. A continuación se comentan algunos puntos importantes sobre las vitaminas del complejo B tratados en la directriz [2].
Tiamina (vitamina B1)
La tiamina es una vitamina hidrosoluble esencial para el metabolismo de los carbohidratos y la energía [3].
¿En quién es útil determinar el estado de la tiamina?
- La tiamina puede determinarse en los eritrocitos o en la sangre total:
- Pacientes con sospecha de deficiencia asociada a cardiomiopatía y tratamiento diurético prolongado
- Pacientes sometidos a una evaluación nutricional como parte de una dieta médica prolongada y tras una cirugía bariátrica
- Síndrome de realimentación
- Encefalopatía
El estado de la tiamina se evalúa midiendo el difosfato de tiamina (ThDP) en los eritrocitos o en la sangre total. Si no es posible determinar el ThDP en los eritrocitos o en la sangre total, puede considerarse la medición de la transcetolasa eritrocitaria y su activación por la tiamina.
¿Cuándo deben administrarse cantidades adicionales?
Para los pacientes ingresados en el servicio de urgencias o en la unidad de cuidados intensivos, la directriz recomienda la administración de tiamina (100-300 mg/día por vía intravenosa) desde el ingreso durante 3-4 días. En los pacientes ingresados en planta en los que se sospeche una ingesta reducida de alimentos en los días anteriores o un consumo elevado de alcohol, debe administrarse tiamina (100-300 mg/día) por vía oral o en infusión.
¿Cómo se pueden administrar cantidades adicionales?
Dado que la tiamina se absorbe bien (excepto en la gastritis relacionada con el alcohol), pueden administrarse suplementos orales, enterales o intravenosos. Sin embargo, dada la gravedad de los síntomas agudos de carencia, lo más eficaz es la administración intravenosa de 3 x 100-300 mg al día.
| Los micronutrientes engloban un grupo heterogéneo desde el punto de vista fisiopatológico y funcional de sustancias como las vitaminas, los minerales y los oligoelementos. Investigaciones recientes demuestran la importancia de los micronutrientes en diversas patologías. Las vitaminas del complejo B intervienen en numerosas reacciones metabólicas. Las vitaminas B son cofactores (coenzimas) con cuya ayuda las enzimas catalizan las reacciones químicas. Las coenzimas son no-proteínas orgánicas que se unen a su proteína asociada (apoenzima) y juntas forman una enzima funcional (holoenzima). |
| según [2] |
Riboflavina (vitamina B2)
La riboflavina interviene en las reacciones redox y las funciones antioxidantes, en el metabolismo de otras vitaminas del grupo B (niacina, B6, B12 y folato) y en la producción de energía. La riboflavina también es necesaria para la producción normal de anticuerpos y tiene varios efectos inmunomoduladores [5]. La deficiencia nutricional aguda es poco frecuente, a menos que la riboflavina no se incluya en la formulación de micronutrientes o en el tratamiento de pacientes de alto riesgo (Tabla 1) . Es importante recordar que la deficiencia de riboflavina suele ir acompañada de deficiencias de piridoxina, folato y niacina.
¿En quién es útil la determinación del estado de la riboflavina?
La determinación del estado de la riboflavina puede ser necesaria si existe una sospecha clínicamente justificada de la presencia de una posible deficiencia. El estado de la riboflavina puede determinarse por la actividad de la glutathon reductasa en el hemograma. La determinación de la concentración de flavin adenina dinucleótido es otro método validado para la determinación de la riboflavina, especialmente en el contexto de la inflamación. El interés actual se centra en el papel que desempeña la riboflavina en la determinación de las concentraciones circulantes de homocisteína, sobre todo en pacientes con polimorfismos en el gen MTHFR como factor de riesgo de hipertensión y enfermedades cardiovasculares [6,7]. Los ensayos aleatorios en hipertensos (con y sin enfermedad cardiovascular manifiesta) homocigotos para el genotipo MTHFR 677 TT muestran que la suplementación dirigida de riboflavina (1,6 mg/día) reduce la presión arterial sistólica independientemente de la medicación antihipertensiva [8–11]. También hay pruebas de que la suplementación con altas dosis de riboflavina (400 mg) puede ser beneficiosa en la profilaxis de la migraña [12].
La nutrición enteral debe proporcionar al menos 1,2 mg de riboflavina al día en 1500 kcal. En caso de deficiencia aguda, la riboflavina se administra por vía oral en una dosis de 5-10 mg/día hasta la recuperación. La nutrición parenteral debe contener de 3,6 a 5 mg de riboflavina al día.
¿Cuándo deben administrarse cantidades adicionales?
Pueden administrarse cantidades adicionales de riboflavina en los siguientes casos:
- Deficiencia clínica sospechada o probada
- Pacientes con riesgo de deficiencia
- En pacientes con deficiencia de otras vitaminas del complejo B
- En pacientes con deficiencia de mioadenilato deaminasa, ya que algunos de ellos son sensibles a este cofactor.
¿Cómo se pueden administrar cantidades adicionales?
En caso de carencia, pueden tomarse de 5 a 10 mg/día de riboflavina por vía oral. La deficiencia clínica de riboflavina puede requerir la administración intravenosa de 160 mg de riboflavina durante cuatro días. En pacientes con deficiencia múltiple de acil-CoA deshidrogenasa (MADD), la riboflavina puede administrarse en dosis de 50-200 mg/día.
Niacina (vitamina B3)
Niacina es un término colectivo para ácido nicotínico y nicotinamida. Todos los tejidos del organismo convierten la niacina ingerida en su forma metabólicamente activa más importante, la coenzima nicotinamida adenina dinucleótido (NAD). Más de 400 enzimas necesitan NAD para catalizar reacciones en el organismo.
¿En quién es útil la determinación del estado de la niacina?
En caso de síntomas clínicos como diarrea, dermatitis y demencia (enfermedad de la pelagra), puede medirse el nivel de NAD en la sangre o en los tejidos. Alternativamente, con una muestra de sangre almacenada, se puede esperar a ver los efectos de los suplementos de niacina sobre los síntomas. La DNAD en sangre o tejidos puede utilizarse como medida del estado de la niacina.
¿Cuándo y cómo deben administrarse cantidades adicionales?
Pueden requerirse dosis más altas si se sospecha una deficiencia de niacina debido a un historial clínico de alto riesgo y/o a la presencia de signos o síntomas. La administración oral/entérica debe realizarse siempre cuando el tracto gastrointestinal sea funcional. En casos de malabsorción e intestino corto, puede optarse por la vía parenteral.
Ácido pantoténico (vitamina B5)
El ácido pantoténico es un componente de la coenzima A (CoA) y de la proteína transportadora de acilo (ACP), por lo que interviene en numerosos procesos bioquímicos de la respiración oxidativa, el metabolismo de los lípidos, la síntesis de esteroides, moléculas acetiladas (aminoácidos, carbohidratos) así como prostaglandinas [14].
¿Para quién es útil la determinación del estado del ácido pantoténico?
La directriz recomienda determinar el ácido pantoténico en la sangre. Debe considerarse una posible deficiencia de ácido pantoténico en pacientes con síntomas neurológicos. Existen pruebas de asociaciones con la enfermedad de Huntington y la enfermedad de Alzheimer.
La nutrición enteral debe proporcionar al menos 5 mg de ácido pantoténico al día con una ingesta de 1500 kcal. La nutrición parenteral debe proporcionar al menos 15 mg de ácido pantoténico al día.
¿Cuándo y cómo deben administrarse cantidades adicionales?
En el contexto de síntomas neurológicos atípicos, puede administrarse ácido pantoténico adicional junto con otras vitaminas del grupo B.
Piridoxina (vitamina B6)
El nombre de vitamina B6 hace referencia a un grupo de seis compuestos de piridina solubles en agua (vitaminas B6) que incluyen la piridoxina, la piridoxamina, el piridoxal y sus respectivas formas fosforiladas [15]. La forma biológicamente activa de la vitamina B6 es el fosfato de piridoxal, que sirve como coenzima para más de 160 reacciones enzimáticas. Estas reacciones incluyen la transaminación, la racemización, la descarboxilación y la escisión aldólica, que afectan al metabolismo de los hidratos de carbono, las proteínas y los lípidos [15]. La función más importante de la vitamina B6 activa y fosforilada en la célula está relacionada tanto con la biosíntesis como con la degradación de los aminoácidos y es fundamental en las reacciones de transaminación [16]. Otras funciones incluyen la gluconeogénesis (a través de la glucógeno fosforilasa), la unión a receptores de esteroides, la síntesis de neurotransmisores y la biosíntesis del hemo.
¿En quién es útil la determinación del estado de la pirodixina?
Si hay indicios de carencia de piridoxina, puede determinarse el estado de la vitamina B6 midiendo los niveles plasmáticos de fosfato de piridoxal (PLP). En pacientes en estado crítico o en casos de inflamación, debe medirse la PLP en los eritrocitos.
La nutrición enteral debe proporcionar al menos 1,5 mg de piridoxina al día en 1500 kcal. La nutrición parenteral debe proporcionar de 4 a 6 mg de piridoxina al día.
¿Cuándo y cómo deben administrarse cantidades adicionales?
En el contexto de una sobredosis de isoniazida o de una intoxicación glicólica, una dosis elevada de piridoxina debe formar parte de la terapia.
Biotina (vitamina B7)
La biotina se encuentra en todas las células del cuerpo humano. Desempeña un papel importante en el metabolismo de los ácidos grasos, la glucosa y los aminoácidos, ya que es un cofactor para cinco carboxilasas que son cruciales para su metabolismo [17,18]. La biotina también es un regulador de la expresión génica e influye en las funciones de las células T y las células asesinas naturales del sistema inmunitario adaptativo [16]. Unos niveles suficientes de biotina también son esenciales para el desarrollo normal del feto.
¿En quién es útil determinar el estado de la biotina?
Entre las condiciones que aumentan el riesgo de desarrollar una carencia de biotina se encuentran el consumo de alcohol, la malabsorción en el contexto de una enfermedad inflamatoria intestinal, el síndrome del intestino irritable, la enfermedad celíaca, la desnutrición grave, el tabaquismo y el embarazo. El uso prolongado de antibióticos puede destruir los microorganismos que producen biotina. Además, hay resultados de estudios que sugieren una deficiencia de biotina asociada a la falta de suplementación de pacientes alimentados por vía parenteral y existen pruebas de que el uso a largo plazo de anticonvulsivos se asocia a una peor absorción y a una mayor necesidad de biotina [2].
El estado de la biotina puede obtenerse en presencia de síntomas clínicos que sugieran una deficiencia de biotina (por ejemplo, dermatitis, caída del cabello o síntomas neurológicos) y un historial que sugiera una ingesta inadecuada. El estado de la biotina se determina mediante la medición directa de la biotina en sangre y orina y debe complementarse con la determinación de la actividad de la biotinidinasa.
En nutrición enteral, deben suministrarse al menos 30 μg de biotina al día en 1500 kcal. Para la nutrición parenteral, los suplementos vitamínicos deben proporcionar 60 μg de biotina al día.
¿Cuándo y cómo deben administrarse cantidades adicionales?
Las madres lactantes deben recibir una ingesta oral de al menos 35 μg de biotina al día. La suplementación también puede ser necesaria en pacientes con terapia de sustitución renal. Pueden administrarse cantidades adicionales de biotina por vía oral, enteral o intravenosa, dependiendo de la función intestinal.
Folato y ácido fólico (vitamina B9)
Folato es un término genérico que se refiere a una familia de moléculas que varían en función de su estado de oxidación, la naturaleza química de las unidades C1 y la longitud de la cadena lateral de glutamato [20].
¿En quién es útil determinar el estado de la vitamina B9?
En pacientes con anemia macrocítica o con riesgo de desnutrición, el estado del ácido fólico debe medirse al menos una vez en la evaluación inicial y repetirse a los tres meses de la suplementación para comprobar su normalización. El ácido fólico y la vitamina B12 suelen medirse ambos cuando se realizan pruebas para detectar la anemia. En el caso de las enfermedades que se sabe que aumentan la necesidad de ácido fólico, el estado del ácido fólico puede medirse cada 3 meses hasta la estabilización y después una vez al año.
El estado del ácido fólico debe determinarse en plasma o suero (estado a corto plazo) o en eritrocitos (estado a largo plazo) utilizando un método validado frente al ensayo microbiológico. El método de referencia para medir el folato es la prueba microbiológica con L. rhamnosus. El análisis simultáneo de la homocisteína mejora la interpretación de las mediciones de laboratorio. El nivel A está respaldado por pruebas bioquímicas.
La nutrición enteral debe proporcionar 330-400 μg de equivalente de folato dietético (EFD) al día en 1500 kcal. La nutrición parenteral debe proporcionar 400-600 μg de ácido fólico al día.
¿Cuándo y cómo deben administrarse cantidades adicionales?
En caso de deficiencia alimentaria o de hemodiálisis crónica, pueden administrarse de 1 a 5 mg de ácido fólico al día por vía oral. En caso de deficiencia, debe administrarse por vía oral durante cuatro meses, o hasta que se corrija la causa de la deficiencia. Cuando los síntomas clínicos se hayan resuelto y los recuentos sanguíneos se hayan normalizado, debe administrarse una dosis de mantenimiento, es decir, unos 330 μg DFE (equivalente de folato dietético) para adultos y 600 μg DFE para mujeres embarazadas y lactantes, al día.
En pacientes en hemodiálisis crónica con hiperhomocisteinemia, pueden ser necesarias cantidades más elevadas durante periodos más largos: 5 mg o más de ácido fólico al día en pacientes no diabéticos y 15 mg al día en pacientes diabéticos [21,22].
Para prevenir los defectos del tubo neural, las mujeres en edad fértil o las que no toman anticonceptivos orales y viven en países donde los alimentos básicos no están enriquecidos con ácido fólico deben tomar suplementos de ácido fólico (400 μg/día) periconceptualmente/en edad fértil. Se recomienda tomar cantidades adicionales de ácido fólico por vía oral. En caso de tratamiento oral ineficaz o de intolerancia, puede administrarse alternativamente ácido fólico (0,1 mg/día) por vía subcutánea, intravenosa o en infusión.
Cobalamina (vitamina B12)
La vitamina B12 (cobalamina) es un micronutriente hidrosoluble esencial sintetizado por hongos y microorganismos y en el estómago de los rumiantes en función del contenido en cobalto del suelo [23].
¿En quién es útil determinar el estado de la cobalamina?
La carencia de cobalamina debe descartarse en todos los pacientes que presenten anemia o macrocitosis aislada y que hayan sido diagnosticados de polineuropatías, enfermedades neurodegenerativas o psicosis. En todos los pacientes de riesgo o en tratamiento con cobalamina, la adecuación de la ingesta debe revisarse al menos una vez al año en función de la desaparición de los síntomas clínicos y de los marcadores de laboratorio disponibles.
Los pacientes adultos con riesgo o sospecha de deficiencia de cobalamina deben someterse a un cribado con la combinación de al menos dos biomarcadores (holotranscobalamina, ácido metilmalónico), con la cobalamina sérica como sustituto. Los pacientes con enfermedades autoinmunes o con glositis, anemia y neuropatía deben someterse a pruebas de detección de la anemia perniciosa en presencia de anticuerpos antifactor intrínseco, independientemente de los niveles de cobalamina.
La nutrición enteral debe proporcionar al menos 2,5 μg de cianocobalamina al día en 1500 kcal. La nutrición parenteral debe proporcionar al menos 5 μg de cianocobalamina al día.
¿Cuándo y cómo deben administrarse cantidades adicionales?
Para las madres lactantes, se recomienda una ingesta oral de al menos 2,8 μg de cianocobalamina al día. Los pacientes con problemas de absorción de cobalamina deben recibir suplementos de por vida, ya sea en forma de una dosis diaria de 350 μg de cobalamina o como una inyección IM de 1000-2000 μg de cobalamina cada 1-3 meses. La administración intranasal y sublingual son vías alternativas [19].
En caso de síntomas clínicos agudos de deficiencia, anticuerpos contra el factor intrínseco, antecedentes de gastrectomía total o enfermedad malabsortiva continua, la administración debe ser por infusión, comenzando con dosis altas de 1000 μg de cobalamina en días alternos durante quince días (o diariamente durante cinco días).
El tratamiento debe continuarse al menos dos veces al mes hasta que hayan desaparecido todos los síntomas clínicos y/o los factores etiopatogénicos (incluida la macrocitosis). La monitorización del potasio en sangre debe realizarse como parte de la terapia de saturación.
Literatura:
- Hauner, H et al: Leitfaden Ernährungstherapie in Klinik und Praxis (LeKuP). En: Current Nutritional Medicine 2019; 44: 384-419.
- Berger MM, et al: Directriz ESPEN sobre micronutrientes. Clin Nutr 2022; 41(6): 1357-1424.
- Johnson CR, et al: Deficiencia de tiamina en países de ingresos bajos y medios:trastornos, prevalencias, intervenciones previas y recomendaciones actuales. Nutr Health 2019; 25: 127e51.
- “La carencia de tiamina y su prevención y control en las grandes emergencias”. Ginebra: OMS; 1999. www.who.int/publications/i/item/WHO-NHD-99.13,(última consulta: 20.03.2023).
- Packer M: Cardiomiopatía por cobalto: una reevaluación crítica a la luz de un reciente resurgimiento. Circ Heart Fail 2016: 9.
- Powers HJ: Riboflavina (vitamina B-2) y salud. Am J Clin Nutr 2003; 77: 1352e60.
- McNulty H, et al: Riboflavina, genotipo MTHFR y presión arterial: un enfoque personalizado para la prevención y el tratamiento de la hipertensión. Mol Aspect Med 2017; 53: 2e9.
- Horigan G, et al: La riboflavina reduce la presión arterial en pacientes con enfermedades cardiovasculares homocigotos para el polimorfismo 677C->T en la MTHFR. J Hypertens 2010; 28: 478e86.
- Wilson CP, et al: La riboflavina ofrece una estrategia específica para controlar la hipertensión en pacientes con el genotipo MTHFR 677TT: un seguimiento de 4 años. Am J Clin Nutr 2012; 95: 766e72.
- Wison CP, et al: Blood pressure in treated hypertensive individuals with the MTHFR 677TT genotype is responsive to intervention with riboflavin: findings of a targeted randomized trial. Hipertensión 2013; 61: 1302e8.
- Psara E, Pentieva K, Ward M, McNulty H: Revisión crítica de la nutrición, la presión arterial y el riesgo de hipertensión a lo largo del ciclo vital: ¿juegan algún papel las vitaminas B? Bioquímica 2020; 173: 76e90
- Schoenen J, Jacquy J, Lenaerts M: Eficacia de las dosis altas de riboflavina en la profilaxis de la migraña. Un ensayo controlado aleatorio. Neurología 1998; 50: 466e70
- Comité Permanente del Instituto de Medicina (IOM). Ingestas dietéticas de referencia de tiamina, riboflavina, niacina, vitamina B6, folato, vitamina B12, ácido pantoténico, biotina y colina. En: (US) NAP, editor. Ingestas dietéticas de referencia de tiamina, riboflavina, niacina, vitamina B6, folato, vitamina B12, ácido pantoténico, biotina y colina. Washington (DC); 1998.
- Trumbo P: Ácido pantoténico. En: AC R, B C, Cousins RJ, Tucker KL, Ziegler TR (Eds). La nutrición moderna en la salud y la enfermedad. 11ª ed. Baltimore, MD: Lippincott Williams & Wilkins; 2014. P. 351e7
- Oppici E, et al.: La piridoxamina y el piridoxal son más eficaces que la piridoxina en el rescate de variantes defectuosas de plegamiento de la alanina:glioxilato aminotransferasa humana causante de hiperoxaluria primaria tipo I. Hum Mol Genet 2015; 24: 5500e11.
- Parra M, Stahl S, Hellmann H: La vitamina B(6) y su papel en el metabolismo y la fisiología celular. Células 2018: 7.
- Agrawal S, Agrawal A, Said HM: La deficiencia de biotina aumenta la respuesta inflamatoria de las células dendríticas humanas. Am J Physiol Cell Physiol 2016; 311: C386e91.
- Gifford JL, de Koning L, Sadrzadeh SMH: Estrategias para mitigar el riesgo que supone la interferencia de la biotina en los inmunoensayos clínicos. Clin Biochem 2019; 65: 61e3.
- Shankar P, Boylan M, Sriram K. Deficiencias de micronutrientes tras la cirugía bariátrica. Nutrición 2010;26:1031e7
- Scaglione F, Panzavolta G: El folato, el ácido fólico y el 5-metiltetrahidrofolato no son lo mismo. Xenobiotica 2014; 44: 480.
- Capelli I, et al: Administración de ácido fólico y vitamina B12 en la ERC, ¿por qué no? Nutrientes 2019: 11.
- Angelini A, et al.: La relación entre la homocisteína, el ácido fólico y la vitamina B12 en las enfermedades renales crónicas. G Ital Nefrol 2021; 38: 2021
- Jarquin Campos A, et al.: Precisión diagnóstica de la holotranscobalamina, la vitamina B12, el ácido metilmalónico y la homocisteína en la detección de la deficiencia de B12 en una amplia población mixta de pacientes. Dis Markers 2020; 2020: 7468506.
PRÁCTICA GP 2023; 18(4): 15-19